Введение
Анемиями страдают 825 млн женщин и 444 млн мужчин во всем мире, что определяет медико-социальную значимость данного полиэтиологического состояния, характеризующегося уменьшением содержания гемоглобина (Hb) и/или количества эритроцитов в единице объема крови, что приводит к тканевой гипоксии [1, 2]. Более половины случаев анемии (66,2%) приходится на железодефицитную анемию (ЖДА), развитие которой связано с алиментарными причинами (недостаточное потребление железа, особенно при повышенной в нем потребности у детей, подростков и женщин во время беременности), нарушением усвоения железа (вследствие дефицита витамина В12 или фолиевой кислоты) или его потерей вследствие кровотечений [1–4]. Возникновение системных нарушений при ЖДА определяется многообразием функциональных свойств железа (клеточное дыхание, окислительное фосфорилирование, рост и дифференцировка нервной ткани) [3, 4].
Второе место по распространенности занимают врожденные наследственные гемолитические анемии (ГА), при которых происходит усиленное разрушение эритроцитов с накоплением продуктов их распада в крови [1, 2, 5, 6]. Разновидностью ГА, поражающей 1–2% населения мира и связанной с нарушением синтеза одной из четырех цепей глобина, гемолизом, микро-, анизоцитозом эритроцитов и эритропенией при нормальном или повышенном уровне ферритина в плазме крови, являются талассемии [1, 5, 6]. Гомозиготная (большая) β-талассемия (БТ) требует регулярных гемотрансфузий, проведения хелаторной терапии (для связывания и выведения избыточного железа) и проявляется дисфункцией различных органов и систем, включая орган зрения, вследствие гипоксии, токсического воздействия продуктов гемолиза и избыточного железа (абсорбционная и трансфузионная перегрузка) [5, 6].
Считается, что офтальмологические проявления развиваются примерно у трети пациентов с анемиями. Клиническая манифестация офтальмологических проявлений анемии сопровождается снижением зрительных функций и изменениями картины глазного дна, которые могут включать ангиопатию («штопорообразная» извитость артериол, расширение и извитость вен), ретинопатию (геморрагии в наружных и внутренних слоях сетчатки, «мягкие» и «твердые» экссудаты, изменения ретинального пигментного эпителия, ишемическая ретинопатия, макулярный отек), оптическую нейропатию, а в отдельных случаях — тромбоз центральной вены сетчатки, непроходимость центральной артерии сетчатки и ишемическую оптическую нейропатию [4, 7, 8]. В связи с этим актуальной научно-практической задачей является оптимизация своевременной диагностики ранних, в том числе доклинических, микроциркуляторных изменений сетчатки у пациентов с анемией без снижения зрительных функций и офтальмоскопических признаков патологии, что по предложению ряда авторов может быть обозначено термином «доклиническая ретинопатия» (ДР) [9, 10]. Успешное решение этой задачи даст возможность осуществлять мониторинг состояния сетчатки у пациентов с анемиями и минимизировать риски клинической манифестации офтальмологических проявлений. Ценным диагностическим инструментом, позволяющим объективно оценивать морфометрические параметры сетчатки, является метод оптической когерентной томографии с ангиографией (ОКТА). Вместе с тем в доступной научной литературе представлены единичные публикации, отражающие изменения ОКТА-параметров сетчатки (биомаркеры) при ЖДА и БТ у детей, что определило актуальность и цель нашего исследования.
Цель исследования: изучить морфометрические параметры сетчатки у детей с ЖДА и БТ при помощи методики ОКТА и выявить биомаркеры ДР.
Материал и методы
Были обследованы 90 детей (180 глаз) в возрасте 7–18 лет (36 мальчиков, 54 девочки): 30 здоровых детей и 60 детей с анемиями. Дизайн: проспективное обсервационное одномоментное исследование «случай — контроль». В 1-ю группу (контроль) вошли 30 здоровых детей без признаков гематологической и офтальмологической патологии. Во 2-ю группу включили 30 детей с ЖДА, а в 3-ю группу — 30 детей с БТ.
Критерии включения: возраст 7–18 лет; максимальная корригированная острота зрения (МКОЗ) ≥0,8; уровень Hb ≤110 г/л; для 2-й группы — подтвержденный диагноз ЖДА; для 3-й группы — подтвержденный диа-гноз гомозиготной (большой) БТ, уровень ферритина ≥1000 мкг/л, регулярная гемотрансфузионная терапия (1 раз в 4–6 нед.), получение хелаторной терапии.
Критерии исключения: офтальмоскопические признаки ретинопатии или нейропатии; аномалии рефракции со сферическим и/или цилиндрическим компонентами >3,0 диоптрий; аксиальная длина глазного яблока >25 мм; непрозрачность оптических сред; офтальмогипертензия; глаукома. Для исключения завышения значимости различий между группами сравнения в статистический анализ включали результаты обследования правого глаза [11]. Исследование проводилось на клинической базе кафедры офтальмологии БухГосМИ (Республиканский специализированный научно-практический центр «Микрохирургия глаза») и в отделении детской гематологии Областного многопрофильного медицинского центра в 2024–2025 гг. У родителей детей, включенных в исследование, получали информированное согласие. Все диагностические процедуры соответствовали положениям Хельсинкской декларации (1964 г.) и ее более поздним поправкам, а также стандартам этического комитета БухГосМИ.
У всех наблюдавшихся проводили: стандартное офтальмологическое обследование (МКОЗ, кераторефрактометрию, пневмотонометрию, биомикроскопию, офтальмоскопию, статическую автоматизированную периметрию с оценкой среднего отклонения светочувствительности (MD) и отклонения паттерна (PSD)); оценку гематологических показателей (уровень Hb, средний корпускулярный объем эритроцитов — MCV, уровень ферритина); ОКТА (спектральный доменный томограф Optopol Revo FC). В ходе ОКТА определяли параметры фовеальной аваскулярной зоны (ФАЗ) и сосудистую плотность (СП, %) капиллярных сплетений сетчатки (площадь сканирования 3×3 мм, центрация на область фовеолы). Параметры ФАЗ включали: площадь (мм2), периметр (мм) и индекс циркулярности (ИЦ, в долях единицы), представляющий собой кратное периметра ФАЗ пациента к периметру идеального круга с такой же площадью. СП оценивали в поверхностном капиллярном сплетении (ПКС) и глубоком капиллярном сплетении (ГКС): в зоне 3×3 мм (total), верхней и нижней половинах области сканирования, фовеальной области и парафовеа.
Статистические методы включали: расчет среднего (M) и его стандартного отклонения (SD); оценку достоверности различий (критерии Манна — Уитни, Краскела — Уоллиса, Фишера); расчет коэффицента корреляции Пирсона; бинарную логистическую регрессию с ROC-анализом (для определения наиболее целесообразных диагностических биомаркеров ДР). Различия считали статистически значимыми при р<0,05. Для статистической обработки использовали приложение SPSS DATAtab (2025).
Результаты исследования
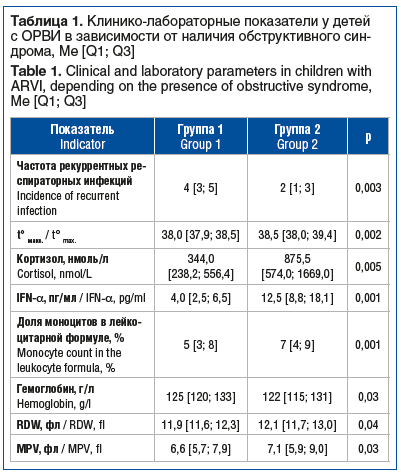
Демографические показатели пациентов в группах сравнения не имели статистически значимых различий, что позволяет говорить об их сопоставимости (табл. 1).

У детей с ЖДА (табл. 2) определялось достоверное снижение уровней Hb, ферритина и показателя MCV. У детей с БТ значимым было снижение уровней Hb и MCV, а также повышение уровня ферритина.

Результаты оценки функциональных показателей органа зрения у лиц, включенных в исследование (табл. 3), свидетельствуют о том, что МКОЗ и индекс PSD не имели значимых отличий в группах сравнения. Тенденция к ухудшению индекса MD у детей с ЖДА без офтальмоскопических признаков ретинопатии оказалась незначимой. У детей с БТ без клинических признаков ретинопатии снижение индекса MD было достоверным, однако значения показателя оставались в граничных значениях нормы (> -3,0 dB) у большинства пациентов (74%).

Результаты сравнительной оценки морфометрических ОКТА-параметров сетчатки у детей в условиях нормы и при анемиях без офтальмоскопических признаков ретинопатии представлены в таблице 4 и на рисунке.

У детей с ЖДА была отмечена тенденция к меньшим значениям площади и периметра ФАЗ сравнительно со здоровыми детьми. Вместе с тем у детей с ЖДА была зафиксирована достоверно меньшая величина ИЦ ФАЗ (0,5±0,05; р<0,001) сравнительно c контролем (0,63±0,05). Между величиной ИЦ ФАЗ и уровнем Hb отмечалась положительная корреляция (r=0,54; р=0,002). Также у детей с ЖДА была выявлена достоверно меньшая СП-ПКС (включая зоны: 3×3 мм — total, верхнюю и нижнюю половины зоны сканирования, нижнюю половину парафовеа). Наиболее значимым оказалось снижение СП-ПКС total (37,3±0,95%; р=0,001) относительно контроля (38,5±1,1%). Тенденция к снижению СП-ГКС у детей с ЖДА была недостоверной. Анализ возможности применения ОКТА-биомаркеров у детей с ЖДА показал, что оценка ИЦ ФАЗ (при пороге отсечения 0,55) позволяет выявлять доклинические микроциркуляторные нарушения сетчатки (ДР) с чувствительностью 73,33% и специфичностью 70% (AUC=0,73), в то время как оценка СП-ПКС total (порог отсечения 37,5%) дает возможность диагностировать ДР с чувствительностью 56,67% и специфичностью 70% (AUC=0,66). У детей с БТ, сравнительно с контролем, были выявлены значимые изменения всех параметров ФАЗ, включая увеличение ее площади и периметра, а также снижение ИЦ (см. табл. 4). Наиболее значимым различием при БТ оказалась меньшая величина ИЦ ФАЗ (0,45±0,06; р<0,001). Также у детей с БТ определялось значимое снижение СП во всех оцениваемых зонах обоих капиллярных сплетений. Наиболее значимым было снижение СП-ПКС total (36,15±1,69%; р<0,001). При БТ снижение ИЦ ФАЗ и СП-ПКС total показало положительную корреляцию со снижением уровня Hb (r>0,55; р<0,05) и отрицательную корреляцию с повышением уровня ферритина (r>-0,5; р<0,05). Оценка возможности использования ОКТА-биомаркеров для диагностики ДР у детей с БТ продемонстрировала: для ИЦ ФАЗ (порог отсечения 0,55): чувствительность 70%, специфичность 83% (AUC=0,82); для СП-ПКС total (порог отсечения 37,5%): чувствительность 76,67%, специфичность 83,3% (AUC=0,88).

Обсуждение
В нашем исследовании у детей с ЖДА без офтальмоскопических признаков ретинопатии была выявлена тенденция к меньшим значениям площади и периметра ФАЗ по сравнению с контролем, что, по мнению Y. Wu et al. [12], может быть обусловлено активацией компенсаторных механизмов в условиях анемии. Эта тенденция оказалась незначимой, что, по-видимому, было обусловлено высокой вариабельностью указанных ОКТА-параметров как в условиях нормы, так и при ЖДА. Полученные результаты соотносятся с данными M.F. Korkmaz et al. [13] (обследовавших лиц с ЖДА того же гендерного и возрастного состава), а также S. Koca et al. [14] (обследовавших лиц с ЖДА 42,9±9,4 года), однако отличаются от данных Y. Wu et al. (включивших в свое исследование беременных женщин молодого возраста с ЖДА, у которых было зафиксировано значимое снижение рассматриваемых показателей относительно нормы) [12]. Вместе с тем у детей с ЖДА нами было отмечено снижение ИЦ ФАЗ вследствие изменений ее формы. Необходимо отметить, что изменение формы (контура) ФАЗ может быть связано с окклюзией и ремоделированием мелких капилляров в условиях ишемии, а снижение ИЦ ФАЗ может быть биомаркером ранних и доклинических микроциркуляторных изменений сетчатки [10, 15, 16]. Помимо этого, в нашем исследовании было выявлено достоверное снижение СП-ПКС, что также может быть признаком доклинических микроциркуляторных нарушений [9, 10, 12–17]. Выявление точного механизма развития микроциркуляторных нарушений сетчатки при ЖДА требует проведения дальнейших исследований, однако считается, что он связан со снижением уровня Hb и хронической тканевой гипоксией (что соотносится с данными о положительной корреляции между ИЦ и Hb в нашем исследовании), а также с уменьшением способности к деформации микроцитарных эритроцитов, что создает условия для гиперкоагуляции и повреждения капиллярного русла [4, 18–20].
У детей с большой БТ без офтальмоскопических признаков ретинопатии нами были отмечены достоверно большие, чем в контроле, значения площади и периметра ФАЗ, меньшие значения ИЦ ФАЗ и значимое снижение СП-ПКС и СП-ГКС, что, по данным ряда авторов, является проявлением доклинических микроциркуляторных изменений сетчатки [10, 15, 16, 21]. Полученные нами данные соотносятся с результатами G. Cennamo et al. [22], обследовавших пациентов среднего возраста с большой БТ, получающих регулярную гемотрансфузионную и хелаторную терапию. Изменения морфометрических ОКТА-параметров сетчатки при БТ оказались более выраженными, чем при ЖДА (см. табл. 4). По-видимому, это было связано со значительным повышением уровня ферритина относительно показателей нормы, а также с достоверно меньшим уровнем Hb на фоне проводимой терапии в сравнении с больными с ЖДА (см. табл. 2). Влияние указанных факторов на состояние микроциркуляции сетчатки подтверждается значимой положительной корреляцией между ИЦ ФАЗ, СП-ПКС total и уровнем Hb, а также отрицательной корреляцией между ИЦ ФАЗ, СП-ПКС total и уровнем ферритина. Выявленные в нашем исследовании изменения ОКТА-параметров у детей с ЖДА и БТ без офтальмоскопических признаков ретинопатии могут свидетельствовать о присутствии у них доклинических микроциркуляторных нарушений сетчатки (ДР). Бинарная логистическая регрессия и ROC-анализ показали, что наиболее целесообразными ОКТА-биомаркерами ДР у детей с анемиями могут быть: при ЖДА — снижение ИЦ ФАЗ (порог отсечения 0,55); при БТ — снижение СП-ПКС (порог отсечения 37,5%).
Корреляция микроциркуляторных нарушений сетчатки с гематологическими параметрами при анемиях дает основание считать главным направлением лечебного воздействия у этой категории пациентов нормализацию картины крови [4, 7, 8, 20]. Вместе с тем реализация этой стратегии далеко не всегда является простой задачей, особенно у пациентов с БТ, у которых, помимо снижения уровня Hb, фиксируются высокие значения ферритина (абсорбционная и трансфузионная перегрузка), что отягощает микроциркуляторные и ишемические нарушения сетчатки, а также вызывает ее нейродегенеративные изменения [7, 8]. В свою очередь, хелаторная терапия, направленная на связывание и выведение «избыточного железа» при БТ, по данным ряда авторов, также может усугублять микроциркуляторные нарушения, хроническую тканевую гипоксию и процессы нейродегенерации [7, 8, 20]. Необходимо отметить, что в ранее проводившихся исследованиях было описано истончение сетчатки в фовеальной и парафовеальной зонах, комплекса ганглиозных клеток и слоя нервных волокон сетчатки у пациентов с ЖДА и БТ без офтальмоскопических признаков ретинопатии, что указывает на ранние нейродегенеративные изменения при ДР [9, 22–25]. В связи с этим, несмотря на проводимое гематологическое лечение, у части пациентов с анемиями происходит клиническая манифестация ретинопатии и/или нейропатии, что приводит к снижению зрительных функций и ухудшению качества жизни [4, 7, 8]. По нашему мнению, приведенные факты определяют актуальность дальнейшей оптимизации подходов к своевременному выявлению и мониторингу ранних изменений сетчатки у детей с анемиями, а также к лечебному воздействию, направленному на купирование микроциркуляторных и нейродегенеративных нарушений, в том числе путем проведения ретинопротекторной терапии (РПТ). Перспективными фармакологическими агентами для РПТ могут быть так называемые нейропептиды — щелочные полипептиды с молекулярной массой 1000–10 000 Да, полученные методом кислотной экстракции из тканей сетчатки и головного мозга крупного рогатого скота [26].
Препараты пептидной природы (пептидные биорегуляторы или цитомедины) занимают особое положение между малыми молекулами и белками, представляют собой внутренние сигнальные молекулы, которые регулируют физиологические функции клеток в составе тканей, органов и систем организма [27, 28]. Благодаря этим особенностям пептиды могут действовать как нейромедиаторы, гормоны, факторы роста или лиганды ионных каналов. Связываясь со специфическими рецепторами клеточной поверхности или с ионными каналами, пептиды запускают каскады внутриклеточных эффектов, восполняющих отсутствующие функции клеток. Важным свойством препаратов пептидной природы является их тканеспецифичность, позволяющая оказывать эффекты на уровне определенных тканей как в регуляции физиологических процессов, так и при проведении лечебного воздействия [26–28].
Для проведения РПТ в Российской Федерации был разработан и успешно применяется в офтальмологической практике препарат на основе комплекса водорастворимых полипептидных фракций с молекулярной массой ≤10 000 Да, выделенных из сетчатки крупного рогатого скота (Ретиналамин®) [26, 29–32]. Механизм действия препарата связан с его способностью улучшать метаболизм тканей глаза, нормализовывать функции клеточных мембран, стимулировать внутриклеточный синтез белка и регулировать процессы перекисного окисления липидов [29–33]. Исследование лиганд-рецепторного взаимодействия лио-филизата Ретиналамина с исследуемыми мишенями in vitro (метод конкурентного радиолигандного связывания) показало, что препарат, взаимодействуя с AMPA-, NMDA- и mGluR1-рецепторами, оказывает прямой нейропротективный эффект при ретинопатии и глаукоме [26]. Доказанные в многочисленных доклинических и клинических исследованиях эффекты Ретиналамина включают: нормализацию реологических свойств крови, проницаемости сосудистой стенки и состояния микроциркуляции в условиях ишемии сетчатки (ангиопротекция); стимулирующее воздействие на нейроэпителий и глиальные клетки сетчатки, улучшение функционального взаимодействия пигментного эпителия и наружных сегментов фоторецепторов, стимуляцию репаративных процессов, снижение глутаматной нейротоксичности (ретинопротекция); уменьшение проявлений местной воспалительной реакции [26, 29–33]. Одной из важных особенностей Ретиналамина является его применение у взрослых и детей короткими курсами в течение 10 дней в виде внутримышечных инъекций или парабульбарно, при этом в исследованиях было показано, что он проникает в ткани глаза и оказывает пролонгированный эффект, а повторные курсы через 3–6 мес. обладают потенцирующим эффектом, повышая эффективность РПТ [26, 29–33]. С учетом многолетнего опыта эффективного и безопасного использования Ретиналамина в качестве ретинопротекторного лекарственного препарата у пациентов с глаукомой, возрастной макулярной дегенерацией, миопией, непролиферативной диабетической ретинопатией, абиотрофией сетчатки и другими видами ретинопатий представляется целесообразным его применение и у пациентов с анемиями.
Заключение
Оптическая когерентная томография с функцией ангио-графии позволила выявить микроциркуляторные изменения сетчатки у детей с анемией без офтальмоскопических признаков ретинопатии. При ЖДА наиболее чувствительным ОКТА-биомаркером ДР оказался индекс циркулярности ФАЗ (площадь под кривой — AUC=0,73; порог отсечения 0,55; чувствительность 73,33%, специфичность 70%). У детей с большой БТ наиболее чувствительным ОКТА-биомаркером ДР была СП-ПКС в зоне 3×3 мм (AUC=0,82; порог отсечения 37,5%; чувствительность 76,67%, специфичность 83,3%). Для минимизации рисков клинической манифестации ретинопатии у данной категории пациентов, помимо стабилизации гематологических показателей, представляется перспективным применение РПТ Ретиналамином, доказавшим в многолетних исследованиях при заболеваниях, связанных с патологией сетчатки и зрительного нерва, свою высокую эффективность и безопасность.
СВЕДЕНИЯ ОБ АВТОРАХ:
Янченко Сергей Владимирович — д.м.н., профессор кафедры офтальмологии БухГосМИ; 200126, Республика Узбекистан, г. Бухара, ул. Гиджуванская, д. 10; ORCID iD 0000-0002-7371-689X
Саидова Нигора Фарходовна — аспирант кафедры офтальмологии БухГосМИ; 200126, Республика Узбекистан, г. Бухара, ул. Гиджуванская, д. 10; ORCID iD 0009-0001-7312-3541
Малышев Алексей Владиславович — д.м.н., заведующий офтальмологическим отделением ГБУЗ «НИИ — ККБ № 1»; 350000, Россия, г. Краснодар, ул. 1 Мая, д. 167; заведующий кафедрой офтальмологии ФГБОУ ВО
«МГТУ»; 385000, Россия, г. Майкоп, ул. Первомайская, д. 191; ORCID iD 0000-0002-1448-9690
Хаирова Елена Николаевна — д.м.н., доцент, профессор кафедры терапии с курсом фармакологии и фармации Медицинского института непрерывного образования ФГОУ ВО «РОСБИОТЕХ»; 125080, Россия, 125080, г. Москва, Волоколамское ш., д. 11; ORCID iD 0000-0003-2954-8996
Тешаев Шухрат Жумаевич — д.м.н., профессор, ректор БухГосМИ; 200126, Республика Узбекистан, г. Бухара, ул. Гиджуванская, д. 10; ORCID iD 0009-0002-1996-4275
Одилова Гулжамол Рустамовна — д.м.н., доцент, заведующая кафедрой офтальмологии БухГосМИ; 200126, Республика Узбекистан, г. Бухара, ул. Гиджуванская, д. 10; ORCID iD 000-0001-8825-8134
Давлатов Салим Сулейманович — д.м.н., доцент, заведующий отделом контроля качества БухГосМИ; 200126, Республика Узбекистан, г. Бухара, ул. Гиджуванская, д. 10; ORCID iD 0000-0002-3268-7156
Контактная информация: Янченко Сергей Владимирович, e-mail: eye2105sv@gmail.com
Конфликт интересов отсутствует.
Статья поступила 01.12.2025.
Поступила после рецензирования 22.12.2025.
Принята в печать 26.01.2026.
ABOUT THE AUTHORS:
Sergey V. Yanchenko — Dr. Sc. (Med.), Professor of the Department of Ophthalmology, Bukhara State Medical Institute; 10, Gidzhuvanskaya st., Bukhara, 200126, Republic of Uzbekistan; ORCID iD 0000-0002-7371-689X
Nigora F. Saidova — Postgraduate Student, Department of Ophthalmology, Bukhara State Medical Institute; 10, Gidzhuvanskaya st., Bukhara, 200126, Republic of Uzbekistan; ORCID iD 0009-0001-7312-3541
Alexey V. Malyshev — Dr. Sc. (Med.), Head of the Department of Ophthalmology, Scientific Research Institute — Regional Clinical Hospital No. 1; 167, 1 Maya st., Krasnodar, 350000, Russian Federation; Head of the Department of Ophthalmology, Maykop State University of Technology, 191, Pervomaiskaya str., Maykop, Republic of Adygea, 385000, Russian Federation; ORCID iD 0000-0002-1448-9690
Elena N. Khairova — Dr. Sc. (Med.), Associate Professor, Professor of the Department of Therapy with a Course of Pharmacology and Pharmacy, at the ROSBIOTECH Medical Institute of Continuous Education; 11, Volokolamskoe road, Moscow, 125080, Russian Federation; ORCID iD 0000-0003-2954-8996
Shukhrat Zh. Teshaev — Dr. Sc. (Med.), Professor, Rector of Bukhara State Medical Institute; 10, Gidzhuvanskaya st., Bukhara, 200126, Republic of Uzbekistan; ORCID iD 0009-0002-1996-4275
Gulzhamol R. Odilova — Dr. Sc. (Med.), Assistant Professor, Head of the Department of Ophthalmology, Bukhara State Medical Institute; 10, Gidzhuvanskaya st., Bukhara, 200126, Republic of Uzbekistan; ORCID iD 000-0001-8825-8134
Salim S. Davlatov — Dr. Sc. (Med.), Assistant Professor, Head of the Quality Control Department, Bukhara State Medical Institute; 10, Gidzhuvanskaya st., Bukhara, 200126, Republic of Uzbekistan; ORCID iD 0000-0002-3268-7156
Contact information: Sergey V. Yanchenko, e-mail: eye2105sv@gmail.com
There is no conflict of interest.
Received 01.12.2025.
Revised 22.12.2025.
Accepted 26.01.2026.