Введение
Несмотря на стремительное развитие фармацевтической промышленности и наличие множества противогрибковых препаратов, лечение кандидозного вульвовагинита (КВВ) остается актуальной проблемой. Из-за высокой заболеваемости, длительного клинического течения [1], частых рецидивов [2, 3] и растущей резистентности к азолам [4] существует неудовлетворенная потребность в новых вариантах лечения пациенток с КВВ. В настоящее время основной концепцией лечения КВВ является восстановление нормальной вагинальной микробиоты. Физиологические механизмы нормотипичной колонизации вагинальной микробиоты играют решающую роль в подавлении морфологического размножения дрожжей Candida до гифальной формы, что в конечном итоге определяет степень патогенности грибка [5–8]. Сочетание противогрибковых препаратов с известным механизмом действия с препаратами, способствующими восстановлению нормальной вагинальной микробиоты, представляет собой продуктивную стратегию повышения эффективности лечения [5]. Эффективность различных лекарственных форм пробиотиков изучалась на протяжении десятилетий, однако результаты остаются противоречивыми [9–12]. Таким образом, наша цель — провести исследование комбинированного препарата, содержащего лактулозу в качестве пребиотика и противогрибковое средство. Хотя данные об использовании лактулозы при лечении КВВ ограниченны, важно отметить, что многочисленные исследования, изучающие ее влияние на кишечную микробиоту (и, в частности, на рост бифидобактерий), свидетельствуют о ее потенциальной пользе [13].
Исследуемый препарат Экофуцин® ДУО1 (натамицин 100 мг + лактулоза 300 мг, суппозитории вагинальные) представляет собой комбинацию противогрибкового средства натамицина и пребиотика лактулозы. Натамицин — это полиеновый антибиотик широкого спектра действия. Его фунгицидная активность обусловлена связыванием со стеролами клеточной мембраны грибов, что увеличивает проницаемость клеточной мембраны, приводя к потере важных клеточных компонентов и в конечном итоге к лизису клеток. Натамицин активен в отношении большинства дрожжеподобных грибов, дерматофитов, дрожжей и других грибов, а также некоторых простейших, таких как трихомонады, однако неэффективен против грамположительных и грамотрицательных бактерий. Поскольку натамицин оказывает местное действие и плохо всасывается (менее 3% проникает через кожу и неповрежденные слизистые оболочки), его местное применение практически не связано с системными нарушениями или побочными эффектами [14].
Лактулоза — это синтетический дисахарид, состоящий из остатков галактозы и фруктозы, связанных на β-гликозидном уровне [15]. Она не переваривается ферментами млекопитающих, однако может ферментироваться нормальной микрофлорой [16], способствуя росту бифидобактерий и лактобацилл. В результате ферментации лактулозы образуются короткоцепочечные жирные кислоты (молочная, уксусная и муравьиная), которые подавляют рост грибов Candida и других патогенов [17]. Исследования на животных показали, что лактулоза при пероральном приеме абсорбируется слабо и метаболизируется кишечной микробиотой [18]. Таким образом, системной абсорбции лактулозы при интравагинальном введении не ожидается.
Поскольку натамицин не подавляет рост и размножение лактобацилл, мы предполагаем, что сочетание антимикотической и пребиотической терапии при КВВ будет иметь синергический эффект. Эта комбинация будет стимулировать формирование нормальной микрофлоры влагалища, одновременно подавляя рост Candida.
Таким образом, клиническое исследование было направлено на то, чтобы проверить, обладает ли препарат Экофуцин® ДУО (натамицин 100 мг + лактулоза 300 мг, суппозитории вагинальные) превосходящей эффективностью в сравнении с Пимафуцином (натамицин 100 мг, суппозитории вагинальные) или лактулозой (300 мг, суппозитории вагинальные). Второй целью исследования было изучение безопасности комбинированных суппозиториев при лечении КВВ у небеременных взрослых женщин. Исследование было разработано на основе рекомендаций Управления США по санитарному надзору за качеством пищевых продуктов и лекарственных средств (FDA) по разработке препаратов для лечения КВВ [19]. Для настоящей работы был предложен адаптивный план исследования, поскольку влияние лактулозы на развитие грибковой инфекции в настоящее время неизвестно.
Материал и методы
Исследование «Natamycine+Lactulose-supp-12/21» (разрешение на проведение клинического исследования № 482 от 11.08.2022) проводилось с декабря 2022 г. по июль 2023 г. в двух странах: Российской Федерации (1 исследовательский центр) и Республике Беларусь (5 исследовательских центров). Перед включением пациенток в исследование было получено одобрение от комитета по этике Минздрава России (выписка из протокола № 305 от 22.03.2022) и местных этических комитетов (Заключение б/н от 05.12.2022, выданное комитетом по этике Минской городской поликлиники № 4; Заключение б/н от 28.11.2022, выданное комитетом по этике Минской городской амбулатории № 5; Заключение б/н от 05.12.2022, выданное комитетом по этике Минской городской клинической больницы скорой медицинской помощи; Заключение б/н от 02.12.2022, выданное комитетом по этике Минской центральной поликлиники № 2 Фрунзенского района; Заключение б/н от 29.11.2022, выданное комитетом по этике Минской городской больницы № 1). Исследование координировалось кафедрой репродуктивной медицины и хирургии Московского государственного медико-стоматологического университета им. А.И. Евдокимова и проводилось в соответствии с Декларацией Всемирной медицинской ассоциации по этике медицинских исследований с участием человека (Хельсинкская декларация) и руководящими принципами Международной конференции по гармонизации (надлежащая клиническая практика). Исследование NCT06411314 ретроспективно зарегистрировано 13.05.2024.
Перед включением в исследование участницы получили письменные и устные объяснения целей, задач и методов исследования, а также потенциальных преимуществ и рисков, связанных с участием. Участники и исследователь заполнили форму информированного согласия в двух экземплярах с датами и подписями от руки. Исследователь хранил первый экземпляр подписанной формы информированного согласия в досье исследователя, а второй экземпляр находился у участницы. Исследование проводили в соответствии с рекомендациями CONSORT. Исследование достигло заранее установленного уровня значимости для основного показателя эффективности (p<0,01556) и было прекращено на этапе промежуточного анализа.
Пациентки
В исследование были включены женщины в возрасте от 18 до 60 лет с клинически и микроскопически установленным диагнозом КВВ (МКБ-10 B37.3), подтвержденным всеми тремя критериями: 1) два или более из следующих признаков и симптомов КВВ: белые или желтовато-белые творожистые, густые или кремообразные выделения из влагалища; зуд, жжение и боль в области вульвы; зуд и жжение в аногенитальной области; дискомфорт в области вульвы; зуд, жжение, болезненное мочеиспускание (дизурия); 2) наличие дрожжевых клеток в мазке из влагалища; 3) pH влагалища ≤4,5. Диагностические критерии были стандартизированы во всех центрах и соответствовали рекомендациям FDA по разработке препаратов для лечения КВВ [1], а также Приложению 100. Беременных и кормящих женщин не включали в исследование. Все пациентки согласились использовать эффективные методы контрацепции на протяжении всего исследования и в течение 3 нед. после его завершения. Допустимыми методами контрацепции были комбинированные оральные контрацептивы в низких или микродозах, барьерные или двойные барьерные методы.
Пациенток не включали в исследование при наличии любого из следующих критериев: клинический и лабораторный диагноз бактериального вагиноза; вульвовагинит, вызванный специфическими патогенами (Trichomonas vaginalis, Chlamydia trachomatis, Neisseria gonorrhoeae); хронические воспалительные, атрофические или онкологические заболевания женских половых органов; предшествующие операции на наружных или внутренних половых органах в течение последних 6 мес.; роды и аборт в течение последних 6 мес.
У пациенток должен был быть стабильный менструальный цикл продолжительностью не более 35 дней. Для участия в исследовании участницы должны были воздерживаться от приема любых пребиотиков или пробиотиков, а также системных или местных противогрибковых, антибактериальных или противопротозойных препаратов в течение как минимум 2 нед. до скрининга и на протяжении всего исследования. Участницам исследования не разрешалось использовать внутриматочные спирали (гормональные или негормональные), местные вагинальные противогрибковые или антибактериальные препараты, а также вагинальные антисептики в течение 7 дней до скринингового визита. Женщин с тяжелым или хроническим заболеванием в период обострения также исключали из скрининга. Выборка для исследования формировалась из пациенток, посещавших специализированные отделения медицинских учреждений, и, следовательно, была репрезентативна для общей популяции.
Дизайн исследования
Исследование представляло собой международное рандомизированное контролируемое клиническое исследование (маскированное для эксперта, проводящего оценку данных) фазы III. Статистической целью исследования являлась демонстрация того факта, что оригинальная фиксированная комбинация натамицин + лактулоза (100 мг + 300 мг, суппозитории вагинальные) в составе препарата Экофуцин® ДУО (АО «АВВА РУС», Россия) при применении превосходит Пимафуцин® (натамицин 100 мг, суппозитории вагинальные, производитель — «Теммлер Италиа С.р.Л.», Италия) и лактулозу (300 мг, суппозитории вагинальные). Для достижения цели исследования было проведено четыре очных визита в исследовательский центр: Визит 0 (скрининг, дни -7–1), Визит 1 (рандомизация, день 1), Визит 2 (оценка эффективности лечения, день 7±1) и Визит 3 (оценка эффективности лечения, дни 20–27±1). Продолжительность исследования составила 34±2 дня.
Рандомизация и лечение
Регистрацию участниц исследования в исследовательских центрах проводили с помощью ПО OpenClinica 3.14 (OpenClinica, LLC), централизованной веб-системы. Участниц исследования случайным образом распределяли по группам лечения с использованием метода блочной рандомизации с различными размерами блоков через интерактивную веб-систему ответов. Присвоенный пациентке код рандомизации документировали в первичных документах, электронных формах историй болезни, отчетах о нежелательных явлениях (НЯ) и т. д. Присвоенный код рандомизации оставался неизменным на протяжении всего исследования. Для достижения цели исследования после рандомизации были сформированы 3 группы (1:0,5:1): группа 1 — Экофуцин® ДУО (100 мг + 300 мг, суппозитории вагинальные) (АО «АВВА РУС», Россия); группа 2 — лактулоза (300 мг, суппозитории вагинальные); группа 3 — Пимафуцин® (натамицин 100 мг, суппозитории вагинальные, производитель — «Теммлер Италиа С.р.Л.», Италия). Исследуемый препарат и препараты сравнения применяли в идентичном режиме, т. е. по одному суппозиторию вводили интравагинально 1 р/сут перед сном в течение 6 дней подряд. Суппозиторий вводили как можно глубже во влагалище в положении пациентки лежа на спине.
Исследуемый препарат Экофуцин® ДУО и препарат сравнения Пимафуцин® имеют существенные различия во внешнем виде, что делало невозможным полную маскировку исследователя и пациентки. В связи с этим использовали открытый план исследования. Чтобы учесть потенциальное влияние открытого плана на оценку эффективности, пациенток осматривал врач, не знавший о распределении пациенток по группам лечения.
Процедуры исследования
На скрининговом визите женщины, желавшие принять участие в исследовании, встречались с врачом и получали полную письменную и устную информацию обо всех процедурах и рисках исследования. После подписания и проставления даты на форме информированного согласия врач проводил скрининговый визит для оценки соответствия участницы критериям включения/невключения. Скрининговый визит включал в себя комплексное физическое обследование (в том числе гинекологический осмотр), оценку демографических характеристик, размеров тела, а также истории болезни и приема лекарств. Для подтверждения диагноза бактериального вагиноза проводили аминовый тест. На скрининговом визите образцы материала из влагалища исследовали на наличие урогенитальных инфекций (T. vaginalis, C. trachomatis, N. gonorrhoeae) методом полимеразной цепной реакции. Образцы крови собирали для анализа на ВИЧ, гепатит В (HBsAg), гепатит С (антитела к HCV), сифилис и гематологические показатели. Также проводили экспресс-тесты на наличие β-субъединицы хорионического гонадотропина человека в моче для исключения беременности, а также общий анализ мочи.
На Визите 1 пациенток повторно обследовали на предмет соответствия критериям включения и исключения, рандомизировали и назначали соответствующий группе рандомизации препарат. Каждая пациентка прошла обучение по применению суппозиториев и получила рекомендации по коррекции образа жизни, чтобы избежать использования любых вагинальных устройств для введения, таких как спермициды, тампоны, спреи, диафрагмы или презервативы. Кроме того, пациентке было рекомендовано воздержаться от половых контактов за 48 ч до следующего визита.
На последующих Визитах 2 и 3 регистрировали жалобы пациенток и проводили полное физическое обследование. Врач, не знавший о распределении пациенток по группам, проводил гинекологический осмотр и брал образец вагинального мазка. Во время Визита 2 пациентки предоставляли пустые упаковки от суппозиториев для оценки соответствия критериям. Во время Визита 3 отбирали образцы крови и мочи для проведения анализов.
Безопасность оценивали на протяжении всего исследования путем опроса пациенток, физического обследования, лабораторных анализов и инструментальных методов.
Гинекологическое обследование
Проводилось стандартное гинекологическое обследование. Во время гинекологического осмотра во всех исследовательских центрах врач-исследователь (не маскированный, Визит 0) и врач-оценщик (маскированный, Визиты 2 и 3) оценивали тяжесть симптомов КВВ по 4-балльной шкале (дополнительный файл 1).
Микроскопическое исследование (мазок из влагалища с 10% гидроксидом калия и без него)
В ходе Визитов 0, 2 и 3 с помощью ложки Фолькмана из заднебоковой части свода влагалища брали биологический образец для микроскопического исследования (нативный вагинальный образец с 10% раствором гидроксида калия (КОН) и без него). Нативные образцы микроскопически оценивали на наличие и форму эпителиальных клеток, наличие и количество полиморфноядерных лейкоцитов (ПЯЛ), ключевых клеток, лактобацилл и другой микрофлоры, псевдомицелия дрожжеподобных грибов и трихомонад, идентифицированных по их характерной подвижности. Результаты микроскопического исследования нативного образца представляли в соответствии с Руководством по сбору биологических образцов и лабораторным исследованиям в месте проведения исследования, версия 1.0 от 14.12.2022 (дополнительный файл 2).
Во время Визитов 0, 2 и 3 с помощью ложки Фолькмана из заднебоковой части свода влагалища брали биологический образец для микроскопического исследования (нативный вагинальный образец с 10% раствором KOH). На предметное стекло наносили 1–2 капли теплого (предпочтительно 37 °C) 10% раствора KOH и биологический образец. Биологический образец смешивали с одной-двумя каплями теплого 10% раствора KOH, накрывали покровным стеклом и немедленно исследовали под световым микроскопом (медицинский микроскоп «МИКМЕД-5»; АО «ЛОМО», Россия) с различным увеличением (×5, ×10 и ×40). Для нативного образца с 10% раствором KOH результаты микроскопического исследования представляли в соответствии с Руководством по сбору биологических образцов и лабораторным исследованиям в месте проведения исследования, версия 1.0 от 14.12.2022, при этом отмечали наличие псевдомицеллия или дрожжевых клеток.
Культуральный анализ (культура мазка из влагалища) на предмет наличия Candida spp. и Lactobacillus spp.
Во время Визитов 0, 2 и 3 проводили культуральный анализ для определения эндогенной вагинальной микрофлоры. Анализ предоставлял информацию о наличии или отсутствии роста, количестве лактобацилл, условно-патогенных микроорганизмов и грибов, выращенных в составе культуры, а также о роде и виде всех представителей, включая грибы. Кроме того, прилагалось описательное изображение микроскопического исследования мазка (бактериоскопии).
Оценка pH влагалища
Уровень pH влагалища измеряли во время Визитов 0, 2 и 3 полуколичественным методом с использованием индикаторных полосок Colpo-Test pH (ООО «Биосенсор АН», Россия). pH образца определяли полуколичественно путем визуального сравнения цвета и интенсивности цвета тест-полоски с эталонной цветовой шкалой.
Оценка пациенткой эффективности по 4-балльной шкале
В рамках оценки эффективности каждая пациентка заполняла анкету в присутствии лечащего врача. Анкета содержала закрытые варианты ответов от 0 балла (отсутствие клинических симптомов) до 3 баллов (тяжелые клинические симптомы) (см. дополнительный файл 1).
Основные показатели состояния организма
Во время всех визитов у пациенток измеряли частоту сердечных сокращений, частоту дыхания, систолическое и диастолическое артериальное давление, а также температуру тела. Артериальное давление измеряли на плечевой артерии в положении сидя в соответствии со стандартными рекомендациями.
Эффективность и безопасность
В качестве основного показателя эффективности в данном исследовании была определена доля (%) пациенток, достигших клинического ответа (выздоровления) к Визиту 2. Клиническим ответом считали отсутствие значимых признаков и симптомов КВВ (белые или желтовато-белые творожистые, густые или кремообразные выделения из влагалища; зуд, жжение и боль в области влагалища; зуд и жжение в аногенитальной области; дискомфорт в области влагалища; зуд, жжение, болезненное мочеиспускание [дизурия]). Вторичными показателями эффективности были: доля (%) пациенток с клиническим ответом к Визиту 2; доля (%) пациенток с микробиологическим выздоровлением (отсутствие Candida spp. во время Визитов 2 и 3); доля пациенток с общим (клиническим и микроскопическим) выздоровлением на Визитах 2 и 3; оценка эффективности лечения пациенткой по 4-балльной шкале во время Визитов 2, 3; микроскопическое изменение количества лактобацилл в вагинальных образцах на Визитах 2 и 3 в сравнении с исходным уровнем (Визит 0).
Оценивали следующие показатели безопасности: частота возникновения любых НЯ, частота возникновения серьезных НЯ (СНЯ), частота возникновения НЯ и СНЯ, вероятно связанных (по мнению исследователя) с исследуемым препаратом в исследуемой дозе, а также частота возникновения НЯ и СНЯ, приведших к прекращению приема исследуемого препарата.
Динамика клинических симптомов, лабораторных показателей и результатов pH-теста представлена в дополнительных файлах 3–9, доступных в онлайн-версии статьи.
Статистический анализ
Первичные параметры эффективности. В ходе исследования анализировали гипотезу превосходства исследуемого препарата над каждым из препаратов сравнения. В рамках анализа сформулированы следующие статистические гипотезы:
H0: pA — pB ≤ 0,05
HA: pA — pB > 0,05
где pA — доля пациенток с клиническим ответом (выздоровлением) к Визиту 2 в группе натамицин + лактулоза; pB — доля пациенток с клиническим ответом (выздоровлением) к Визиту 2 в группе лактулозы или группе Пимафуцина.
На всех этапах исследования с целью адекватного контроля общей ошибки I рода выполняли иерархическое тестирование. Сначала проводили сравнение между Экофуцином ДУО и лактулозой. Если было очевидно статистически значимое превосходство, то проводили сравнение между Экофуцином ДУО и Пимафуцином. Для подтверждения гипотезы исследования необходимо, чтобы препарат показал свое превосходство над обоими препаратами сравнения.
С учетом характера гипотезы превосходства был использован односторонний вариант точного критерия Фишера с уровнем значимости, определяемым этапом анализа (промежуточным или финальным) и группами сравнения (см. ниже). С учетом выбранного метода анализа для оценки статистических гипотез были рассчитаны доли (выраженные в процентах), разница долей между группами и доверительные интервалы (ДИ) для долей и для разницы долей между группами. Для расчета ДИ для долей был использован биномиальный метод Клоппера — Пирсона, для расчета ДИ для разницы долей был использован метод Ньюкомба — Вилсона. Для демонстрации превосходства исследуемого препарата над препаратом сравнения мы предположили, что ДИ для межгрупповой разницы в долях (pA — pB) пациенток, достигших клинического ответа (выздоровления) к Визиту 2, не пересечет нижний предел 0,05 (5%). Значение p, полученное для одностороннего точного теста Фишера для демонстрации эффективности, составило <0,01556 для промежуточного анализа и <0,013812 для окончательного анализа при сохранении основных предположений. Значения p для сравнений Экофуцина ДУО с лактулозой и с Пимафуцином были идентичны.
Исследование имело адаптивный дизайн, позволяющий пересчитать размер выборки на основе результатов промежуточного анализа. Размер выборки рассчитывали с использованием адаптивного подхода, основанного на групповом последовательном дизайне. Предполагалось, что промежуточный анализ будет проведен после достижения 50% набора пациенток. Для промежуточного анализа было определено, что для группы 1 и группы 3 потребуется набрать по 88 пациенток (включая выбывших во время исследования). Если промежуточный анализ подтвердит основные предположения, в каждую группу (1 и 3) будет набрано еще по 88 пациенток. Группа 2 (лактулоза) должна включать 34 пациентки до промежуточного анализа и еще 34 пациентки после промежуточного анализа.
Основной анализ проводили по популяции по протоколу (ПП).
Вторичные параметры эффективности. Вторичные параметры эффективности анализировали с использованием точного теста Фишера или критерия χ2 (в зависимости от ожидаемого значения в таблицах сопряженности). Для расчета 95% ДИ для пропорций использовали биномиальный метод Клоппера — Пирсона.
Для анализа микроскопических изменений количества лактобациллярных выделений в вагинальных образцах на Визитах 2 и 3 по сравнению с исходным уровнем использовали критерий Манна — Уитни для сравнения между группами и парный критерий Вилкоксона для сравнения внутри групп.
Основной анализ вторичных параметров эффективности проводили в популяции ПП.
Статистический анализ выполняли с использованием ПО Statistica версии 10.0. Анализ демографических и других исходных характеристик был запланирован для всего аналитического набора данных и набора данных для анализа безопасности. Базовые характеристики оценивали только в наборе данных для анализа безопасности, поскольку наборы не различались. Описательную статистику использовали для представления всех групповых данных, включая демографические данные, результаты лабораторных исследований, результаты инструментального и физикального обследования, а также жизненно важные показатели для каждой группы лечения. Сопутствующие заболевания и нежелательные явления кодировали с использованием MedDRA. Сопутствующие препараты кодировали по классификации ATX.
Результаты исследования
Пациентки
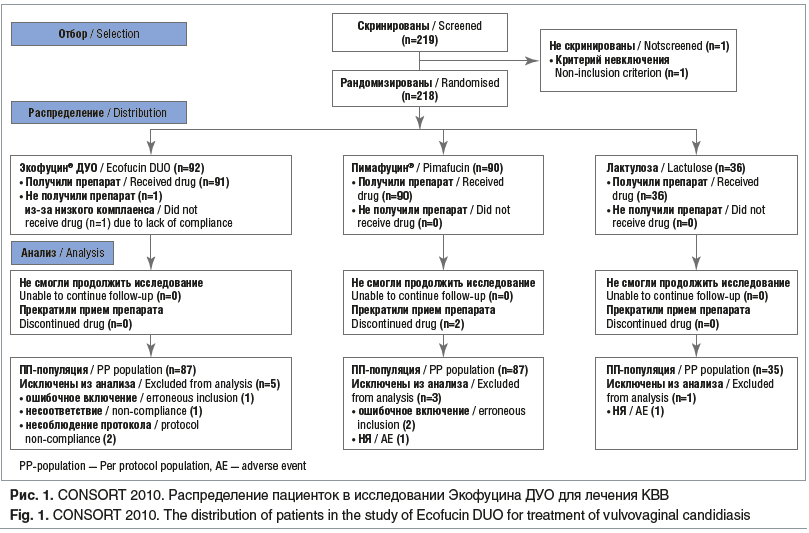
В исследовании приняли участие 219 пациенток, из которых 218 были рандомизированы: 4,13% (9/218) рандомизированных пациенток досрочно выбыли из исследования, т. е. 5,43% (5/92) пациенток выбыли из группы Экофуцина ДУО и 3,33% (3/90) пациенток выбыли из группы Пимафуцина (различия между группами статистически незначимы, р=0,721). Из группы лактулозы было исключено 2,78% (1/36) женщин, что статистически незначимо (p=1,000) по сравнению с группой Экофуцина ДУО (рис. 1). Таким образом, в популяцию ПП вошли 209 пациенток: 87 пациенток в основной группе, 87 пациенток в группе Пимафуцина и 35 пациенток в группе лактулозы. В набор данных для анализа безопасности вошли 217 пациенток, так как одна женщина не получила ни одной дозы исследуемого препарата.
Причины исключения из исследования: ошибочное включение: пациентки, не соответствующие критериям включения; несоблюдение протокола: пациентки, не завершившие лечение; несоблюдение протокола: пациентки, допустившие серьезные нарушения протокола; отзыв информированного согласия: пациентки, не пожелавшие продолжать участие в исследовании; НЯ: возникновение нежелательного события, повлекшего за собой отказ пациентки от участия в исследовании.
Демографические характеристики пациенток в исследуемой и контрольных группах были сопоставимы, включая возраст и индекс массы тела (ИМТ). Различия в массе тела между группами, получавшими комбинацию натамицин + лактулоза и исключительно лактулозу, не были статистически значимыми, поскольку ИМТ между группами не различался (табл. 1). Поскольку в исследовании участвовали только женщины, сравнение и описание групп по полу неприменимо.

Первичные параметры эффективности
В ходе исследования были получены следующие результаты. К Визиту 2 клиническое выздоровление в популяции ПП отмечалось у 81,6% (71/87) женщин в группе Экофуцина ДУО по сравнению с 42,9% (15/35) в группе лактулозы. Разница между долями составила 38,8% (далее — «исследуемый препарат» минус «препарат сравнения») с 95% ДИ 19,9–55,1%. Статистический анализ показал, что Экофуцин® ДУО превосходит лактулозу. Это подтверждается тем фактом, что нижняя граница 95% ДИ не пересекала значение 0,05 (5%), а значение p одностороннего точного критерия Фишера оказалось меньше 0,001 (табл. 2).
Исследуемый препарат сравнивали со вторым препаратом сравнения на основании данных о превосходстве Экофуцина ДУО над лактулозой. В группе Пимафуцина в популяции ПП клиническое выздоровление к Визиту 2 наблюдалось у 62,3% (55/87) пациенток. Разница между долями составила 18,4% (95% ДИ 5,11–30,9%). Статистический анализ показал, что Экофуцин® ДУО превосходит Пимафуцин®. Это подтверждается тем фактом, что нижняя граница 95% ДИ не пересекает значение 0,05 (5%), а значение p одностороннего точного критерия Фишера составляет 0,005 (табл. 3).



Вторичные параметры эффективности
Во время Визита 3 клиническое выздоровление в популяции ПП отмечалось у 90,8% (79/87) женщин в группе Экофуцина ДУО по сравнению с 62,9% (22/35) в группе лактулозы. Различия между группами были статистически значимыми (p<0,001) в пользу Экофуцина ДУО (рис. 2). В популяции ПП сравнительный анализ между группами Экофуцина ДУО и Пимафуцина выявил статистически значимую разницу в доле выздоровевших пациенток к Визиту 3 в пользу исследуемого препарата (р=0,021). Таким образом, клиническое выздоровление отмечалось у 90,8% (79/87) женщин в основной группе и у 78,2% (68/87) женщин в группе сравнения (см. рис. 2).

В группе Экофуцина ДУО микробиологическое выздоровление (Визит 2) наблюдалось у 75,9% (69/87) пациенток к Визиту 2 (рис. 3) и у 90,8% (79/87) пациенток к Визиту 3 (рис. 4). В группе лактулозы 45,7% (16/35) и 74,3% (26/35) пациенток ответили положительно во время Визитов 2 и 3 соответственно. Статистически значимые различия наблюдались между группами в обеих временных точках (Визит 2 — р=0,001, Визит 3 — р=0,017). В группе Пимафуцина у 71,3% (65/87) и 88,5% (77/87) пациенток отмечалось микробиологическое выздоровление во время Визитов 2 и 3 соответственно. Статистически значимых различий между группой Экофуцина ДУО и группой Пимафуцина по показателю микробиологического выздоровления обнаружено не было.


Во время Визита 2 общее (клиническое и микроскопическое) выздоровление в популяции ПП отмечалось у 71,1% (61/87) женщин в группе Экофуцина ДУО в сравнении с 22,9% (8/35) в группе лактулозы (рис. 5). Различия между группами были статистически значимыми в пользу исследуемого препарата (p<0,001).

Во время Визита 3 Экофуцин® ДУО также показал более высокую эффективность по сравнению с лактулозой (p<0,001) (рис. 6). На этот момент у 85,1% (74/87) субъектов, получавших комбинацию, наблюдалось клиническое и микробиологическое выздоровление в сравнении с 51,4% (18/35) пациенток, получавших монотерапию лактулозой. Во время Визита 2 не отмечалось статистически значимой разницы в клинической и микробиологической эффективности в популяции ПП между Экофуцином ДУО и Пимафуцином (p=0,083). Однако фиксированная комбинация превосходила монотерапию Пимафуцином к Визиту 3 (p=0,028).
Во время Визитов 2 и 3 участницы исследования оценивали эффективность по 4-балльной шкале. На Визите 2 в популяции ПП 2,30% (2/87), 54,0% (47/87) и 43,7% (38/87) пациенток, получавших Экофуцин® ДУО, и 10,3% (9/87), 44,8% (39/87) и 44,8% (39/87) пациенток, получавших Пимафуцин®, оценили терапию как удовлетворительную, хорошую и отличную соответственно (разница между группами отсутствует, р=0,700). На этих же визитах 17,1% (6/35), 48,6% (17/35) и 31,4% (11/35) женщин в группе лактулозы оценили лечение как удовлетворительное, хорошее и отличное соответственно (различия между группами не были статистически значимыми по сравнению с группой Экофуцина ДУО, р=0,058) (рис. 7).


На Визите 3 в популяции ПП 2,30% (2/87), 29,9% (26/87) и 66,7% (58/87) женщин в группе Экофуцина ДУО и 1,15% (1/87), 41,4% (36/87) и 57,5% (50/87) женщин в группе Пимафуцина оценивали терапию как удовлетворительную, хорошую и отличную соответственно (разница между группами отсутствует, р=0,357). Во время того же визита 2,86% (1/35), 51,4% (18/35) и 37,1% (13/35) женщин в группе лактулозы оценивали лечение как удовлетворительное, хорошее и отличное соответственно (разница между группами была статистически значимой по сравнению с группой Экофуцина ДУО, р=0,007) (рис. 8).

Во время Визита 3 количество вагинальных лактобацилл (по логарифмической шкале) было значительно выше в группе комбинации натамицин + лактулоза. Таким образом, во время Визита 0 в основной группе исследования количество лактобацилл (Me (Q1; Q3) составляло 4,00 (0,00; 5,00) lg КОЕ/мазок. Во время Визита 3 наблюдался статистически значимый рост до 5,00 (3,00; 6,00) lg КОЕ/мазок (внутригрупповая разница была статистически значимой, p<0,001). В группах сравнения наблюдалось менее выраженное улучшение с течением времени. К Визиту 3 были выявлены статистически значимые различия между группой комбинированной терапии и группой лактулозы (р=0,028), а также группой Пимафуцина (p<0,001).
Микроскопическое исследование проводили у пациенток с нормальным или низким уровнем вагинальных лактобацилл. Среди женщин с КВВ с низким исходным числом вагинальных лактобацилл Экофуцин® ДУО повышал вагинальные уровни лактобацилл до референтных значений у 15,4% пациенток (95% ДИ 2,03–28,7) к Визиту 2 (статистически значимое значение [95% ДИ не включает ноль]). К Визиту 3 Экофуцин® ДУО повышал вагинальные уровни лактобацилл до референтных значений у 20,9% (95% ДИ 5,91–35,85) пациенток с низкими исходными значениями этого показателя (статистически значимо [95% ДИ разницы не включает ноль]). Применение Пимафуцина и лактулозы не оказало влияния на количество пациенток с нормальным или низким уровнем лактобацилл на Визитах 2 и 3 по сравнению с Визитом 0. На Визите 3 доля женщин с нормальным уровнем лактобацилл в группе Экофуцина ДУО была статистически значимо выше, чем в группе Пимафуцина (р=0,007), с аналогичными исходными значениями во время Визита 0 (р=0,675) (табл. 4).


Безопасность
В ходе исследования НЯ были зарегистрированы у 6,59% (6/91) пациенток в группе Экофуцина ДУО и у 11,1% (10/90) пациенток в группе Пимафуцина, однако статистически значимых различий между группами не выявлено (р=0,284). В группе лактулозы НЯ зарегистрировано не было. Ни у одной пациентки из всех групп не возникало СНЯ.
Наиболее частым СНЯ считается легкая анемия (2 и 8 случаев в группе исследуемого препарата и 5 из 11 случаев в группе Пимафуцина). НЯ со стороны мочеполовой системы были зарегистрированы в 2 из 8 случаев в группе Экофуцина ДУО и в 5 из 11 случаев в группе Пимафуцина.
Два из восьми легких НЯ в группе Экофуцина ДУО были связаны с исследуемым препаратом, а именно: жидкий стул (n=1) и зуд в вульвовагинальной области (n=1). В группе Пимафуцина такое же количество легких НЯ было связано с лечением, а именно: раздражение в месте введения (n=1) и преждевременные менструации (n=1). Таким образом, в ходе исследования было выявлено в общей сложности 4 нежелательные реакции.
В отношении НЯ средней степени тяжести не было выявлено связи с лечением ни в одной из групп.
Определенная связь была установлена для одного случая в группе Пимафуцина. В группе Экофуцина ДУО связь с терапией не была установлена ни для одного случая (отсутствие межгрупповых различий, p=1,000). Вероятная связь была признана для одного случая в основной группе; такая связь не выявлялась в группе Пимафуцина (p=1,000). Одно НЯ в группе исследуемого препарата и одно НЯ в группе сравнения были, возможно, связаны с лечением (p=1,000). Сомнительная связь была выявлена для 6 НЯ в группе Экофуцина ДУО и 8 НЯ в группе препарата сравнения (отсутствие статистически значимых межгрупповых различий, p=1,000). Условной связи ни для одного из НЯ в двух группах установлено не было, в то время как одно НЯ было неопределенно связано с Пимафуцином (статистически значимых различий между группами не выявлено, р=1,000).
Таким образом, статистически значимых различий между НЯ, связанными с лечением, не выявлено: р=0,577 между группой Экофуцина ДУО и группой Пимафуцина.
Три из всех 19 случаев НЯ в обеих группах были средней тяжести, а 16 случаев НЯ были легкими; случаев тяжелых НЯ не зарегистрировано (табл. 5). В группе Экофуцина ДУО был зарегистрирован 1 случай средней тяжести по сравнению с двумя случаями в группе сравнения. Статистически значимых различий между группами не выявлено (p=0,737).
Обсуждение
Исследование продемонстрировало превосходящую эффективность оригинальной фиксированной комбинации натамицина и лактулозы (100 мг + 300 мг, суппозитории вагинальные, Экофуцин® ДУО, производитель — АО «АВВА РУС», Россия) в сравнении с лактулозой (300 мг, суппозитории вагинальные) у взрослых пациенток с КВВ. Превосходство было продемонстрировано во все моменты времени (на Визитах 2 и 3) как в отношении клинического, так и в отношении микробиологического выздоровления и, следовательно, в отношении общего (как клинического, так и микробиологического) выздоровления. Анализ анкет, заполненных пациентками на заключительном визите, показал, что удовлетворенность лечением была выше при применении Экофуцина ДУО, чем при монотерапии лактулозой. В группе лактулозы посев вагинальных культур не выявил изменений в количестве лактобацилл во время Визитов 2 и 3 в сравнении с исходным уровнем. К заключительному визиту наблюдалась статистически и клинически значимая разница в пользу Экофуцина ДУО. Об этом свидетельствовало увеличение числа колоний лактобацилл.
Превосходящая эффективность исследуемого препарата Экофуцин® ДУО по сравнению с Пимафуцином была получена для первичной клинической точки, т. е. клинического выздоровления на втором визите. Было обнаружено, что комбинированный препарат более эффективен, чем монотерапия натамицином, в достижении клинического выздоровления на последнем визите. Никаких различий между двумя методами лечения относительно микробиологического выздоровления обнаружено не было. Однако в основной группе было больше пациенток с общим выздоровлением на заключительном визите по сравнению с группой сравнения.
По субъективной оценке, эффективности лечения различий между группами Экофуцина ДУО и Пимафуцина не выявлено. В группе Пимафуцина не наблюдалось существенной разницы в количестве вагинальных лактобацилл между исходным и оценочным визитами. При заключительном визите доля женщин с нормальным уровнем лактобацилл в группе Экофуцина ДУО была статистически значимо выше, чем в группе Пимафуцина с аналогичными исходными значениями.
Оценка безопасности не показала существенных различий между исследуемым препаратом Экофуцин® ДУО и препаратами сравнения. Установлено, что профиль безопасности Экофуцина ДУО сопоставим с профилем безопасности Пимафуцина при лечении пациенток с КВВ.
С развитием науки о микробиоте (в том числе вагинальной) быстро растет интерес к пребиотикам. Исследование продемонстрировало положительное влияние Экофуцина ДУО на количество лактобактерий у пациенток с КВВ: во время заключительного визита наблюдалось увеличение числа лактобацилл в сравнении с исходными значениями. В результате у большего количества пациенток были достигнуты референтные уровни лактобацилл.
Предыдущие данные показали, что снижение концентрации лактобактерий не является характерной чертой КВВ [20, 21]. Во время Визита 1 у 35,9% (78/217) от общего числа пациенток в вагинальных выделениях отмечались референтные уровни этого сапрофита. Однако исследование с использованием секвенирования нового поколения показало, что связанные с КВВ изменения вагинальной микробиоты более сложные и разносторонние, чем считалось ранее [22]. На основании этой гипотезы можно предположить, что пациенткам требовалась коррекция вагинального биоценоза. Это связано с тем, что группа с более высоким количеством лактобацилл в вагинальных выделениях показала лучшие клинические и микроскопические результаты.
Более высокая эффективность комбинированной терапии, а также увеличение количества лактобацилл имеют большое значение. При КВВ во время лечения антимикотиками симптомы исчезают, однако нормальная флора влагалища не восстанавливается, что увеличивает риск повторного заражения. Лактулоза в составе препарата Экофуцин® ДУО в качестве пребиотика может восстанавливать нормальную флору влагалища, увеличивая количество собственных лактобацилл, сокращая время клинической ремиссии, и, возможно, предотвращает повторные эпизоды инфекции. Поскольку лактулоза способствует росту лактобацилл, что было показано в данном исследовании, а натамицин уничтожает Candida spp., данная фиксированная комбинация восстанавливает нормальный вагинальный микробиом.
Лактобациллы могут производить метаболиты, включая лактат, антимикробные средства и молочную кислоту, чтобы подавлять пролиферацию патогенов. Молочная кислота снижает pH влагалища (3,5–4,5), что обеспечивает защиту от вирусных, бактериальных и паразитарных инфекций. Лактобациллы также производят бактериоцины и перекись водорода, обладающие бактерицидной и антимикробной активностью, что препятствует колонизации патогенных организмов. Они также могут конкурентно препятствовать прикреплению патогенов к эпителию и удерживать патогены физически, предотвращая их колонизацию, а также регулировать иммунный или воспалительный ответ, снижая воспаление за счет снижения содержания цитокинов, таких как IL-1β. Наконец, лактобациллы могут улучшать барьерную функцию, производя лактат, который увеличивает вязкость слизи, способствуя улавливанию вирусов, и предотвращая повреждающее действие патогенов на ДНК эпителиальных клеток [23]. Таким образом, преимущества лактобацилл очевидны, и в данном исследовании превосходящая эффективность фиксированной дозы, вероятнее всего, объясняется влиянием лактулозы на восстановление нормальной флоры.
Ограничения исследования
В исследовании участвовали небеременные женщины репродуктивного возраста, поэтому результаты могут отличаться в других возрастных группах, как и результаты беременных женщин.
Используемый для микроскопического исследования посев вагинальной культуры Candida spp. и Lactobacillus spp. характеризуется определенными ограничениями по чувствительности.
В исследование не включали женщин с рецидивирующим КВВ. Кроме того, период наблюдения ограничен 1 мес., что не позволяет сделать выводы о долгосрочных эффектах исследуемой комбинации препаратов.
Заключение
В настоящем международном рандомизированном контролируемом клиническом исследовании (маскированном для эксперта, проводящего оценку данных) было продемонстрировано, что оригинальная фиксированная комбинация натамицин + лактулоза (100 мг + 300 мг, суппозитории вагинальные) в составе препарата Экофуцин® ДУО (АО «АВВА РУС», Россия) показала превосходящую эффективность по сравнению с препаратом Пимафуцин® (натамицин, 100 мг, суппозитории вагинальные, производитель — «Теммлер Италиа С.р.Л.», Италия), а также лактулозой (300 мг, суппозитории вагинальные) у взрослых женщин с КВВ, как и сравнимый профиль безопасности.
1На момент проведения исследования торговое название препарата еще не было зарегистрировано в России. Лекарственный препарат Экофуцин® ДУО (натамицин 100 мг + лактулоза 300 мг, суппозитории вагинальные) зарегистрирован на территории Российской Федерации 07.05.2025. Регистрационный номер ЛП-№(010070)-(РГ-RU).
Дополнительная информация / Supplementary Information
Онлайн-версия статьи содержит дополнительные материалы, доступные по адресу: / The online version contains supplementary material available at https://doi.org/10.32364/2618-8430-2026-9-1-2
Дополнительный файл 1: Таблица П1. Оценка тяжести симптомов КВВ по 4-балльной шкале / Additional file 1: Table 1. Assessment of the severity of the symptom of vulvovaginal candidiasis on a 4-point scale
Дополнительный файл 2. Таблица П2. Регистрация результатов оценки нативных мазков / Additional file 2: Table S2. Registration of native smear assessment results
Дополнительный файл 3: Таблица П3. Оценка тяжести симптомов КВВ (выделений) (популяция FAS) / Additional file 3: Table S3. Assessment of the severity of symptoms of VVC (discharge) (FAS population)
Дополнительный файл 4: Таблица П4. Оценка тяжести симптомов КВВ (зуд, жжение и боль) (популяция FAS) / Additional file 4: Table S4. Assessment of the severity of symptoms of VVC (itching, burning, and pain) (FAS population)
Дополнительный файл 5: Таблица П5. Оценка тяжести симптомов КВВ (зуд и жжение на коже) (популяция FAS) / Additional file 3: Table S5. Assessment of the severity of symptoms of VVC (itching and burning on the skin) (FAS population)
Дополнительный файл 6: Таблица П6. Оценка тяжести симптомов КВВ (дискомфорта) (популяция FAS) / Additional file 6: Table S6. Assessment of the severity of VVC symptoms (discomfort) (FAS population)
Дополнительный файл 7: Таблица П7. Оценка тяжести симптомов КВВ (дизурия) (популяция FAS) / Additional file 7: Table S7. Assessment of the severity of symptoms of VVС (dysuria) (FAS population)
Дополнительный файл 8: Таблица П8. Оценка тяжести симптомов КВВ (диспареунии) (популяция FAS) / Additional file 8: Table S8. Assessment of the severity of symptoms of VVC (dyspareunia) (FAS population)
Дополнительный файл 9: Таблица П9. Результаты измерения pH вагинальной жидкости (популяция безопасности) / Additional file 9: Table S9. Vaginal fluid pH results (safety population)
Впервые статья Volkova O.N., Amel’chenko E.V., Makeeva O.V., Tolmachev S.A., Lesovaya E.A., Zacharia L.C., Dikovskiy A.V. Efficacy and safety of vaginal suppositories containing combination of Natamycin and Lactulose in treatment of vulvovaginal candidiasis: international, randomized, controlled, superiority clinical trial (combination of Natamycin and Lactulose for treatment of vulvovaginal candidiasis) была опубликована в журнале BMC Womens Health. 2025;25:77. DOI: 10.1186/s12905-025-03616-3
Согласие всех авторов на публикацию на русском языке получено.
Сведения об авторах:
Волкова Оксана Николаевна — к.м.н., УЗ «Городская клиническая больница неотложной медицинской помощи»; 220024, Республика Беларусь, г. Минск, ул. Лейтенанта Кижеватова, д. 58, пом. 4
Амельченко Елена Владимировна — УЗ «Городская клиническая больница неотложной медицинской помощи»; 220024, Республика Беларусь, г. Минск, ул. Лейтенанта Кижеватова, д. 58, пом. 4.
Макеева Оксана Васильевна — руководитель медицинского отдела АО «АВВА РУС»; 121614, Россия, г. Москва, ул. Крылатские Холмы, д. 30, к. 9.
Сергей Алекандрович Толмачев — АО «АВВА РУС»; 121614, Россия, г. Москва, ул. Крылатские Холмы, д. 30, к. 9.
Лесовая Екатерина Александровна — АО «АВВА РУС»; 121614, Россия, г. Москва, ул. Крылатские Холмы, д. 30, к. 9.
Лефтерис С. Захария — AVVA Pharmaceuticals Ltd, Лимасол, Кипр.
Диковский Александр Владимирович — AVVA Pharmaceuticals Ltd, Limassol, Cyprus.
Контактная информация: Лефтерис С. Захария, e-mail: l.zacharia@avvapharma.com
Источник финансирования: исследование финансировалось средствами АО «АВВА РУС».
Конфликт интересов: Макеева О.В., Толмачев С.А., Лесовая Е.А., Захария Л.С., Диковский А.В. являются сотрудниками АО «АВВА РУС» и AVVA Pharmaceuticals Ltd.
Статья поступила 15.01.2026.
Поступила после рецензирования 22.01.2026.
Принята в печать 30.01.2026.