Введение
Инфекции нижних дыхательных путей, в частности пневмонии, представляют собой одну из актуальных проблем современной медицины. Наиболее высокой заболеваемостью, безусловно, отличаются внебольничные пневмонии (ВП) — пневмонии, развившиеся вне стационара или в первые 48 ч госпитализации в стационар [1]. Заболеваемость ВП существенно вариативна, составляет от 1,2 до 2,4 случая на 1000 человек в Европе и США, существенно возрастая среди лиц пожилого возраста [2, 3]. В Российской Федерации заболеваемость ВП составляет порядка 408 на 100 тыс. населения1. Традиционно случаи ВП ассоциировались с бактериальными агентами, однако в последнее время, особенно в педиатрической практике, все большую роль в развитии ВП принято отводить респираторным вирусным агентам [4, 5]. Несмотря на это, одним из распространенных бактериальных агентов, ответственных за развитие ВП, является Mycoplasma pneumoniae. Этот микроорганизм способен вызывать как спорадические случаи заболевания, так и вспышки в различных организованных коллективах [6, 7]. В ряде наблюдений в детской практике указанный инфекционный агент может быть ответственен за развитие порядка 60% ВП [8].
Октябрь — декабрь 2023 г. ознаменовался сообщениями о вспышках ВП, вызванной M. pneumoniaе, в Китае и разных странах Европы, преимущественно у детей [9]. В дальнейшем подъем заболеваемости микоплазменной инфекцией также отмечался в Российской Федерации и регистрируется вплоть до настоящего времени.
M. pneumoniae принадлежит к классу Mollicutes, порядок Mycoplasmatales, семейство Mycoplasmataceae, род Mycoplasma. Эти микроорганизмы являются самыми маленькими среди внеклеточных патогенных бактерий и отличаются следующими характеристиками: отсутствие ригидной клеточной стенки, что обусловливает полиморфизм клеток; малый размер генома, определяющий ограниченность биосинтетических возможностей и высокие требования к условиям культивирования; способность паразитировать на мембране эукариотической клетки и длительно персистировать в организме человека; нечувствительность к антибиотикам, действующим на уровне клеточной стенки [10, 11]. Указанные биологические особенности существенно затрудняют назначение ранней эффективной эмпирической антибактериальной терапии, так как остальные главные возбудители ВП в рамках стартовой терапии требуют назначение β-лактамных антибиотиков.
Следует отметить также тот факт, что в рамках этио-логической верификации диагноза ВП, вызванных M. pneumoniae, ведущими методами являются полимеразная цепная реакция (ПЦР) и ряд серологических методов исследования. Доступность указанных методов существенно ограничена в рамках рутинной клинической практики, поэтому поиск методов клинического прогнозирования инфекций, вызванных M. pneumoniae, является актуальным вопросом, решение которого существенно повысит эффективность оказания медицинской помощи данной категории пациентов. Кроме того, ранняя целенаправленная антибактериальная терапия с учетом глобальных перспектив поможет значимо оказать влияние на растущую антибактериальную резистентность.
Цель исследования: изучить клинико-эпидемиологичесские и лабораторные особенности пневмоний, вызванных M. pneumoniae, и разработать методы клинического прогнозирования.
Материал и методы
Проведено одноцентровое ретроспективное исследование, включавшее 3884 пациента с верифицированным диагнозом «внебольничная пневмония», проходивших лечение в 2022–2024 гг. Исследование проведено в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации «Этические принципы проведения научных медицинских исследований с участием человека», Федеральным законом от 21.11.2011 № 323 ФЗ «Об основах охраны здоровья граждан в Российской Федерации», а также с требованиями Федерального закона от 27.07.2006 № 152-ФЗ «О персональных данных» (ред. от 21.07.2014, с изм. и доп., вступил в силу с 01.09.2015).
Верификацию диагноза осуществляли согласно актуальным на указанный период клиническим рекомендациям «Пневмония (внебольничная)». Пациенты проходили лечение в ГБУЗ НСО «Детская городская клиническая больница № 3». Было сформировано две исследовательские группы: группа 1 (n=1779) — пациенты с типичными пневмониями и верифицированным бактериальным агентом (Streptococcus pneumoniае, Klebsiella pneumoniае и др.), проходившие лечение в 2022–2023 гг.; группа 2 (n=1325) — пациенты с атипичными пневмониями, вызванными M. pneumoniae, проходившие лечение в 2024 г. Изучали медицинские карты стационарного больного. Верификацию возбудителя пневмонии осуществляли при помощи методов современной этиологической диагностики (посев мокроты на микрофлору; ПЦР мокроты на ДНК M. pneumoniae; ИФА крови на антитела к M. pneumoniae), а также данных клинической и эпидемиологической картины.
Анализировали основные клинические и эпидемиологические данные с целью выявления вероятных факторов риска микоплазменной этиологии заболевания.
Статистическую обработку данных выполняли в лицензионной версии программы Statistica 12.0. Учитывая отсутствие нормальности распределения показателей (не пройденный критерий Шапиро — Уилка), количественные параметры представлены в виде медианы и 1-го и 3-го квартилей (Me [Q1; Q3]). Качественные показатели представлены как абсолютные и относительные (%) значения. Сравнение по количественным показателям выполняли с помощью U-критерия Манна — Уитни, по качественным — критерия Пирсона. С целью выявления факторов риска применяли методы логистической регрессии — рассчитывали показатель отношения шансов (ОШ), 95% доверительный интервал (95% ДИ). Результаты считали статистически значимыми при уровне значимости р<0,05.
Результаты и обсуждение
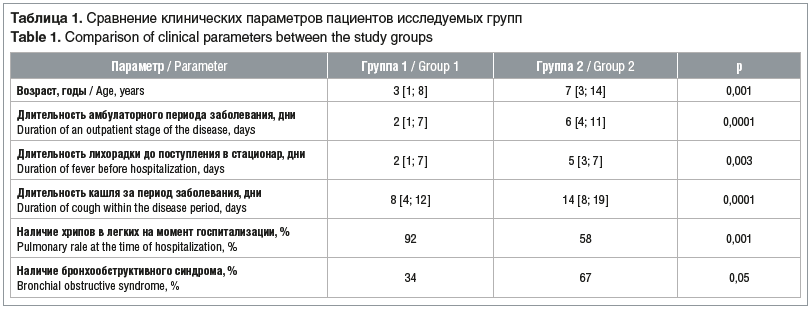
При проведении сравнительного анализа клинико-лабораторных параметров двух исследуемых групп были выявлены статистически значимые отличия. Данные по клиническим параметрам представлены в таблице 1.

В результате анализа полученных данных был определен ряд клинических параметров, более характерных для пациентов с ВП, ассоциированными с M. pneumoniaе. Больные характеризовались старшим возрастом, а также более длительным и клинически менее выраженным течением заболевания. Обращает на себя внимание достаточно длительный период амбулаторного лечения, а также более продолжительный период лихорадочной реакции до поступления в стационар (оценка выраженности лихорадочной реакции не являлась целью работы, однако в обеих группах температура тела была в диапазоне фебрильных значений). Указанный факт свидетельствует об относительно удовлетворительной переносимости температурных реакций и в целом о нетяжелом течении инфекций нижних дыхательных путей, вызванных M. pneumoniae. Существенным моментом является разница в аускультативной картине, проявляющаяся в значительно менее выраженной физикальной симптоматике, что в рутинной клинической практике может существенно затруднять диагностику атипичной пневмонии. Существенным признаком реализации атипичной пневмонии являлось наличие бронхообструктивного синдрома. Соответственно, при наличии признаков бронхиальной обструкции в сочетании с проявлениями интоксикационного синдрома рацио-нально проведение визуализации органов грудной клетки с учетом настороженности относительно развития атипичных инфекций нижних дыхательных путей.
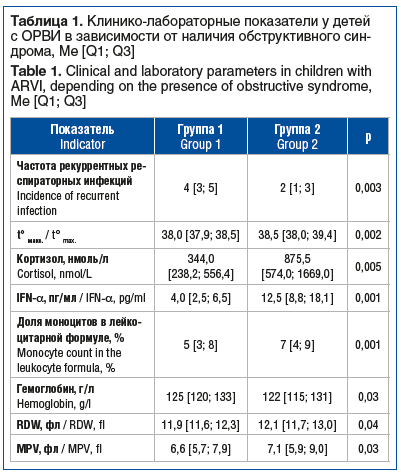
Как показал сравнительный анализ уровня лейкоцитов и С-реактивного белка (СРБ) в исследуемых группах (табл. 2), у пациентов с атипичными ВП отмечалась значительно менее выраженная провоспалительная активность. Указанная картина наблюдалась, несмотря на бактериальную природу патологии и наличие инфильтративных изменений, подтвержденных проведением рентгенографического исследования. Данное обстоятельство в сочетании с современным «антитрендом» на гипердиагностику пневмоний [12, 13] может существенно отсрочивать раннее назначение эффективной эмпирической антибактериальной терапии. В то же время это рационально использовать в рамках рутинной клинической практики и не стремиться к смене «антитренда» на гиподиагностику атипичной пневмонии.

Учитывая полученные выше результаты, а также клинические особенности течения атипичных ВП, ассоциированных с M. pneumoniae, складывается определенное понимание возможности лечения указанного патологического процесса преимущественно в амбулаторных условиях. В связи с тем, что верификация M. pneumoniае в настоящее время базируется исключительно на высокоспецифичных методах детекции, в частности методе ПЦР, создаются объективные сложности в доступности указанных методов. Данные особенности диктуют необходимость разработки методов верификации диагноза, базируясь на совокупности клинических и параклинических данных. В связи с этим по результатам проведенного исследования нами был предложен ряд потенциальных факторов риска развития ВП, ассоциированных с M. pneumoniae (табл. 3).

Полученные факторы риска рационально широко применять в рутинной клинической практике. Сочетание указанных факторов при сопоставлении с клинико-эпидемиологическими данными говорит о высокой вероятности инфекции нижних дыхательных путей, ассоциированной с M. pneumoniae. Также при реализации указанных параметров рационально включать в круг выбора эмпирической антибактериальной терапии препараты с внутриклеточным проникновением, в частности макролиды. Следует отметить, что выбор конкретного препарата из указанной группы должен осуществляться с учетом данных антибактериальной резистентности инфекционных агентов, в том числе и M. pneumoniae, на конкретной территории.
Тема прогнозирования рисков реализации инфекций нижних дыхательных путей, вызванных M. pneumoniae, является актуальной в современном ключе. Значительный вклад в изучение вопроса внесли коллеги из Китая, учитывая начало широкого распространения микоплазменной инфекции с территории данного государства в 2024 г. Так, в исследовании [14] было показано, что возможными факторами риска микоплазменной инфекции являлись: более старший возраст, более длительная лихорадка, более низкий уровень СРБ, а также более высокий уровень тромбоцитов. Кроме того, факторами риска тяжелой инфекции, ассоциированной с M. pneumoniae, явился ряд параклинических параметров, в частности более высокие уровни интерлейкина 5, интерферона γ и СОЭ. Ряд параметров имеет важные пересечения с нашим исследованием.
Важными ограничениями исследования являются его ретроспективный характер, а также проведение исследования на данных реального лечебно-диагностического процесса.
Заключение
В результате проведенного исследования был определен ряд клинико-лабораторных, а также эпидемиологических параметров, являющихся статистически значимыми факторами риска реализации пневмоний, вызванных M. pneumoniae. Требуется дальнейшее изучение эффективности предложенных критериев в выявлении микоплазменной пневмонии. Тем не менее полученные данные могут использоваться в условиях реальной клинической практики для повышения эффективности назначения эмпирической антибактериальной терапии.
Сведения об авторах:
Карпович Глеб Сергеевич — к.м.н., ассистент кафедры инфекционных болезней ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; врач-инфекционист ГБУЗ НСО «ДГКБ № 3»; 630040, Россия, г. Новосибирск, ул. Охотская, д. 81; ORCID iD 0000-0003-0982-6952
Куимова Ирина Валентиновна — д.м.н., профессор кафедры инфекционных болезней ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0000-0003-4727-1636
Рябиченко Татьяна Ивановна — д.м.н., ведущий научный сотрудник лаборатории иммунологии ФИЦ ФТМ; 630060, Россия, г. Новосибирск, ул. Тимакова, д. 2; ORCID iD 0000-002-0990-0078
Обухова Ольга Олеговна — д.м.н., главный научный сотрудник, руководитель лаборатории иммунологии ФИЦ ФТМ; 630060, Россия, г. Новосибирск, ул. Тимакова, д. 2; ORCID iD 0000-0002-9834-1799
Кашников Дмитрий Валерьевич — студент 6-го курса ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0009-0009-3584-6931
Урманаев Альберт Альбертович — студент 6-го ФГБОУ ВО НГМУ Минздрава России; 630091, Россия, г. Новосибирск, Красный пр-т, д. 52; ORCID iD 0009-0007-7213-1543
Контактная информация: Карпович Глеб Сергеевич, e-mail: karpovich.gleb@yandex.ru
Прозрачность финансовой деятельности: авторы не имеют финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 14.07.2025.
Поступила после рецензирования 08.08.2025.
Принята в печать 31.08.2025.
About the authors:
Gleb S. Karpovich — С. Sc. (Med.), assistant of the Department of Infectious Diseases, Novosibirsk State Medical University; 52, Krasnyi ave., Novosibirsk, 630091, Russian Federation; infectious disease physician of Children’s City Clinical Hospital No. 3; 81, Okhotskaya str., Novosibirsk, 630040, Russian Federation; ORCID iD 0000-0003-0982-6952
Irina V. Kuimova — Dr. Sc. (Med.), Professor of the Department of Infectious Diseases, Novosibirsk State Medical University; 52, Krasnyi ave., Novosibirsk, 630091, Russian Federation; ORCID iD 0000-0003-4727-1636
Tatiana I. Ryabichenko — Dr. Sc. (Med.), Leading Scientific Officer at the Laboratory of Immunology, Federal Research Center for Fundamental and Translational Medicine; 2, Timakov str., Novosibirsk, 630060, Russian Federation; ORCID iD 0000-002-0990-0078
Olga O. Obukhova — Dr. Sc. (Med.), Chief Scientific Officer, Head of the Laboratory of Immunology, Federal Research Center for Fundamental and Translational Medicine; 2, Timakov str., Novosibirsk, 630060, Russian Federation; ORCID iD 0000-0002-9834-1799
Dmitriy V. Kashnikov — 6th-year Student, Novosibirsk State Medical University; 52, Krasnyi ave., Novosibirsk, 630091, Russian Federation; ORCID iD 0009-0009-3584-6931
Albert A. Urmanaev — 6th-year Student, Novosibirsk State Medical University; 52, Krasnyi ave., Novosibirsk, 630091, Russian Federation; ORCID iD 0009-0007-7213-1543
Contact information: Gleb S. Karpovich, e-mail: karpovich.gleb@yandex.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 14.07.2025.
Revised 08.08.2025.
Accepted 31.08.2025.
1О состоянии санитарно-эпидемиологического благополучия населения в 2022 году: Государственный доклад. М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека; 2023.