Введение
Сахарный диабет 2 типа (СД2) и гипертоническая болезнь (ГБ) являются основными факторами риска (ФР) атеросклеротических сердечно-сосудистых заболеваний (АССЗ). Общие механизмы формирования ГБ и СД2 (ожирение, системное воспаление, окислительный стресс, инсулинорезистентность (ИР), эндотелиальная дисфункция, повышение активности ренин-ангиотензин-альдостероновой системы) объясняют эпидемиологические данные о высокой частоте сочетанного течения СД2 и ГБ [1, 2]. Нарушение регуляции метаболизма глюкозы, приводящее к митохондриальной дисфункции, системному воспалению и окислительному стрессу, обусловливает формирование структурно-функциональных изменений сердца и сосудов (фиброз, ремоделирование, дисфункция) в рамках диабетической кардиомиопатии и микроангиопатии. Изменения сердечно-сосудистой системы при СД2 и ГБ имеют во многом сходные черты: гипертензия приводит к повышению жесткости артерий и возрастанию постнагрузки, что, в свою очередь, вызывает ремоделирование сердца за счет гипертрофии желудочков, стимуляции фибробластов с развитием интерстициального фиброза. ГБ как важнейший самостоятельный ФР развития микрососудистых повреждений, ремоделирования и дисфункции сердечно-сосудистой системы усугубляет патофизиологические последствия гипергликемии, ИР, гиперинсулинемии, ускоряя развитие завершающей стадии сердечно-сосудистого континуума [3]. Сочетание СД2 и ГБ связано со снижением качества жизни пациентов, увеличением риска развития неблагоприятных сердечно-сосудистых событий, терминальных стадий микро- и макрососудистых осложнений, сердечной недостаточности (СН) и преждевременной смерти [4, 5]. Ранними доклиническими маркерами кардиальной дисфункции и ремоделирования являются диастолическая дисфункция левого желудочка (ДД ЛЖ), изменение геометрии сердца без клинических проявлений СН [6, 7]. Бессимптомная ДД ЛЖ и/или систолическая дисфункция левого/правого желудочка сердца, повышение давления наполнения являются вариантами функциональных признаков пред-СН. Концепция пред-СН, принятая мировым сообществом кардиологов, подчеркивает прогрессирующий характер СН и обосновывает необходимость раннего терапевтического вмешательства на доклинической стадии с целью отсрочки или предотвращения манифестации симптомной СН [8, 9].
Выявление факторов, повышающих вероятность развития ДД ЛЖ сердца у пациентов с СД2 и ГБ, с целью свое-временного лечебно-профилактического вмешательства является примером индивидуализации лечения, что соответствует концепции прецизионной медицины.
Цель исследования: изучить распространенность ФР формирования ранних структурно-функциональных изменений сердца с целью построения прогнозной модели ДД ЛЖ в группе пациентов с СД2 и ГБ без АССЗ.
Материал и методы
Исследование проводилось на базе кафедры внутренних болезней и семейной медицины дополнительного профессионального образования ФГБОУ ВО ОмГМУ Минздрава России, БУЗОО «ККД» с 2023 по 2026 г. Проведен ретроспективный анализ амбулаторных карт пациентов в соответствии с критериями включения/невключения.
Критерии включения: СД2, ГБ, возраст 18–65 лет, полноценность клинико-анамнестических данных, наличие результатов эхокардиографического исследования (ЭхоКГ). Критерии невключения: возраст менее 18 и более 66 лет, СД 1 типа, симптоматическая артериальная гипертензия (АГ), фракция выброса (ФВ) ЛЖ <50%, фибрилляция предсердий, АССЗ, неатеросклеротические ССЗ (кардиомиопатии, миокардиты) в анамнезе, гемодинамически значимые пороки сердца, анемии различного генеза.
С целью расчета объема выборки применялось уравнение [10]:
N = [(Zα/2)2 × p (1 — p) / d2] = [(1,96)2 × 0,35 (1 — 0,65) / (0,05)2],
где p — расчетное значение распространенности (35%) [11], d — допустимая погрешность выборки (5%), Zα/2 — критическое значение при 95% доверительном интервале (95% ДИ) определенности (1,96).
В анализ были включены медицинские данные 349 амбулаторных карт пациентов, отобранных в соответствии с критериями включения и невключения. На основании клинико-лабораторных данных дополнительно рассчитывали триглицеридно-глюкозный индекс (ТГИ) по формуле [12]: ТГИ = ln (триглицериды (ТГ) натощак (мг/дл) × глюкоза плазмы натощак (ГПН) (мг/дл)) / 2; для оценки долгосрочной вариабельности показателей (ГПН, HbA1c) рассчитывали стандартное отклонение (SD) по формуле: √∑nk = 1 (xi — x)2 / n — 1; скорректированное SD по формуле: SD / √n / n — 1; коэффициент вариации (CV) по формуле: SD / Х; скорректированный коэффициент вариации по формуле: CV / √n / n — 1, где n — общее количество измерений параметра, xi — последовательное измерение уровня параметра и X — средний уровень параметра [13].
Для решения задачи изучения ФР, повышающих вероятность ДД ЛЖ, пациенты были разделены на 2 группы.
Для построения мультивариантной предсказательной модели развития ДД ЛЖ была использована архитектура глубокого обучения TabNet с последующим SHAP-анализом для постфакторной оценки вклада каждого признака в предсказания модели.
Статистический анализ данных осуществляли с использованием пакета программ Excel (Microsoft, США). При распределении, отличном от нормального, данные записывали как медиана (Ме), нижний квартиль (Q1) и верхний квартиль (Q3). При сравнении двух независимых выборок по количественному признаку использовали критерий Манна — Уитни (U), критерий χ2 Пирсона. Качественные признаки описывали как доля (%). Для оценки взаимосвязи различных факторов и клинических исходов рассчитывали отношение шансов (ОШ), границы 95% ДИ. Во всех случаях критический уровень значения p принимали менее 0,05. ФР выявляли посредством обработки структурированных табличных клинических данных с применением нейросетевой архитектуры глубокого обучения TabNet, для интерпретации решений модели (определение и анализ маркеров, влияющих на вероятность выявления исхода) применяли SHAP-анализ.
Результаты и обсуждение
Медиана возраста в группе на момент сбора данных составила 62 (57; 65) года, мужчин было 27,51% (n=96). Индекс массы тела (ИМТ) в группе составил 32,87 (29,74; 37,81) кг/м2. Пациенты характеризовались наличием избыточной МТ в 26,93% (n=94) случаев, ожирением 1-й степени — в 32,38% (n=113), ожирением 2-й степени — в 23,78% (n=83), ожирением 3-й степени — в 16,91% (n=59) случаев. Длительность СД составила 8 (3; 12) лет, длительность ГБ — 10 (7; 18) лет. Возраст верификации диагноза СД2 составил 52 (43; 57) года, диагноза ГБ — 49 (42; 54) лет. По результатам ЭхоКГ ДД ЛЖ была выявлена у каждого второго пациента — в 56,73% (n=198). Установленный диагноз СН с сохраненной ФВ имели 19,77% (n=69).
Пациенты были разделены на 2 группы: группа 1 (наличие ДД ЛЖ, n=198) и группа 2 (отсутствие ДД ЛЖ, n=151). Группы были сопоставимы по полу (мужчины составляли 26,77 и 28,48% соответственно в группах 1 и 2, χ2=0,125; р=0,724) и возрасту (62 (58; 64) и 62 (55; 65) года соответственно в группах 1 и 2, р=0,536).
В группе 1 отмечался более длительный анамнез СД2 (8 (4; 14) и 6 (2; 10) лет соответственно в группах 1 и 2, р<0,05) и ГБ (11 (8; 19) и 8 (5; 14) лет соответственно в группах 1 и 2, р<0,05), более молодой возраст выявления ГБ (48 (41; 54) и 50 (44; 55) лет соответственно, р<0,05)), чаще отмечалась 3-я степень АГ в дебюте ГБ (87,88 и 26,49% соответственно в группах 1 и 2, р<0,001), чаще диагностировалась концентрическая гипертрофия ЛЖ (ГЛЖ) (25,76 и 7,28% соответственно в группах 1 и 2, р<0,001), любые микрососудистые осложнения СД2 (84,34 и 68,87% соответственно в группах 1 и 2, р<0,001), имелся анамнез курения (29,79 и 13,33% соответственно в группах 1 и 2, р<0,001) и был выше индекс коморбидности Чарлсон (5 (3; 6) и 4 (3; 4) соответственно в группах 1 и 2, р<0,001).
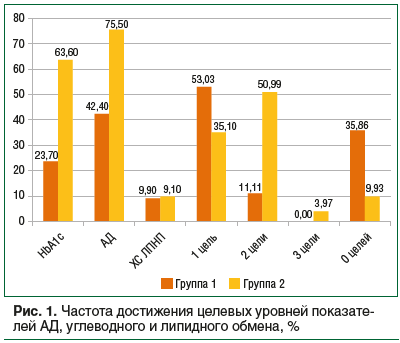
Достижение 3-компонентной цели терапии (целевые уровни АД, HbA1c, холестерина липопротеинов низкой плотности (ХС ЛПНП)) было отмечено только у 6 (3,97%) пациентов группы 2 (рис. 1).

В группе 1 реже применялась гипотензивная монотерапия (р<0,001), чаще — 3-компонентная терапия (38,88 и 23,18% соответственно в группах 1 и 2, p<0,01), при этом реже отмечено достижение нормотензии (42,93 и 75,49% соответственно в группах 1 и 2, p<0,001) с более высокими уровнями систолического (САД) и пульсового артериального давления (ПАД) (p<0,001). В группе 1 пациенты значимо реже получали монотерапию пероральными сахароснижающими препаратами (ПССП) (41,41 и 56,95% соответственно в группах 1 и 2, р=0,004), чаще — препараты инсулина (р<0,001), при этом не было отмечено различий между группами в частоте применения ПССП с органопротективными свойствами (10,61 и 9,27% соответственно в группах 1 и 2, р=0,681). Пациенты группы 1 имели более высокий уровень HbA1c (табл. 1) и реже достигали HbA1c <7,0% (23,33 и 64,24% соответственно в группах 1 и 2, p<0,001). Пациенты группы 1 имели более высокие уровни ТГ, ТГИ, ГПН и более высокие показатели долгосрочной вариабельности HbA1c (табл. 1).

Мы проанализировали влияние метаболических и гемодинамических факторов на риск развития ДД ЛЖ (рис. 2) [14]. Наибольшая вероятность ДД ЛЖ отмечена при уровне ГПН >8,31 ммоль/л (OШ 2,932; 95% ДИ 1,708–5,031; p=0,000) и HbA1c >7,6% (OШ 2,404; 95% ДИ 1,436–4,025; p=0,000). Показатели вариабельности HbA1c продемонстрировали прогностическую значимость в развитии ДД ЛЖ при уровне CV HbA1c >0,065 (OШ 1,786; 95% ДИ 1,076–2,964; р=0,012), SD HbA1c >0,49 (OШ 1,829; 95% ДИ 1,103–3,033; р=0,001), SDскор HbA1c >0,40 (OШ 1,865; 95% ДИ 1,119–3,108; р=0,008). Вероятность ДД ЛЖ значимо повышалась при уровне ТГИ >9,81 (OШ 3,955; 95% ДИ 2,229–7,006; р=0,000), САД >140 мм рт. ст. (OШ 2,383; 95% ДИ 1,392–4,080; р=0,000) и ПАД >54 мм рт. ст. (OШ 2,801; 95% ДИ 1,630–4,812; р=0,000).

При построении мультивариантной предсказательной модели развития ДД ЛЖ отобранные для прогнозирования ДД ЛЖ признаки включали: 3 признака, связанных с ГБ (исходная степень АГ, достижение цели по АД, уровень САД), 5 признаков, связанных с метаболическими параметрами (ТГИ, ГПН, HbA1c, показатели долгосрочной вариабельности гликемии), 3 признака — общие (индекс коморбидности Чарлсон, микрососудистые осложнения, достижение любых двух целей терапии) (рис. 3).

При анализе важности и направленности влияния признаков на прогноз исхода (ДД ЛЖ) с использованием SHAP-анализа (рис. 4) было выявлено, что наибольшее влияние оказывают 6 показателей: степень АГ, достижение цели АД, среднее значение САД, ГПН, SD HbA1c, HbA1c. Наибольший вес среди признаков имела степень АГ (уровень АД при верификации диагноза ГБ) (SHAP=0,128), демонстрируя положительный паттерн интерпретации, – более высокие значения АД ассоциированы с увеличением прогноза. Данная закономерность патогенетически обусловлена хронической гемодинамической перегрузкой с неизвестной длительностью на додиагностическом этапе [15]. Результаты нашего исследования согласуются с данными, представленными в других работах, посвященных этой теме [16, 17]. Отметим, что анализ графика демонстрирует, что в нашей когорте влияние АГ на прогноз, выстраиваемый моделью, варьирует: в некоторых наблюдениях «промежуточные» значения признака снижают вероятность исхода. Другие показатели, связанные с АД: достижение цели по АД (SHAP=0,042) и среднее значение САД (SHAP=0,034) продемонстрировали значимое влияние на прогноз. Отметим, что линейный отрицательный паттерн для признака «достижение целевого уровня АД» косвенно подтверждает то, что контроль АД, являясь модифицируемым фактором, и в группе коморбидных пациентов с ГБ и СД2 сохраняет значение целевого показателя терапии [18, 19].

Вторым по значимости фактором, продемонстрировавшим линейный положительный паттерн интерпретации, был уровень ГПН (SHAP=0,080). Положительная направленность влияния указывает, что повышение уровня ГПН ассоциируется с повышенной вероятностью ДД ЛЖ, в то время как более низкие значения соответствуют ее снижению. Полученные данные косвенно подчеркивают независимый вклад исходной гипергликемии в патогенез нарушения диастолической функции у пациентов с СД2. Наши данные согласуются с результатами исследования Т.Г. Утиной и соавт. [20], где среднее значение ГПН имело более высокую прогностическую значимость в развитии дисфункции миокарда, чем HbA1c.
В нашем исследовании впервые была оценена прогностическая роль SD HbA1c (SHAP=0,034), которая имела более выраженную значимость в развитии ДД ЛЖ и существенно превосходила по силе влияния на прогноз исхода скорректированный показатель SD HbA1c (SHAP=0,029), что согласуется с современными представлениями о важности стабильности гликемического контроля [21, 22]. Низкие значения снижают вероятность исхода, далее при увеличении SD HbA1c влияние на прогноз утрачивается, а затем по мере увеличения значения признака обнаруживается повышение вероятности и силы влияния на прогноз ДД ЛЖ (рис. 5). Можно сделать вывод, что в нашей когорте пациентов более существенное клиническое значение имел высокий показатель долгосрочной вариабельности гликемии в сравнении с его более низкими значениями.

С точки зрения влияния на структурно-функциональные показатели сердца ключевое значение приобретает не только своевременное достижение целевых значений HbA1c, которое имело менее весомый вклад (SHAP=0,023), но и длительное сохранение минимальной вариабельности гликемии, в том числе долгосрочной вариабельности HbA1c, которая может отражать феномен метаболической памяти, демонстрируя более тесную корреляцию со смертностью от всех причин у пациентов с СД2 по данным предыдущих исследований [23]. Достижение комбинированных целей терапии (АД и HbA1c) ассоциировано со снижением вероятности обнаружения ДД ЛЖ, что является важным наблюдением, подтверждающим значимость одновременного контроля СД2 и ГБ для профилактики развития структурно-функциональных изменений сердца. Наши данные согласуются с работой Е.В. Королевой [24], ориентированной на ранние структурно-функциональные изменения сердца в группе пациентов с СД2, где была показана высокая распространенность ДД ЛЖ, ассоциированная со стажем СД2, наличием ГБ, неудовлетворительным контролем СД2 и ГБ. Высокий индекс коморбидности Чарлсон указывает на то, что большее количество сопутствующей патологии увеличивает вероятность ДД ЛЖ и позволяет предположить, что оценка индекса коморбидности у пациентов с СД2 и ГБ может улучшить стратификацию риска развития ДД ЛЖ в данной когорте пациентов. Несмотря на относительно небольшой вклад по сравнению с другими факторами, показатель ТГИ (SHAP=0,008) оказывал значимое влияние на вероятность обнаружения исхода. Полученные данные согласуются с результатами S.H. Ustabaş et al. [25], которые также выявили связь ТГИ с показателями субклинической дисфункции миокарда у пациентов с впервые выявленным СД2.
Оценка качества модели классификации была выполнена на тестовой выборке (n=70), для получения оценки качества модели на всей выборке (n=349) была проведена стратифицированная 5-кратная кросс-валидация с использованием традиционных метрик качества модели. На тестовой выборке была получена высокая чувствительность — 0,950 (0,854±0,083 при кросс-валидации на всей выборке из 349 пациентов) и умеренная специфичность — 0,70. Высокая чувствительность позволяет использовать разработанную модель как скрининговую для дифференциальной диагностики группы риска ДД ЛЖ от группы с низким риском. Положительная прогностическая значимость модели составила 0,81, отрицательная прогностическая значимость — 0,91. Точность (эффективность) модели составляет 0,84. Площадь под ROC-кривой равна 0,8850, что характеризует предсказательную способность модели как «очень хорошую» (рис. 6).

С учетом дисбаланса классов была рассчитана площадь под Precision-Recall кривой (PR-AUC) — метрика, более информативная при дисбалансе классов, чем ROC-AUC. Полученное высокое значение (0,913) подтвердило способность модели выявлять положительный класс с высокой точностью и полнотой. При достижении высоких значений Recall (>0,90) модель сохраняет Precision на уровне >0,80, что является приемлемым для скрининговой задачи. Таким образом, полученные результаты свидетельствуют о потенциальной применимости разработанной модели в качестве скринингового инструмента для стратификации риска ДД ЛЖ у пациентов с СД2 и ГБ без АССЗ. Высокая чувствительность модели позволяет рассматривать ее как инструмент предварительного отбора пациентов для дальнейшего углубленного обследования.
Выявление ФР, повышающих вероятность развития ДД ЛЖ на доклинической стадии, является основной задачей для своевременной профилактики развития СН и улучшения долгосрочного прогноза. В нашем исследовании было выявлено, что пациенты с ДД ЛЖ отличаются достоверно более длительным анамнезом СД2 и ГБ, значимо более высоким ИМТ, достоверно более высокой распространенностью микрососудистых осложнений диабета, более высоким индексом коморбидности Чарлсон и большей распространенностью курения в сравнении с пациентами без ДД ЛЖ. У пациентов с ДД ЛЖ (группа 1) отмечалась статистически значимо более высокая степень АГ при верификации диагноза ГБ, более молодой возраст выявления ГБ, они значительно реже достигали целевого уровня АД, имея более высокие уровни САД и ПАД и чаще получая 3-компонентную гипотензивную терапию. В группе 1 значимо чаще диагностировалась концентрическая ГЛЖ. В группе с ДД ЛЖ чаще, чем в группе 2, назначалась инсулинотерапия, однако целевые значения HbA1c достигались реже. В группе 1 ни в одном случае не наблюдалось достижение цели 3-компонентной терапии (целевые уровни АД, HbA1c, ХС ЛПНП).
В нашей когорте пациентов шансы развития ДД ЛЖ были значимо выше при уровне ГПН >8,31 ммоль/л, HbA1c >7,6%, при более высоких значениях вариабельности HbA1c (CV HbA1c >0,065, SD HbA1c >0,49, SDскор HbA1c >0,40), показателях САД >140 мм рт. ст. и ПАД >54 мм рт. ст., значениях ТГИ >9,81. Модель глубокого обучения TabNet позволила выделить наиболее значимые ФР ДД ЛЖ у пациентов с СД2 и ГБ без АССЗ: степень АГ при верификации диагноза ГБ, индекс коморбидности Чарлсон, ГПН, HbA1c, SD HbA1c, среднее значение САД, ТГИ, достижение цели АД, достижение цели HbA1c, достижение двух любых целей (АД, HbA1c, ХС ЛПНП). При анализе важности и направленности влияния признаков на прогноз исхода (ДД ЛЖ) с использованием SHAP-анализа наибольшее влияние оказывают 6 показателей: степень АГ, достижение цели АД, среднее значение САД, ГПН, SD HbA1c, HbA1c.
Заключение
Таким образом, проведенное исследование демонстрирует, что формирование ДД ЛЖ у пациентов с СД2 и ГБ без АССЗ носит мультифакторный характер и ассоциировано с комплексом метаболических, гемодинамических и общеклинических показателей. В качестве наиболее значимых и потенциально модифицируемых мишеней для превентивной стратегии вмешательства следует выделить контроль долгосрочной вариабельности гликемии, достижение комбинированных целей терапии (по АД и HbA1c) и управление ПАД. Оценка долгосрочной вариабельности гликемии при рутинном мониторинге пациентов с СД2 и ГБ, наряду с традиционными показателями, может стать ключевым элементом для выделения группы высокого риска развития ДД ЛЖ и своевременной коррекции терапии, направленной на улучшение долгосрочного кардиоваскулярного прогноза. Полученные результаты свидетельствуют о потенциальной применимости разработанной модели в качестве скринингового инструмента для стратификации риска ДД ЛЖ у пациентов с СД2 и ГБ. Высокая чувствительность (0,95) и точность (0,84) модели позволяют рекомендовать ее применение в клинической практике врачей, курирующих пациентов указанной группы, как инструмент выделения группы риска развития ДД ЛЖ для дальнейшего углубленного обследования и планирования лечебно-профилактических мероприятий.