Введение
Ожирение прочно удерживает позиции одной из главных неинфекционных пандемий XXI в. По данным Всемирной организации здравоохранения, с 1990 г. распространенность ожирения среди взрослых выросла более чем вдвое, а среди подростков — в 4 раза[1]. В 2025 г. Международная федерация по борьбе с ожирением представила обновленные данные World Obesity Atlas, согласно которым к 2030 г. более 3 млрд человек будут иметь избыточную массу тела или ожирение, при этом около 2 млрд из них будут страдать клинически значимым ожирением, требующим медицинского вмешательства [1].
Хорошо известно, что ожирение является ключевым звеном в патогенезе сахарного диабета 2 типа (СД2), сердечно-сосудистых заболеваний (ССЗ), метаболически ассоциированной жировой болезни печени (МАЖБП), синдрома обструктивного апноэ сна (СОАС), остеоартрита и ряда онкологических заболеваний [2, 3]. Кроме того, сегодня ожирение перестало рассматриваться лишь как фактор риска ассоциированных с ним осложнений, а получило статус самостоятельного хронического заболевания, требующего пожизненного контроля и терапии [4].
Современная позиция в отношении ожирения была отражена в консенсусном заявлении Американской ассоциации клинических эндокринологов (AACE) «Алгоритм ведения взрослых пациентов с ожирением / хроническим заболеванием, обусловленным избыточным накоплением жировой ткани» [5]. Цель настоящего обзора — сопоставить предложенные AACE подходы к диагностике и лечению ожирения и действующие клинические рекомендации Российской ассоциации эндокринологов (РАЭ) 2024 г. [4], подчеркнуть имеющиеся отличия для практикующих специалистов.
Изменения в диагностических подходах
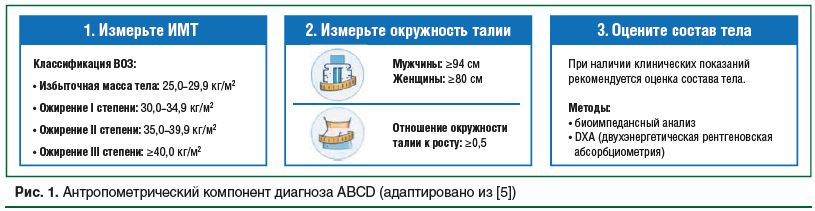
Международное руководство AACE 2025 г. вводит новый диагностический термин — Adiposity-Based Chronic Disease (ABCD) — хроническое заболевание, обусловленное избыточным накоплением жировой ткани. Этот термин призван, с одной стороны, уйти от стигматизирующей лексики, а с другой — подчеркнуть биологическую основу заболевания — нейрогормональную дисрегуляцию энергетического баланса [5]. Согласно предложенным рекомендациям диагноз ABCD включает два компонента: антропометрический и клинический. Антропометрический компонент позволяет подтвердить избыточное количество жировой ткани с помощью таких показателей, как индекс массы тела (ИМТ), окружность талии (ОТ) и отношение окружности талии к росту (ОТ/рост), а также визуализирующих методов с учетом этнических особенностей [5].
Сегодня в РФ междисциплинарные клинические рекомендации, утвержденные Минздравом России в 2024 г., регламентируют использование показателя ИМТ для постановки диагноза «ожирение» [4]. Как известно, в соответствии с критериями ВОЗ, избыточная масса тела устанавливается при значении показателя от 25 до 29,9 кг/м2, а ожирение — при ИМТ 30 кг/м2 и более [6].
Однако в последние годы парадигма использования ИМТ смещается в сторону расширения диагностических инструментов для оценки истинного количества жировой ткани в организме. Эксперты AACE подчеркивают, что ИМТ, будучи полезным скрининговым инструментом, не является синонимом количества жира в организме и может приводить к диагностическим ошибкам без учета индивидуальных особенностей пациента. Так, клиническая интерпретация повышенных значений ИМТ всегда требует подтверждения того, что это повышение действительно обусловлено избыточным количеством жировой ткани, а не другими факторами. В связи с этим рекомендации AACE предписывают обязательный комплексный анализ, включающий оценку ряда параметров: возраст, пол, мышечная масса, наличие сарко- и остеопении [7].
Для преодоления этих ограничений, согласно обновленным рекомендациям AACE, наряду с оценкой ИМТ выступают такие антропометрические параметры, как ОТ и отношение ОТ/рост. Так, пороговые значения ОТ для представителей европеоидной расы, населения Африки и Ближнего Востока составляют ≥94 см у мужчин и ≥80 см у женщин. В то же время для лиц азиатского происхождения используются более низкие пороговые значения ОТ, а именно ≥90 см у мужчин и ≥80 см у женщин [5, 8]. Таким образом, измерение ОТ сегодня является неотъемлемым методом диагностики ABCD. Превышение этих пороговых значений напрямую коррелирует с повышением риска ССЗ, инсулинорезистентности и других метаболических нарушений, что обусловлено патогенным влиянием висцеральной жировой ткани [9, 10].
В последние годы все большее значение приобретает и такой показатель, как отношение ОТ/рост, который рассматривается как более точный предиктор наличия факторов сердечно-сосудистого риска по сравнению с изолированным измерением ОТ и ИМТ [11]. Систематический обзор и метаанализ, опубликованный в Obesity Reviews в 2022 г., подтвердил высокую диагностическую точность пороговых значений соотношения ОТ/рост ≥0,5 для выявления факторов кардиометаболического риска [12]. Однако эксперты отмечают, что для некоторых специфических регионов могут требоваться корректировки. Например, оптимальные пороговые значения данного расчетного показателя для Восточной и Юго-Восточной Азии начинаются от ≥0,46. В то же время в тех случаях, когда антропометрические параметры и результаты обследования не соответствуют или вовсе противоречат клиническим данным, для оценки состава тела и/или распределения жировой ткани рекомендуется использовать дополнительные инструментальные методы, включая двухэнергетическую рентгеновскую абсорбциометрию (DXA), импедансную плетизмографию или магнитно-резонансную томографию. Несмотря на то, что определение единых пороговых значений процента жировой ткани требует дальнейших исследований, уже сегодня можно ориентироваться на показатели, ассоциированные с повышением кардиометаболического риска. Согласно имеющимся данным превышение количества жировой ткани более 25% у мужчин и более 32% у женщин может служить маркером избыточной жировой массы [13, 14]. Алгоритм представлен на рисунке 1.
![Рис. 1. Антропометрический компонент диагноза ABCD (адаптировано из [5]) Рис. 1. Антропометрический компонент диагноза ABCD (адаптировано из [5])](https://www.rmj.ru/upload/medialibrary/ace/pol8btxm8dxddx8ej15ru6akxaga8hg7/24-1.png)
Второй компонент при постановке диагноза «ожирение» носит клинический характер. Как известно, помимо степени выраженности ожирения, используется и классификация по стадиям. Так, РАЭ предложена стадийная классификация ожирения, где выделяют ожирение 0 стадии (ИМТ ≥30 кг/м2 без осложнений), стадии 1 (наличие одного или нескольких осложнений средней тяжести) и стадии 2 (наличие тяжелых осложнений) [4].
В свою очередь, экспертами AACE предлагается ввести термин ORCD (Obesity-Related Complications and Disease), то есть осложнения ожирения и ассоциированные с ним заболевания (табл. 1) [5].

Таким образом, согласно предложенной классификации, на основании наличия или отсутствия осложнений ожирения или ассоциированных с ним заболеваний рекомендовано стадировать данное заболевание на доклиническое (стадия 1) и клиническое (стадии 2 и 3) [5, 7]. Данная классификация представляется более обоснованной в связи с высокой коморбидностью больных ожирением.
Целевые показатели при терапии ожирения
На сегодняшний день клинические рекомендации РАЭ устанавливают целевые показатели снижения массы тела в зависимости от коморбидной патологии. К примеру, для улучшения течения дислипидемии и артериальной гипертензии (АГ) достаточно снижения массы тела на 5–15%, в то время как для достижения ремиссии СД2 или регресса MAЖБП требуется потеря >10% массы тела [4].
В консенсусном документе AACE 2025 г. также подчеркивается, что целью терапии является не только потеря массы тела, но и улучшение здоровья и качества жизни пациента, в связи с чем авторы руководства вводят понятие «лечение до целевого показателя осложнения» [5]. Так, процент снижения массы тела рассматривается как биомаркер, целевое значение которого подтверждается динамикой клинических исходов (значение АД, уровень HbA1c, показатели липидограммы, индекс апноэ-гипопноэ и т. д.) (табл. 2).

Таким образом, подобный персонифицированный подход позволяет рассматривать ожирение не как косметическую проблему, а как управляемое хроническое заболевание с четко определенными терапевтическими целями.
Немедикаментозное лечение
В действующих клинических рекомендациях РАЭ немедикаментозная терапия рассматривается как обязательный компонент лечения ожирения и включает гипокалорийную диету, увеличение уровня физической активности и поведенческую коррекцию. Подчеркивается необходимость формирования устойчивого энергетического дефицита, постепенного снижения массы тела и последующего удержания достигнутого результата. Кроме того, отмечается важность индивидуализации подхода с учетом возраста, сопутствующих заболеваний и функциональных возможностей пациента [4].
В свою очередь, рекомендации AACE 2025 г. расширяют концепцию немедикаментозного лечения, рассматривая его как непрерывный и структурированный процесс, направленный не только на снижение массы тела, но и на улучшение клинических исходов, связанных с осложнениями ожирения. Особое внимание уделяется систематической оценке психоэмоционального состояния, выявлению расстройств пищевого поведения, а также интеграции поведенческой терапии как ключевого элемента лечения. Таким образом, в отличие от рекомендаций РАЭ, где основной акцент делается на достижении и поддержании снижения массы тела, подход AACE в большей степени ориентирован на долгосрочное ведение ожирения как хронического заболевания с учетом биопсихосоциальных факторов и клинических исходов [5].
Так, модификация образа жизни является обязательным компонентом лечения пациентов с ABCD, независимо от стадии заболевания и необходимости фармакотерапии или хирургического лечения. Предложенный подход включает три ключевых направления: поведенческую терапию, диетотерапию и физическую активность [5].
Центральным элементом алгоритма является систематическая оценка психологического состояния пациента. Рекомендуется проводить скрининг на наличие тревоги, депрессии, а также расстройств пищевого поведения, поскольку эти факторы могут существенно влиять на эффективность лечения. При наличии соответствующих показаний пациент должен быть направлен на психологическое обследование или специализированную поведенческую терапию. Для повышения приверженности лечению рекомендуется использовать доказательные поведенческие стратегии.
Диетотерапия является ключевым компонентом модификации образа жизни при ABCD и должна основываться на индивидуализированном подходе с учетом клинических особенностей и культурных предпочтений пациента. Основной целью является создание устойчивого энергетического дефицита при сохранении высокого качества рациона. Индивидуализированные стратегии питания могут включать коррекцию соотношения макронутриентов, персонализированный расчет калорийности, использование заменителей пищи и другие подходы, способствующие снижению массы тела. Рекомендуется отдавать предпочтение минимально обработанным, богатым питательными веществами продуктам, включая овощи, фрукты, цельнозерновые продукты и источники качественного белка, а также ограничивать потребление высококалорийных продуктов и напитков. При этом особое внимание должно уделяться обеспечению достаточного поступления белка, пищевых волокон, витаминов и микроэлементов, особенно в условиях выраженного снижения массы тела, что способствует сохранению мышечной массы и предотвращению нутритивных дефицитов.
Важно отметить необходимость индивидуализации рекомендаций по физической активности с учетом функциональных возможностей, состояния здоровья и предпочтений пациента. При необходимости рекомендуется направление пациента к специалисту по лечебной физкультуре или фитнесу. Особое значение имеют силовые упражнения, поскольку они способствуют сохранению мышечной массы, особенно при значительном снижении массы тела.
Медикаментозное лечение ожирения
Наиболее значимые различия между рекомендациями РАЭ и ААСЕ представлены в разделах медикаментозного лечения, что обусловлено появлением современных высокоэффективных инкретинов и твинкретинов.
Рекомендации РАЭ включают четыре основных класса препаратов, зарегистрированных для лечения ожирения в РФ: ингибитор липаз (орлистат), препарат центрального действия с селективным ингибированием обратного захвата серотонина и норадреналина (сибутрамин и его комбинации) и два агониста рецепторов глюкагоноподобного пептида-1 (арГПП-1) — лираглутид (3,0 мг/сут) и семаглутид (2,4 мг/нед.) [4].
В свою очередь, руководство AACE 2025 г. делит препараты на два поколения [5]:
Первое поколение (одобрены до 2014 г.): орлистат, комбинации фентермин / топирамат ER, налтрексон / бупропион ER, лираглутид 3,0 мг. Средняя потеря массы тела при использовании данных препаратов составляет <10%.
Второе поколение: семаглутид 2,4 мг (средняя потеря массы тела ~17%) и тирзепатид — первый двойной агонист рецепторов ГПП-1 и глюкозозависимого инсулинотропного полипептида (арГИП) (средняя потеря массы тела до 22,5%) [5, 8].
Согласно предложенному ассоциацией алгоритму (рис. 2) на основе разделения осложнений, ассоциированных с ожирением, на кардиометаболические и биомеханические, предлагается выбор препаратов в зависимости от клинического состояния. Так, при кардиометаболических осложнениях, включая предиабет, СД2, МАЖБП, ХБП, сердечную недостаточность и АГ, препаратами первой линии являются тирзепатид и семаглутид, тогда как лираглутид, фентермин/топирамат и орлистат рассматриваются как альтернативные варианты терапии [15]. Также тирзепатид является препаратом первой линии и при СОАС, в то время как для профилактики сердечно-сосудистых событий и для лечения остеоартрита предпочтение в данном алгоритме отдается семаглутиду. Таким образом, выбор терапии определяется доказанной способностью препарата улучшать течение осложнений, ассоциированных с ожирением, что отражает современный персонализированный подход к лечению [5, 15–21].
![Рис. 2. Алгоритм выбора медикаментозной терапии, основанный на улучшении течения осложнений, ассоциированных с ожирением (адаптировано из [5]) Рис. 2. Алгоритм выбора медикаментозной терапии, основанный на улучшении течения осложнений, ассоциированных с ожирением (адаптировано из [5])](https://www.rmj.ru/upload/medialibrary/d55/oq7dpgbc50owjg7f5lekey2luvh0h3qs/24-4.png)
Следует отметить, что на сегодняшний день оригинальные препараты семаглутида и тирзепатида официально в РФ и ЕАЭС не зарегистрированы, что послужило стимулом для отечественных фармацевтических компаний к разработке собственных дженериков препарата. Благодаря компании «ГЕРОФАРМ» семаглутид под торговым названием Семавик/Семавик Некст®, а также тирзепатид под торговым наименованием Седжаро® доступны в клинической практике.
Риски использования нелицензированных аналогов инкретиномиметиков — «пептидов»
В настоящее время во всем мире особую тревогу вызывает растущая популярность нелицензированных (компаундированных) аналогов семаглутида и тирзепатида, распространяемых через интернет-магазины. Информация о данных молекулах в рекомендациях РАЭ отсутствует, в то время как согласно руководству AACE их применение категорически не рекомендуется [5]. В отличие от зарегистрированных препаратов, компаундированные версии не проходят верификацию безопасности, эффективности и качества.
Опубликованные данные свидетельствуют о неточных концентрациях, примесях, остатках растворителей, следах металлов и посторонних пептидах в данных препаратах. Все это диктует необходимость предупреждать пациентов, что производство таких аналогов с использованием пептидного синтеза несет риски иммуногенности и тяжелых передозировок, которые в клинической практике могут являться причиной госпитализаций.
Хирургическое лечение
Позиции AACE и РАЭ в отношении бариатрической хирургии в целом совпадают в признании данного метода наиболее эффективным вариантом лечения морбидного ожирения при неэффективности консервативного лечения. Согласно рекомендациям РАЭ хирургическое лечение показано пациентам с ИМТ ≥40 кг/м2 независимо от сопутствующих заболеваний или при ИМТ ≥35 кг/м2 при наличии тяжелых осложнений, таких как СД2 или СОАС [4].
В свою очередь, рекомендации AACE рассматривают бариатрическую хирургию как один из компонентов комплексного и персонализированного лечения ABCD, при этом выбор хирургического вмешательства определяется не только ИМТ, но и наличием осложнений, ассоциированных с ожирением, а также клиническими целями терапии. Дополнительно подчеркивается необходимость интеграции хирургического лечения в общую стратегию долгосрочного ведения пациента, направленную на улучшение клинических исходов и контроль осложнений, а не исключительно на снижение массы тела [5].
Таким образом, в отличие от рекомендаций РАЭ, основанных преимущественно на пороговых значениях ИМТ и наличии сопутствующих заболеваний, подход AACE в большей степени ориентирован на персонифицированную оценку клинической тяжести заболевания и роли хирургического вмешательства как элемента стратегии лечения, направленного на улучшение общего состояния здоровья пациента.
Заключение
Опубликованное в 2025 г. консенсусное заявление AACE представляет собой новый этап в понимании природы ожирения и подходах к его лечению. Ключевым изменением становится окончательный переход от модели, где диагноз основывался преимущественно на показателе ИМТ, к персонализированной оценке заболевания с учетом наличия и степени тяжести связанных с ожирением осложнений (ORCD) и использованию дополнительных диагностических параметров в виде ОТ и отношения ОТ/рост. Введение термина ABCD призвано не только дестигматизировать пациентов, подчеркнуть нейрогормональную природу заболевания, требующую пожизненного контроля, но и обоснованно выбирать класс лекарственных препаратов. Наконец, важным предупреждением для клинической практики становится обозначенная AACE проблема нелегальных компаундированных аналогов инкретиномиметиков.
Прозрачность финансовой деятельности: исследование выполнено при поддержке Министерства здравоохранения Российской Федерации (соглашение № 124021600064-8).
Конфликт интересов: Н.А. Сухоцкая является сотрудником «ГЕРОФАРМ». Остальные авторы заявляют об отсутствии конфликта интересов.
[1] World Health Organization. Obesity and overweight [Internet]. Geneva: WHO; 2024. (Electronic resource.) URL: https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight (дата обращения: 04.12.2025).