Введение
В настоящее время отмечается рост продолжительности жизни, в связи с чем увеличивается число лиц пожилого возраста, у которых часто встречаются сахарный диабет 2 типа (СД2), сердечно-сосудистые и другие сопутствующие заболевания, а также гериатрические синдромы (ГС)[1].
К ГС относят такие возраст-ассоциированные состояния, как саркопения, старческая астения (СА), когнитивные нарушения (КН), остеопороз, ортостатический синдром и др. Характерной чертой ГС является значительное повышение риска развития других ГС при возникновении одного из них [1].
Еще одной особенностью, осложняющей ведение пациентов пожилого возраста, является полипрагмазия — одновременное назначение 5 и более препаратов, что обусловлено как высокой коморбидностью, так и присоединением ГС[2]. По сведениям, представленным в базе данных клинико-эпидемиологического мониторинга сахарного диабета на территории Российской Федерации, доля пожилых пациентов среди пациентов с СД2 составляет 60,5%[3]. В этой группе распространенность полипрагмазии особенно высока и достигает 64% в связи с тем, что пациенты получают не только сахароснижающую терапию, но и терапию сопутствующих заболеваний [2]. При этом иногда пожилые пациенты используют нерекомендованные препараты, а также препараты, повышающие риск гипогликемии и падений. Такая ситуация требует соблюдения баланса между эффективностью и безопасностью терапии [3].
С учетом менее строгих целей гликемического контроля у пожилых пациентов [4] в настоящее время активно обсуждается проведение депрескрайбинга (деинтенсификации терапии) — преднамеренного процесса снижения дозы, отмены или замены препаратов с целью снижения рисков неблагоприятных явлений, в том числе гипогликемии [5]. Существуют данные о потенциальных преимуществах проведения депрескрайбинга в виде уменьшения риска гипогликемии, нежелательных реакций препаратов, улучшения качества жизни и приверженности пациентов лечению.
С целью проанализировать распространенность полипрагмазии и ее последствий у пожилых пациентов с СД2 и обсудить стратегии оптимизации фармакотерапии среди этой категории пациентов мы выполнили поиск научных публикаций в следующих электронных базах данных: PubMed, Cochrane Library, eLibrary, Scopus и Web of Science. Поисковые запросы включали комбинации следующих ключевых слов и фраз: на английском языке: deprescribing, polypharmacy, elderly patients, type 2 diabetes, geriatric syndromes, glycemic control; на русском языке: депрескрайбинг, полипрагмазия, пожилые пациенты, сахарный диабет 2 типа, гериатрические синдромы, гликемический контроль.
Полипрагмазия: терминология и эпидемиология
Термин «полифармация» широко используется во всем мире, в то время как в российской медицинской литературе более распространен термин «полипрагмазия», который происходит от греческих слов poly (много) и pragma (действие, дело), он определяется как одновременное назначение большого количества лекарственных средств, а также лечебно-диагностических процедур, в том числе необоснованно, но чаще используется в контексте приема лекарственных препаратов[4]. Термин «полифармация» касается одновременного применения только нескольких лекарственных препаратов [6]. Обычно эти термины используют в практике в качестве синонимов при назначении 5 и более лекарственных препаратов2, также иногда употребляется термин «гиперполифармация» при применении 10 и более препаратов [6].
В систематическом обзоре F. Remelli et al. [2], в котором полипрагмазия определялась как использование 4–6 препаратов, было показано, что ее распространенность среди пожилых пациентов составляет более 50%. В исследовании Е.А. Пановой и соавт. [7] также было продемонстрировано, что более чем в половине случаев в проанализированных амбулаторных картах пациентов старше 65 лет содержится информация о приеме более 4 препаратов, что подчеркивает широкую распространенность этой проблемы как в мире, так и в России.
Полипрагмазия может вести к возникновению и усугублению ГС, в том числе синдрома падений, КН, СА, а также увеличивать частоту эпизодов гипогликемии. Существующее разнообразие терминов и определений может усложнить обмен информацией между медицинскими работниками из разных стран, а также свидетельствует об отсутствии единого подхода к этой проблеме. Недостаток стандартизации создает сложности при сравнении результатов исследований и разработке согласованных клинических алгоритмов.
Гипогликемия: особенности в пожилом возрасте, связь с полипрагмазией
Эпизоды гипогликемии преимущественно развиваются при применении инсулинотерапии и препаратов сульфонилмочевины (ПСМ). По данным метаанализа (532 542 пациента с СД2), на фоне инсулинотерапии и ПСМ распространенность эпизодов легкой гипогликемии составила 50 и 30%, тяжелой — 21 и 5% соответственно [8].
Следует отметить, что распространенность использования ПСМ очень высока. По данным федерального регистра СД на 01.01.2023, монотерапия ПСМ составляет 22,4%, в комбинации с метформином (что является самой распространенной схемой терапии СД2) — 71,9%, а комбинация препаратов инсулина и пероральных сахароснижающих препаратов достигает 49% при длительности СД2 более 20 лет [9].
В исследовании ACCORD (Action to Control Cardiovascular Risk in Diabetes, 10 251 пациент с СД2, средний возраст 62,2 года) впервые было акцентировано внимание на влиянии гипогликемии на развитие фатальных сердечно-сосудистых событий. В группе интенсивного гликемического контроля (HbA1c <6,0%) по сравнению с традиционным контролем (HbA1c 7,0–7,9%) отмечалось увеличение смертности от сердечно-сосудистых заболеваний (ССЗ) на 22%, что было обусловлено, в первую очередь, эпизодами тяжелой гипогликемии [10]. В исследовании E. Chow et al. [11] у пациентов с СД2 на инсулинотерапии ночные нетяжелые гипогликемии были ассоциированы с увеличением частоты нарушений ритма сердца за счет удлинения интервала QT, что увеличивает риск ранней постдеполяризации, а также пируэтной желудочковой тахикардии (torsades de pointes).
Эпизоды гипогликемии, преимущественно тяжелой, оказывают негативное влияние не только на ССЗ, но и на когнитивные функции. В исследовании R.A. Whitmer et al. [12] (16 667 пациентов с СД2, средний возраст 65 лет) было выявлено, что 2 и более эпизодов тяжелых гипогликемий увеличивают риск развития деменции. По данным метаанализа [13] было отмечено увеличение риска ухудшения когнитивных функций после гипогликемии на 70% и увеличение риска гипогликемии у пожилых людей с деменцией на 60%, что, по мнению авторов, может формировать «порочный круг»: развитие тяжелых гипогликемий ведет к снижению когнитивных функций, а снижение когнитивных функций ведет к ухудшению контроля заболевания, и в результате — к более частым гипогликемиям.
В исследовании T.L. Middleton et al. [14] было отмечено, что у пациентов, получающих ПСМ, большинство гипогликемий были бессимптомными в ночное время. Отсутствие симптомов гипогликемии может быть обусловлено снижением адренергической симптоматики гипогликемии с возрастом. У пожилых людей гипогликемия характеризуется чаще нейрогликопеническими симптомами, которые пациенты воспринимают как проявления сопутствующих заболеваний [15].
В российском исследовании у госпитализированных пациентов с СД2 по данным непрерывного мониторирования гликемии были зарегистрированы эпизоды гипогликемии у 72% пациентов, а по результатам измерений глюкометром — всего у 22%, что свидетельствует о высокой частоте нераспознанных эпизодов гипогликемии у пожилых пациентов [16]. Уменьшение выраженности симптомов, частые эпизоды гипогликемии приводят к нарушению распознавания гипогликемии, формируя тем самым очередной «порочный круг». Значимый вклад в нарушение распознавания гипогликемии вносят автономная нейропатия, дисфункция контринсулярных гормональных реакций при повторных и длительных эпизодах гипогликемии, а также адаптация головного мозга к гипогликемии [17]. У пациентов с нарушением распознавания гипогликемии, в отличие от здоровых добровольцев или от пациентов без нарушения распознавания гипогликемии, изменяется характер распределения кровотока головного мозга и нарушается метаболизм глюкозы [18].
Сочетание таких факторов, как полипрагмазия, особенно включающая ПСМ и инсулинотерапию, а также нарушение распознавания гипогликемий, зачастую приводит к развитию гипогликемий у пациентов пожилого возраста с СД2, что в свою очередь повышает риск падений, КН, развития фатальных сердечно-сосудистых и других неблагоприятных событий.
Полипрагмазия и ГС
Полипрагмазия в значительной степени способствует развитию и усугублению ГС у пожилых пациентов с СД2. Исследования продемонстрировали четкую связь между полипрагмазией и повышенным риском падений среди пожилых людей. В исследовании L. Xue et al. [19] было показано, что у пожилых пациентов, принимавших ≥6 препаратов, частота падений была на 21% выше, чем у лиц без полипрагмазии. В исследовании C.M. Cheng et al. [20] по результатам краткой шкалы оценки психического состояния у пациентов старше 65 лет, принимавших ≥5 препаратов, умеренные КН и деменция встречались чаще в 1,75 и 2,33 раза соответственно. Результаты многоцентрового перекрестного наблюдательного исследования M.A. Carreiro Alonso et al. [21] демонстрируют, что среди пациентов с СД большая часть пациентов имели уровень HbA1c ≤6,5%, что коррелировало с более высокой частотой гипогликемий и тяжелыми КН в этой группе. Кроме того, пациенты на инсулинотерапии чаще имели тяжелые КН, чем на пероральной сахароснижающей терапии. В этом исследовании авторы подчеркивают необходимость переоценки интенсивности сахароснижающей терапии у пожилых пациентов.
Полипрагмазия повышает риск развития СА, характеризующейся снижением физиологических резервов организма и повышенной уязвимостью к стрессовым факторам. В исследовании N. Molist-Brunet et al. [22] в выборке пациентов со средним возрастом 85 лет в 93,3% случаев наблюдалась полипрагмазия (≥5 препаратов), а в 51% — гиперполипрагмазия (≥10 препаратов). Кроме того, у 66,2% этих пациентов было выявлено нерациональное использование препаратов, также было показано, что наиболее часто полипрагмазия встречалась у пациентов с СА.
В исследованиях по оценке результатов интенсивного гликемического контроля (ACCORD 2008 г., ADVANCE 2008 г.) впервые было акцентировано внимание на необходимости определения индивидуальных целевых уровней показателей углеводного обмена для пациентов с СД в зависимости от коморбидности и возраста [10, 23].
Согласно клиническим рекомендациям для пациентов с СД2 в зависимости от возраста, функционального статуса, в том числе наличия СА, КН, риска гипогликемии и ассоциированных ССЗ, определены индивидуальные целевые показатели гликемического контроля [4]. СД2 считается прогрессирующим заболеванием, требующим постоянной интенсификации терапии. При этом зачастую отмечается стремление достигнуть не только целевых показателей, но и значений ниже целевых, что является неверной тактикой, т. к. в группе пожилых пациентов более высокий риск фатальных сердечно-сосудистых событий, а также выше опасность развития гипогликемии. В связи с увеличением возраста, развитием СА и КН, наличием ассоциированных ССЗ необходимо проведение периодического пересмотра схемы лечения. Назначение препаратов, обладающих меньшим риском гипогликемии, может оказаться как более безопасным для пациента, так и более эффективным в плане соблюдения режима лечения, ухода и улучшения прогноза [24]. Одним из эффективных способов решения проблемы полипрагмазии и, как следствие, профилактикой развития ГС и эпизодов гипогликемии, является проведение депрескрайбинга.
Депрескрайбинг: существующие алгоритмы и перспективы развития
Депрескрайбинг — это преднамеренное и контролируемое снижение дозы, отмена или замена препаратов, которые могут вызвать побочные реакции или не оказывают дополнительных положительных эффектов [5].
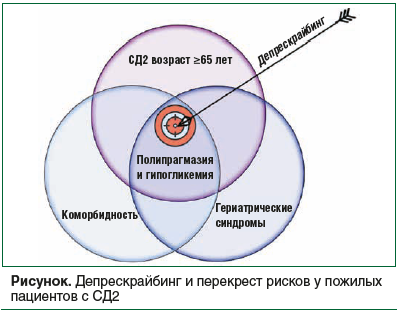
Проведение депрескрайбинга сахароснижающих препаратов у пожилых людей с СД2 преследует несколько целей: снижение риска нежелательных явлений, в том числе гипогликемии, других осложнений, связанных с приемом препаратов, уменьшение количества принимаемых препаратов для улучшения приверженности терапии и повышения качества жизни (см. рисунок).

Существуют различные рекомендации для оптимизации терапии у пожилых пациентов, направленные на помощь клиницистам в коррекции полипрагмазии.
Одним из первых инструментов оценки целесообразности терапии стал индекс рациональности применения лекарственного средства (Medication appropriateness index, MAI). MAI разработан в 1992 г., он состоит из 10 вопросов, касающихся наличия показаний, противопоказаний, побочных эффектов, возможности лекарственного взаимодействия для каждого препарата. Каждый вопрос оценивается по шкале от 1 (полное соответствие препарата) до 3 (полное несоответствие), чем выше общий балл, тем менее рациональным считается применение препарата [25]. MAI обеспечивает структурированную оценку, однако не имеет четких рекомендаций по группам препаратов, в связи с чем носит субъективный характер и требует клинической оценки опытным специалистом [26].
Сходную структуру имеет алгоритм Гарфинкеля (The Garfinkel algorithm или Good Palliative-Geriatric Practice (GP-GP) algorithm), согласно которому получаемая терапия оценивается в соответствии с четырьмя критериями: исключение препаратов, назначенных без показаний, замена на более безопасные препараты, уменьшение дозы и добавление необходимых показанных препаратов. Использование этого алгоритма в исследованиях D. Garfinkel (2009–2016 гг.) приводило к улучшению или замедляло ухудшение функционального, психического и когнитивного статуса, качества сна, аппетита у 82,8% пациентов в течение 3 мес. после депрескрайбинга, а у 68% пациентов результаты сохранялись более 2 лет [27]. Результаты исследования продемонстрировали положительный эффект проведенного депрескрайбинга по этому алгоритму, однако отсутствие четких инструкций по коррекции терапии может приводить к субъективности в принятии решения.
Критерии Бирса разработаны в 1991 г. М. Бирсом с коллегами (Калифорнийский университет) [33]. Эти критерии содержат список потенциально неподходящих лекарств для пожилых людей от 65 лет и старше [28] и регулярно обновляется. Все ПСМ относятся к категории «следует избегать», но если есть необходимость их назначения, то предпочтение следует отдавать короткодействующим (например, глипизид) препаратам. В 2023 г. в критерии были добавлены уточнения по поводу ингибиторов натрий-глюкозного котранспортера-2 (иНГЛТ-2): рекомендовано применять с осторожностью из-за возможности эугликемического кетоацидоза и урогенительных инфекций. Критерии Бирса являются официальным документом, доказательно обоснованным и регулярно обновляемым Американским гериатрическим обществом, они широко признаны и просты в использовании, однако не позволяют учитывать индивидуальные особенности пациента [29].
Критерии STOPP/START разработаны в 2008 г. группой гериатров из Ирландии и представляют собой перечень потенциально не рекомендованных препаратов (STOPP-критерии) и возможных «упущенных» назначений показанных лекарственных средств (START-критерии) для пациентов пожилого возраста [30]. Изначально инструмент включал в себя 65 STOPP- и 22 START-критериев, затем был обновлен и дополнен в 2015 и 2023 гг. (133 STOPP- и 57 START-критериев). В критериях STOPP не рекомендовано использовать ПСМ у пациентов с СД, особенно при повышенном риске падений, метформин — у пациентов с расчетной скоростью клубочковой фильтрации <30 мл/мин/1,73 м2, а также инсулинотерапию у пациентов с ограниченной ожидаемой продолжительностью жизни, если инсулинотерапия не обеспечивает значительного улучшения качества жизни [31]. Преимуществом критериев STOPP/START является наличие многочисленных критериев по различным препаратам, показаниям и противопоказаниям, однако их применение на практике может занять много времени, поскольку алгоритм требует навыка работы с ним и включает обширный перечень препаратов.
Критерии FORTA (Fit fOR The Aged) были разработаны в 2012 г. экспертами из Германии, Австрии и Швейцарии. Критерии FORTA — это инструмент, предназначенный для оптимизации фармакотерапии пожилых людей путем оценки всех принимаемых препаратов согласно классификации по четырем категориям: А (необходимые) — незаменимые лекарства с очевидными преимуществами для пожилых пациентов; В (полезные) — препараты с доказанной эффективностью, но с ограниченными доказательствами безопасности у пожилых людей, могут применяться с осторожностью; С (сомнительные) — лекарственные препараты с сомнительной эффективностью или безопасностью для пожилых людей, следует рассмотреть альтернативные варианты; D (не рекомендованные) — препараты, которых следует избегать из-за недостаточной эффективности или неблагоприятного соотношения риска и пользы у пожилых пациентов [32]. Исследование VALFORTA показало, что применение принципов FORTA привело к значимому снижению количества нежелательных реакций у пожилых пациентов, при этом отмечалось улучшение показателя повседневной базовой активности (индекс Бартел) в группе вмешательства по сравнению с группой контроля [33].
Критерии PRISCUS — это список потенциально неподходящих медикаментов (Potentially Inappropriate Medications, PIMs) для пожилых пациентов, используемый в Германии. Он был разработан в 2010 г. для идентификации лекарственных средств, которые могут увеличивать риск побочных эффектов у лиц старшего возраста. В обновленной версии 2023 г. применения глибенкламида рекомендуется избегать, а глимепирид и акарбозу — применять с осторожностью [34].
В России в 2019 г. начата разработка протокола проведения депрескрайбинга сахароснижающих препаратов для пациентов старше 65 лет, принимающих более 1 сахароснижающего препарата и имеющих риск гипогликемии [35].
Учитывая сложность и трудоемкость анализа практически всех существующих алгоритмов коррекции терапии, в настоящее время разрабатываются и исследуются системы поддержки принятия решений, встроенные в медицинские информационные системы. В исследовании К.М. Niehoff et al. [36] этот инструмент извлекал первичную информацию из электронных амбулаторных карт пациентов, с возможностью внесения дополнительной информации, полученной непосредственно при опросе пациента. В ходе комплексной оценки данных программа выдавала отчет с обратной связью для врача, основанный на оценке несовместимости и нецелесообразности применения препаратов, а также с учетом приверженности пациента.
Проблемы в реализации депрескрайбинга
По результатам систематического обзора S. Chua et al. [37] в большинстве проанализированных работ (в 25 из 33) отмечались положительные результаты в группе проведения депрескрайбинга у пожилых пациентов с СД2. В ряде других исследований также было продемонстрировано, что проведение депрескрайбинга позволило снизить риски гипогликемии без ухудшения гликемического контроля [38].
Несмотря на потенциальный положительный эффект депрескрайбинга у пожилых пациентов, существуют трудности в его проведении как со стороны врачей, так и со стороны пациентов. По данным систематического обзора, медицинскими барьерами проведения депрескрайбинга среди врачей являются отсутствие единых руководств, неопределенность относительно того, кто несет ответственность за отмену препарата, опасения по поводу ухудшения симптомов, отсутствие преемственности между стационаром и амбулаторным звеном, наблюдение пациента у разных специалистов. Со стороны пациентов трудности заключаются в восприятии депрескрайбинга как «отказа от лечения», сложности смещения фокуса с профилактического лечения на паллиативное и обсуждения ожидаемой продолжительности жизни, страхе ухудшения состояния, а также в предыдущем негативном опыте отмены препаратов [39]. В результате этого депрескрайбинг чаще проводится в ответ на возникшую клиническую ситуацию, а не является профилактическим [40].
По результатам национального опроса американских врачей общей практики, гериатров и эндокринологов в ситуациях без упоминания о гипогликемии при HbA1c 7,3–7,7% у пожилых пациентов большинством врачей было принято решение продолжить терапию, при этом при упоминании о любом эпизоде гипогликемии 90% врачей отмечали необходимость отмены препаратов с высоким риском гипогликемии. Однако в качестве целевого уровня HbA1c эндокринологами и врачами общей практики были выбраны более низкие показатели в отличие от рекомендованных индивидуальных целей по данным национального руководства, а гериатрами — более высокие [41].
Психологические барьеры — опасения изменений в терапии и ухудшения своего состояния — могут существенно повлиять на эффективность депрескрайбинга, особенно среди пациентов, длительно принимающих препараты. Психологическая поддержка и разъяснение преимуществ депрескрайбинга могут помочь преодолеть эти барьеры [42]. Важным аспектом является наличие близких людей, готовых поддержать пациента в процессе изменения лекарственной терапии. Поддержка со стороны семьи может улучшить соблюдение схем лечения и минимизировать стресс, связанный с отменой привычных препаратов. В исследовании D. Garfinkel [27] акцентируется внимание на важности поддержки семьи в проведении депрескрайбинга среди пожилых пациентов, однако исследований, целенаправленно изучающих эту тему, не проводилось.
Экономические аспекты депрескрайбинга
Полипрагмазия увеличивает затраты на медицинскую помощь из-за необходимости приобретения большого количества препаратов, а также из-за лечения осложнений, вызванных нежелательными лекарственными взаимодействиями и побочными эффектами. Проведение депрескрайбинга может иметь не только клинические преимущества, но и снизить экономическую нагрузку как на пациентов, так и на систему здравоохранения.
В исследовании Р. Crawford et al. [43] была оценена экономическая эффективность затрат при проведении целенаправленных мероприятий по депрескрайбингу. Участие клинического фармаколога в оптимизации приема лекарственных средств пожилыми людьми не только позволило скорректировать терапию, что привело к уменьшению риска падений, но и позволило снизить ежегодные расходы на нерекомендованные препараты [49]. Однако в литературе крайне мало исследований по оценке экономической эффективности депрескрайбинга.
Заключение
Полипрагмазия у пожилых пациентов с СД2 существенно повышает риски гипогликемии, падений и развития ГС, делая депрескрайбинг ключевым инструментом снижения клинических и экономических рисков. Однако его внедрению могут препятствовать барьеры как со стороны пациентов, так и со стороны врачей, а также отсутствие единых алгоритмов и недостаточная доказательная база, особенно в группах пациентов с КН и СА. Решение требует комплексного подхода: стандартизации рекомендаций, разработки компьютерных систем поддержки решений и учета социально-психологических факторов, что позволит оптимизировать терапию с учетом индивидуальных рисков и улучшить качество помощи
[1] International Diabetes Federation. IDF Diabetes Atlas. 10th ed. 2021. (Electronic resource.) URL: https://diabetesatlas.org/atlas/tenth-edition (access date: 25.12.2025).
2] Приказ Министерства здравоохранения Российской Федерации от 2 ноября 2012 г. № 575н «Об утверждении порядка оказания медицинской помощи по профилю клиническая фармакология». (Электронный ресурс.) URL: https://base.garant.ru/70288220/ (дата обращения: 25.12.2025).
[3] ФГБУ «НМИЦ эндокринологии» Минздрава России. База данных клинико-эпидемиологического мониторинга сахарного диабета на территории Российской Федерации. 2026. (Электронный ресурс.) URL: https://sd.diaregistry.ru/ (дата обращения: 25.12.2025).
[4] Медицинская энциклопедия: полипрагмазия. (Электронный ресурс.) URL: https://dic.academic.ru/dic.nsf/medic2/36467 (дата обращения: 25.12.2025).