Введение
11-оксигенированные андрогены (11-оксиА) — это группа С19-стероидов, синтезируемых в сетчатой зоне коркового вещества надпочечников и тканях-мишенях для глюкокортикоидных и минералокортикоидных гормонов. К предшественникам 11-оксиА, обладающим минимальной биологической активностью, относят 11β-ОН-андростендион и 11β-кетоандростендион. Агонистами рецепторов андрогенов (АР) являются 11β-кетотестостерон и 11β-кетодигидротестостерон. В группу 11-оксиА также входят 11β-ОН-тестостерон и 11β-ОН-дигидротестостерон, парциальные агонисты АР, и метаболиты 11β-ОН-андростерон и 11β-кетоандростерон [1].
11β-ОН-андростендион, являющийся вторым по активности секреции надпочечниковым андрогеном после дегидроэпиандростерона (DHEA), был идентифицирован в 1950-х годах, но расценен как побочный продукт адреналового стероидогенеза [2–4]. Исследования с применением хроматографических методов, проведенные в последние годы, продемонстрировали, что 11-оксиА участвуют как в физиологических процессах, так и в патогенезе различных заболеваний. На клеточных моделях показано, что андрогенная активность 11β-кетотестостерона и 11β-кетодигидротестостерона сопоставима при равных концентрациях с таковыми тестостерона и дигидротестостерона [5, 6]. В исследовании на опухолевых клетках, полученных от больных раком предстательной железы (РПЖ), выявлено, что 11β-кетотестостерон и тестостерон, 11β-дигидротестостерон и дигидротестостерон с одинаковой аффинностью связываются с АР и способствуют клеточному росту [7]. Была показана ассоциация повышенных уровней 11-оксиА и риска развития сахарного диабета 2 типа у мужчин [8]. У больных эндометриозом отмечено увеличение уровня 11-оксиА [9]. Определение уровня 11-оксиА предложено в качестве маркеров врожденной дисфункции коры надпочечников вследствие недостаточности 21-гидроксилазы [10], синдрома поликистозных яичников [11].
Метаболизм 11-оксиА
11-оксиА не подвержены циклическим изменениям, связанным с овуляторным циклом у женщин, но сохраняют циркадианный ритм секреции, характерный для оси гипоталамус — гипофиз — кора надпочечников [12–14]. У здоровых мужчин и женщин уровни 11β-кетотестостерона в крови сопоставимы. В отличие от классических андрогенов продукция 11-оксиА существенно не снижается с возрастом, поэтому 11β-кетотестостерон становится преобладающим активным андрогеном у женщин в постменопаузе. У женщин в репродуктивном периоде уровни 11β-кетотестостерона и тестостерона крови сопоставимы [14, 15]. Концентрация тестостерона в системном кровотоке мужчин в 15 и более раз превышает таковую 11β-кетотестостерона [16], а уровень дигидротестостерона в 20–89 раз выше уровня 11β-кетодигидротестостерона [17–19].
В коре надпочечников 11-оксиА синтезируются по Δ5-пути, в котором прегненолон превращается в DHEA, затем часть DHEA конвертируется в андростендион. 11β-гидроксилаза (CYP11B1) катализирует продукцию 11β-ОН-андростендиона из андростендиона. Наибольшее количество биологически активных 11β-кетотестостерона и 11β-кетодигидротестотерона синтезируется интракринно в периферических тканях: после поступления в клетку из системного кровотока прекурсор превращается в активный андроген и связывается с АР. Каждая клетка определяет количество активного гормона, продуцируемого внутриклеточно с помощью определенного набора ферментов. После завершения биологического действия стероид инактивируется и выводится из клетки. Необходимо отметить, что метаболиты 11-оксиА могут быть вновь превращены в агонисты АР [20].
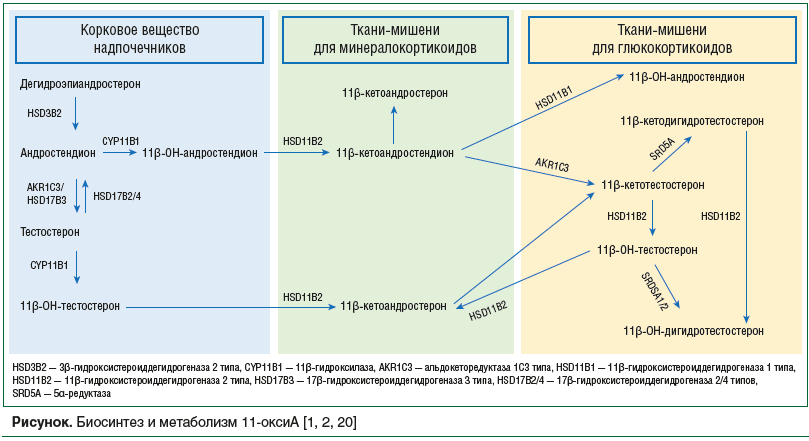
11β-ОН-андростендион является субстратом для 11β-гидроксистероиддегидрогеназы 2 типа (HSD11B2), обильно экспрессируемой в тканях-мишенях минералокортикоидов, в первую очередь в почках. HSD11B2 метаболизирует 11β-ОН-андростендион в 11β-кетоандростендион, который превращается в 11β-кетотестотерон в жировой ткани с помощью фермента альдокеторедуктазы 1С3 (AKR1C3) [1, 20]. Каталитическая эффективность AKR1C3 в 8 раз выше при превращении 11β-кетоандростендиона в 11β-кетотестотерон в сравнении с конвертацией андростендиона в тестостерон [17]. 5α-редуктаза метаболизирует тестостерон в наиболее активный классический андроген дигидротестостерон, но в качестве субстрата может использовать андростендион и его 11-оксигенированные производные. 5α-редуктаза 1 типа (SRD5A1) присутствует в большом количестве органов, включая печень и кожу. 5α-редуктаза 2 типа (SRD5A2) экспрессируется в органах мужской половой системы. SRD5A2 катализирует превращения тестостерона, в то время как SRD5A1 более эффективно метаболизирует 11-оксиА [21]. В тканях-мишенях глюкокортикоидных гормонов 11β-гидроксистероиддегидрогеназа 1 типа (HSD11B1) превращает 11β-кетоандростендион в 11β-ОН-андростендион, 11β-кетотестостерон в 11β-ОН-тестостерон, а также 11β-кетодигидротестостерон в 11β-ОН-дигидротестостерон [20]. Схема биосинтеза и метаболизма 11-оксиА представлена на рисунке.
![Рисунок. Биосинтез и метаболизм 11-оксиА [1, 2, 20] Рисунок. Биосинтез и метаболизм 11-оксиА [1, 2, 20]](https://www.rmj.ru/upload/medialibrary/656/or4unj0bjbq0pglynxifpzbmn80azopy/19-1.png)
Роль 11-оксиА в формировании и прогрессировании гормонозависимых опухолей
К группе гормонозависимых онкологических заболеваний, развитие и рост которых связаны со стероидными гормонами, относят опухоли молочной и предстательной желез, эндометрия и гонад [22]. Длительное время внимание исследователей было приковано к классическим стероидам и их рецепторам как важным факторам патогенеза данных новообразований. Опубликованные данные о биологической активности 11-оксиА привели к появлению в литературе работ, посвященных вкладу 11-оксиА в формирование и прогрессирование гормонозависимых опухолей.
Рак предстательной железы является одним из самых распространенных онкологических заболеваний мужчин [23]. Пятилетняя выживаемость больных с локализованными стадиями аденокарциномы составляет более 99%, при наличии отдаленных метастазов — 31% [24]. АР рассматривается как основное звено патогенеза РПЖ. Блокада сигнальных путей АР с помощью андроген-депривационной терапии является методом выбора лечения поздних стадий заболевания [25]. Андроген-депривационная терапия приводит к развитию более агрессивной формы опухоли — кастрационно-резистентного РПЖ [26], к патофизиологическим механизмам формирования которой относят повышение количества АР в клетках опухоли [27], мутации гена, кодирующего АР, с изменением специфичности рецептора [28], а также постоянную активацию АР в отсутствие лиганда [29]. У таких больных наблюдается снижение уровня тестостерона в системном кровотоке на 90–95%, а внутриопухолевых уровней андрогена — на 50% [30]. Выявлено увеличение внутриопухолевой экспрессии AKR1C3, SRD5A1, 3β-гидроксистероиддегидрогеназы 1 типа (HSD3B1), 17β-гидроксистероиддегидрогеназы 3 типа (HSD17B3) с повышением местной продукции дигидротестостерона [31, 32]. Исследователями было показано, что у больных на фоне андроген-депривационной терапии андрогены, их метаболиты и прекурсоры, высвобождаемые периферическими тканями, в том числе опухолью предстательной железы, наравне с корковым веществом надпочечников вносят вклад в уровень С19-стероидов в системном кровотоке [33].
На клеточной линии LNCaP, служащей для изучения развития кастрационно-резистентного РПЖ, была продемонстрирована способность клеток аденокарциномы превращать 11β-ОН-андростендион в 11β-кетотестостерон и 11β-кетодигидротестостерон [17]. Присутствие 11-оксиА определено в ткани опухолей больных кастрационно-резистентным РПЖ, а также наблюдалось увеличение уровней 11β-кетотестостерона и 11β-кетодигидротестостерона в системном кровотоке [34]. Выявление более медленной инактивации 11-оксиА по сравнению с классическими андрогенами in vitro позволило исследователям предположить, что 11-оксиА являются движущей силой формирования и прогрессирования кастрационно-резистентного РПЖ [7].
В 2022 г. C. Dahmani et al. [35] обследовали 1793 нелеченых больных с локализованным гормоночувствительным РПЖ. С помощью высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией (ВЭЖХ-МС/МС) определяли уровни классических андрогенов и 11-оксиА крови в дооперационном периоде. При проведении многофакторного анализа по Коксу выявлена ассоциация между выживаемостью без метастазов и 11-оксиА: повышение концентрации 11β-ОН-андростендиона было связано со снижением выживаемости, а увеличение уровней 11β-кетотестостерона и 11β-кетоандростерона — с лучшей выживаемостью больных локализованным РПЖ. Авторами отмечено отсутствие взаимосвязи уровня классических андрогенов крови и продолжительности жизни обследованных [35].
G. Snaterse et al. [33] методом ВЭЖХ-МС/МС исследовали уровни андрогенов крови больных (n=29) до и после лечения по поводу кастрационно-резистентного РПЖ. Исследователи показали, что 11β-кетотестостерон служит важным фактором реактивации АР у больных. Беспрогрессивная выживаемость была выше у больных с высокими уровнями 11β-кетотестостерона. Связь выживаемости больных с уровнем тестостерона крови выявлена не была.
Данные о роли андрогенов в патогенезе злокачественных новообразований (ЗНО) женской половой системы [36–39] привели к появлению работ, исследующих вовлеченность 11-оксиА в патогенез данных опухолей.
Международное агентство по изучению рака (The International Agency for Research on Cancer, IARC) в 2022 г. определило рак молочной железы (РМЖ) как наиболее распространенную опухоль, занимающую лидирующее место по смертности среди онкологических заболеваний у женщин [40]. Пятилетняя выживаемость больных с ранними стадиями опухоли превышает 90%, наличие отдаленных метастазов на этапе постановки диагноза снижает данный показатель до ≤40% [41]. Частые рецидивы на фоне проводимой терапии заставляют исследователей продолжать поиски причин прогрессирования заболевания. Нередко в ткани новообразования молочной железы наравне с рецепторами к эстрогенам определяются и АР. В исследовании R. Bleach et al. [42] подтверждена экспрессия АР в клетках первичных злокачественных опухолей молочной железы (n=875). Наличие выраженной цитоплазматической экспрессии АР было ассоциировано с худшей выживаемостью у женщин в постменопаузальном периоде, с резистентным к терапии люминальным В-подтипом РМЖ.
L.C. Houghton et al. [43] изучили взаимосвязь особенностей стероидного метаболома утренней порции мочи, исследованного методом газовой хромато-масс-спектрометрии, и риска развития РМЖ у 991 женщины с отягощенным семейным анамнезом по данному заболеванию. В работу были включены 66% женщин репродуктивного возраста. Пятилетний риск развития злокачественной опухоли молочной железы по шкале BOADICEA (Breast and Ovarian Analysis of Disease Incidence and Carrier Estimation Algorithm) у обследованных составил 0,14–23,8%. Оценка риска по данной шкале включает возраст выявления и смерти от злокачественных заболеваний родственников, а также наличие мутаций генов BRCA1 и BRCA2 у обследованной [44]. В работе увеличение экскреции с мочой 11-оксиА по сравнению с метаболитами глюкокортикоидов, прогестагенов, эстрогенов и классических андрогенов было связано с самым высоким риском развития РМЖ. Удвоение экскреции 11β-ОН-андростерона, метаболита 11β-ОН-андростендиона, было ассоциировано с увеличением риска заболевания на 91% (ОШ 1,9; 95% ДИ 1,2–3,1). Интересно, что наиболее сильная связь наблюдалась в подгруппе женщин с величиной 5-летнего риска, не превышающей 3,4%. Авторы исследования предположили, что в подгруппе больных с наивысшим риском мутации гена BRCA1 вносили больший вклад в вероятность развития заболевания, чем 11-оксиА. Возможно, это связано с тем, что мутантный белок BRCA1 способен активировать АР, конкурентно блокируя взаимодействие андрогенов с их клеточными рецепторами у больных РПЖ и РМЖ [36, 45].
J. Nakayama et al. [46] показали повышенную экспрессию HSD11B1 на клеточных линиях молочных желез человека (MCF10A, HuMEC), в которых были зафиксированы явления эпителиально-мезенхимального перехода (ЭМП), важного этапа метастазирования опухолей. В клетках с мутациями гена HSD11B1 признаков ЭМП не было. Определено 30-кратное увеличение подвижности и инвазии клеток ЗНО молочной железы с наличием неизмененной HSD11B1 по сравнению с группой контроля. В злокачественных клетках, экспрессирующих HSD11B1, показано наличие других ферментов, вовлеченных в биосинтез 11-оксиА. Авторы выдвинули гипотезу о том, что 11β-ОН-тестостерон и 11β-ОН-дигидротестостерон, образующиеся благодаря HSD11B1, индуцируют ЭМП. В клеточной линии MCF10A под воздействием 11β-ОН-тестостерона определено увеличение способности к миграции и инвазии клеток в 2 раза по сравнению с группой контроля. 11β-кетоандростендион, конкурентный селективный ингибитор HSD11B1, подавлял метастазирование, но не влиял на размер первичной опухоли молочной железы [46].
Рак тела матки (РТМ) является шестой по распространенности злокачественной опухолью у женщин [40]. Пятилетняя выживаемость больных с ранними стадиями рака эндометрия составляет 81%, с IVA и IVB стадиями — 17 и 15% соответственно [47]. Причиной развития наиболее часто встречающегося эндометриоидного подтипа считается воздействие избытка эстрогенов на эндометрий, что приводит к стимуляции митоза, а также к злокачественной трансформации железистого эпителия [48].
Опубликованы данные о повышенных уровнях тестостерона и дигидротестостерона крови у больных РТМ [49].
В исследовании C. Dahmani et al. [50] методом ВЭЖХ-МС/МС определены уровни 11-оксиА крови у 272 женщин в постменопаузальном периоде с впервые выявленным раком эндометрия до и через 1 мес. после хирургического лечения в объеме гистерэктомии с оофорэктомией. Связи 11-оксиА с клинико-патологическими характеристиками больных (стадия заболевания, гистологический тип и степень дифференцировки клеток, инвазия опухоли в миометрий и сосудистое русло) выявлено не было. Показан более высокий риск рецидива заболевания после хирургического лечения у больных с повышенными уровнями 11β-ОН-кетоандростерона в дооперационном периоде и 11β-ОН-андростерона в послеоперационном периоде. Концентрация 11-оксиА в крови снизилась через 1 мес. после хирургического лечения больных, что подтверждает вклад клеток злокачественной опухоли и/или окружающих новообразование тканей в стероидный метаболом 11-оксиА [50]. Подтверждена экспрессия SRD5A, HSD11B2, AKR1C3, ферментов, необходимых для синтеза и метаболизма 11-оксиА, в клетках аденокарцином эндометрия [38].
Так же как у больных РМЖ и РПЖ, в работе Y. Audet-Delage et al. [49] уровни тестостерона и дигидротестостерона не были связаны со сниженной выживаемостью больных раком эндометрия.
В проведенных исследованиях показана связь выживаемости больных РПЖ, РТМ с уровнем 11β-ОН-андростендиона крови, главного предшественника биологически активных 11-оксиА, и его метаболита 11β-ОН-андростерона соответственно. Риск развития РМЖ у женщин с отягощенным семейным анамнезом по данному заболеванию был ассоциирован с повышенной экскрецией с мочой 11β-ОН-андростерона. Важно отметить, что в проведенных исследованиях выживаемость не была ассоциирована с уровнями классических андрогенов.
Предполагается, что 11-оксиА могут играть роль в прогрессировании заболевания у больных кастрационно-резистентным РПЖ [1, 7, 21]. Адаптация опухоли к низким уровням классических андрогенов включает повышение экспрессии в опухолевых клетках AKR1C3, SRD5А, что способствует активации АР 11-оксиА [31, 32]. Большой интерес представляют противоречивые данные, полученные у больных с локализованными стадиями РПЖ. Как 11-оксиА способствуют рецидиву заболевания у больных вне андроген-депривационной терапии, когда уровень тестостерона превышает концентрацию 11β-кетотестостерона в системном кровотоке в 15 и более раз? Более того, как объяснить связь повышенных уровней 11β-кетотестостерона и 11β-кетоандростерона с лучшей выживаемостью без метастазов у больных с локализованной аденокарциномой, и 11β-кетотестостерона с лучшей беспрогрессивной выживаемостью у больных с кастрационно-резистентным РПЖ? Авторами выдвинута гипотеза о том, что опухолевые клетки, полагающиеся на андрогензависимую активацию АР, могут обладать преимуществами на фоне сохраняющегося уровня андрогенов в системном кровотоке, что приводит к лучшему ответу больных на терапию, направленную на сигнальные пути АР [33]. Гипотезе противоречат данные о формировании андрогеннезависимых механизмов резистентности на фоне данной терапии, что ассоциировано со снижением выживаемости больных [26–29].
Опираясь на результаты исследования J. Nakayama et al. [46], показавших важность экспрессии фермента HSD11B1 для метастазирования клеток опухоли молочной железы, можно предположить, что данный фермент играет ключевую роль и в прогрессировании РПЖ. HSD11B1 превращает 11β-кетоандростендион в 11β-ОН-андростендион, который может в последующих реакциях метаболизироваться в активный 11-оксиА. Превращение 11β-кетотестостерона и 11β-кетодигидротестостерона в 11β-ОН-тестостерон и 11β-ОН-дигидротестостерон, способствующие метастазированию клеток, также происходит с помощью HSD11B1. Возможно, более низкая экспрессия данного фермента в периферических тканях, в том числе в опухоли, приводит к меньшей интракринной конвертации 11-оксиА в активные агонисты АР, а также 11β-ОН С19 стероиды, что связано с лучшей выживаемостью таких больных.
Заключение
На протяжении 50 лет считалось, что 11-оксиА не обладают биологической активностью. Работы с применением хроматографических методов позволили охарактеризовать стероидный метаболом 11-оксиА и уточнить процессы синтеза и метаболизма данных гормонов. Выдвинуто предположение о том, что изменения интракринной метаболомики 11-оксиА нарушают местный и системный гомеостаз. Несмотря на это, внутриклеточный стероидогенез остается недостаточно изученным. Эффекты андрогенов в организме человека крайне многообразны. Стероидные гормоны могут служить факторами необратимого изменения фенотипа клеток-мишеней. Кроме того, разные эндокринные функции связаны между собой, и один гормон может влиять на элементы биодинамики другого гормона. Картина биосинтеза и метаболизма андрогенов продолжает усложняться. В литературе все чаще появляются данные о влиянии 11-оксиА на развитие и прогрессирование гормонозависимых ЗНО. Экспериментальные и первые клинические работы подтвердили, что 11-оксиА не только участвуют в физиологических процессах, но и могут служить биомаркерами развития и прогрессирования злокачественных опухолей репродуктивных органов человека. Необходимы дальнейшие исследования для подтверждения и внедрения полученных результатов в клиническую практику.