Введение
Сахарный диабет 2 типа (СД2) и гипертоническая болезнь (ГБ) являются распространенным примером коморбидной патологии, что определяет более высокий риск развития микро- и макрососудистых осложнений у данной категории пациентов [1]. Функциональные и морфологические изменения, обусловленные диабетической и гипертензивной микроангиопатией, диабетической кардиомиопатией, в конечном итоге способствующие раннему развитию панваскулярного атеросклероза, на ранних стадиях могут не иметь выраженных субъективных и объективно регистрируемых проявлений. Однако установлено, что, в частности, у пациентов с СД2 и микрососудистой дисфункцией миокарда даже при отсутствии обструктивной ишемической болезни сердца (ИБС) прогноз хуже: выше частота госпитализаций по поводу сердечной недостаточности (СН), риск внезапной сердечной смерти и инфаркта миокарда (ИМ) [2–5]. Ранним изменением функции сердца у больных с СД2 и ГБ является диастолическая дисфункция левого желудочка сердца (ДД ЛЖ), не сопровождающаяся субъективными клиническими проявлениями на ранних стадиях и являющаяся начальным этапом развития СН [6]. Зачастую верификация диагноза СН совпадает с манифестацией явных симптомов и признаков СН, что исключает возможность раннего терапевтического вмешательства, наиболее перспективного с точки зрения торможения механизмов развития сердечно-сосудистого континуума.
Следует отметить, что, несмотря на успехи, достигнутые в лечении СН, терапия недостаточно эффективна в отношении прогноза заболевания и качества жизни пациентов — СН по-прежнему является основной причиной преждевременной смерти пациентов с СД2 [7]. Плейотропные эффекты новых классов сахароснижающих препаратов (ССП) открыли дополнительные перспективы управления повышенным сердечно-сосудистым риском (ССР) коморбидных пациентов с СД2 и ГБ. К препаратам выбора с доказанным улучшением исходов для пациентов с повышенным ССР относят ССП класса ингибиторов натрий глюкозного котранспортера 2 типа (иНГЛТ-2). Кардиопротективные эффекты иНГЛТ-2 доказаны в крупных рандомизированных клинических исследованиях (РКИ) сердечно-сосудистой безопасности эмпаглифлозина, канаглифлозина и дапаглифлозина (EMPA-REG OUTCOME [8], CANVAS [9], DECLARE [10] соответственно) в группах пациентов очень высокого ССР, большинство из которых имели АССЗ, включая ИМ и/или мозговой инсульт. В 2025 г. в «Алгоритмы специализированной медицинской помощи больным сахарным диабетом» в качестве препаратов преимущественного выбора для пациентов с СД2 и повышенным ССР были включены ипраглифлозин и лусеоглифлозин, несмотря на отсутствие результатов крупных РКИ [11]. Важно заметить, что недавно опубликованный систематический обзор и метаанализ 453 исследований, в которых оценивался 21 препарат из 9 классов ССП, показал, в частности, что у пациентов с более низким ССР, ранее не принимавших лекарства, не обнаруживается различий между методами лечения СД2 и плацебо в отношении сердечно-сосудистых осложнений [12], что еще раз указывает на необходимость применения принципов прецизионной медицины в отношении такой клинически и прогностически гетерогенной группы, как пациенты с СД2. На сегодняшний день недостаточно данных о плейотропных эффектах иНГЛТ2 в группе пациентов с СД2 без АССЗ, крупные целенаправленные исследования эффективности ипраглифлозина в группе коморбидных пациентов с СД2 и ГБ без АССЗ не проводились.
Цель исследования: оценить клиническую эффективность ипраглифлозина в группе пациентов с СД2 и ГБ с ДД ЛЖ сердца без АССЗ.
Материал и методы
Проведено одноцентровое открытое проспективное сравнительное исследование в группе пациентов с СД2 и ГБ без АССЗ на базе кафедры внутренних болезней и семейной медицины дополнительного профессионального образования ФГБОУ ВО ОмГМУ Минздрава России и в БУЗОО «ККД» в период с 2023 по 2026 г. Исследование одобрено локальным этическим комитетом ФГБОУ ВО ОмГМУ Минздрава России (протокол № 10 от 19.09.2023).
Критерии включения: подписанное информированное согласие об участии в исследовании, возраст 18–65 лет; наличие ГБ, СД2, ДД ЛЖ; противодиабетическая и гипотензивная терапия неизменна в течение 12 нед., предшествующих включению в исследование; гликированный гемоглобин (HbA1c) <10,0%; индекс массы тела (ИМТ) <40 кг/м2. Критерии невключения: СД 1 типа, симптоматическая артериальная гипертензия, HbA1c >10%, фракция выброса (ФВ) ЛЖ <50%, прием препаратов группы иНГЛТ-2, агонисты рецепторов глюкагоноподобного пептида (арГПП-1); фибрилляция предсердий; АССЗ и неатеросклеротические ССЗ (кардиомиопатии, миокардиты) в анамнезе; гемодинамически значимые пороки сердца, анемии различного генеза, сопутствующие заболевания или патологические состояния, не перечисленные выше, которые могут исказить результаты исследования (печеночная недостаточность, почечная недостаточность, остеопороз, злоупотребление алкоголем, употребление наркотиков, терапия системными глюкокортикостероидами, изменение суточной дозы L-тироксина в течение 2 мес. до включения в исследование, медикаментозная терапия ожирения, онкологические заболевания и пр.).
В ходе исследования применяли критерии исключения: отзыв согласия пациента на участие в исследовании; невозможность наблюдения за пациентом (потеря контакта); развитие заболеваний/состояний, соответствующих критериям невключения; непереносимость ипраглифлозина; существенные нарушения протокола.
В исследовании методом последовательного включения по половозрастным характеристикам были сформированы 2 группы: группа 1 (n=30) получала ипраглифлозин в дозе 50 мг 1 р/сут в монотерапии или в комбинации с другими CCП; группа 2 (n=30) — группа сравнения, получала ранее назначенную терапию без коррекции в ходе наблюдения.
Исходно и через 12 нед. наблюдения всем пациентам проводили антропометрические измерения (рост, масса тела (МТ), окружность талии (ОТ)) и расчет индексов: ИМТ, индекс формы тела (A Body Shape Index, ABSI), индекс округлости тела (Body Roundness Index, BRI) [13]). Выполняли лабораторно-инструментальные исследования, в том числе оценивали биохимические показатели, показатели углеводного (глюкоза крови, HbA1c) и липидного обмена, ремоделирования сердца (предшественник мозгового натрийуретического пептида (N-terminal pro B-type natriuretic peptide, NT-proBNP)), деградации коллагена I типа (C-терминальный телопептид коллагена I типа, СТХ), эхокардиографические (ЭхоКГ), электрокардиографические (ЭКГ, Холтер-ЭКГ), гемодинамические (суточный мониторинг артериального давления (СМАД)) характеристики сердечно-сосудистой системы. Двухмерную ЭхоКГ (ультразвуковой сканер Toshiba Aplio 400, Япония) выполняли с оценкой ФВ ЛЖ по Симпсону, диастолической функции ЛЖ по стандартному протоколу одним оператором [14–16]. ЭКГ, Холтер-ЭКГ (электрокардиограф Schiller АТ-2, Швейцария) проводили по общепринятой методике [17–19]. Для СМАД использовали регистратор Schiller (Швейцария) с последующим анализом результатов на IBM PC-совместимом компьютере (программа «МТ-200» «БиПиЛаб» Н #14060875 Rev.BP2005-01.04.00.2540). Расчет размера выборки осуществлялся с применением калькулятора G*Power [20], расчетный размер группы составил 27 человек. Статистический анализ проводили с использованием программных пакетов анализа Microsoft Excel, Statistica 6.0 (StatSoft Inc., США). Значения количественных признаков представлены как медиана и межквартильный интервал в виде Me (Q1; Q3). Категориальные переменные выражались как число (процент). При сравнении выборок по количественным и качественным признакам в двух зависимых группах использовали критерии Уилкоксона (Т) и χ2 Мак-Немара с поправкой Йейтса соответственно, в двух независимых группах использовали критерий Манна — Уитни (U) и χ2 соответственно. Для оценки взаимосвязи различных факторов и клинических исходов рассчитывали относительный риск (ОР), границы 95% доверительного интервала (95% ДИ). Выявление факторов риска (ФР) и построение прогнозной модели осуществляли посредством обработки структурированных табличных клинических данных с применением нейросетевой архитектуры глубокого обучения TabNet, для интерпретации решений модели применяли SHAP-анализ. Во всех процедурах статистического анализа порог статистической значимости р считали равным 0,05 (5%).
Результаты и обсуждение
Группы были сопоставимы по полу и возрасту, значимо не различались по длительности СД2 и ГБ, микрососудистым осложнениям, ИМТ, ОТ, уровням HbA1c и АД (p>0,05).
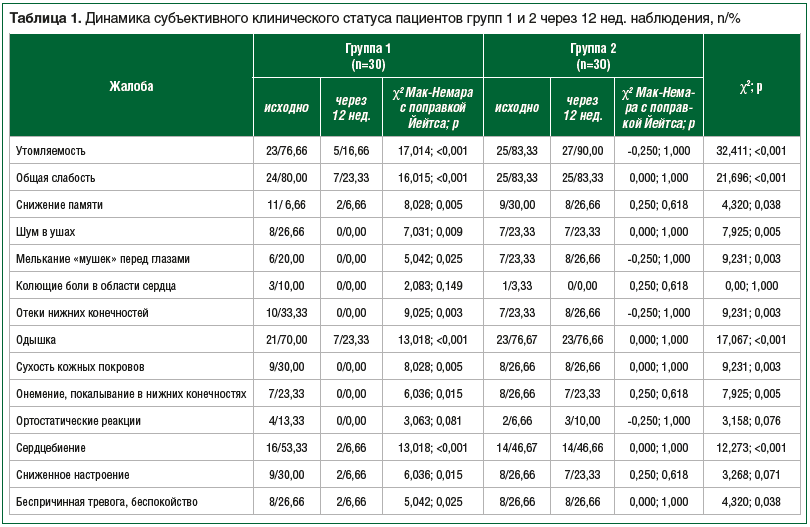
Исходно абсолютное большинство пациентов группы 1 (n=27) и группы 2 (n=28) (χ2=0,218, р=0,641) предъявляли какие-либо жалобы (табл. 1). Только в группе 1 через 12 нед. была отмечена значимая положительная динамика субъективного статуса. При сравнении групп меньшее количество пациентов группы 1 предъявляли указанные жалобы через 12 нед. наблюдения (n=13 и n=28 соответственно, χ2=17,330, р<0,001).

Через 12 нед. исследования только в группе 1 отмечена положительная динамика антропометрических параметров: достоверное снижение МТ от исходной величины (100 (93; 111) кг и 97 (89; 108) кг соответственно; T=0,00; р<0,001), ИМТ (34,44 (32,0; 37,8) кг/м2 и 33,44 (31,17; 36,92) кг/м2 соответственно; Т=0,00; р<0,001), ОТ (113 (108; 119) см и 110,5 (106; 116) см соответственно; Т=0,00; р<0,001). Через 12 нед. была отмечена значимая разница между группами по МТ (U=180,50; р=0,0178). Дельта МТ через 12 нед. в группе 1 составила 3,0 (2,0; 4,0) кг. Наблюдаемая динамика МТ соответствует результатам опубликованных исследований — при использовании иНГЛТ2 продемонстрировано умеренное снижение массы тела в диапазоне от 2 до 4 кг в течение периода от 6 до 12 мес. [21]. В нашем наблюдении впервые отмечено улучшение показателей ABSI и BRI через 12 нед. на фоне терапии ипраглифлозином (рис. 1, 2). В группе 2 не было выявлено динамики перечисленных показателей.


Следует отметить, что расчетные показатели BRI и ABSI (доля и распределение висцерального жира) рассматриваются в настоящее время как более надежные в отношении оценки метаболического статуса и прогноза сердечно-сосудистых осложнений в различных группах пациентов в сравнении с традиционной интерпретацией ИМТ [13, 22–24].
На фоне терапии ипраглифлозином отмечено значимое снижение уровня глюкозы (Т=20,00; р<0,001), HbA1c (Т=28,00; р<0,001) при отсутствии значимых изменений уровня креатинина, рСКФ, электролитов (p>0,05). После 12 нед. лечения ипраглифлозином отмечалось значимое снижение уровня АЛТ (Т=104,50; р=0,008), мочевой кислоты (Т=106,00; р=0,027), триглицеридов (ТГ) (Т=108,00; р=0,017), триглицеридно-глюкозного индекса (ТГИ) (Т=54,00; р=0,000), что согласуется с клинической оценкой эффектов иНГЛТ2 в целом [25]. Улучшение показателей ТГ, ТГИ и АЛТ обращает на себя внимание в связи с опубликованными результатами байесовского метаанализа, продемонстрировавшего значимое влияние ипраглифлозина на снижение уровня ТГ [26], и с результатами метаанализа о положительном влиянии ипраглифлозина на ферменты печени [27]. В группе 2 значимые изменения по антропометрическим и метаболическим параметрам не отмечались (р>0,05). Через 12 нед. группа 1 значимо отличалась от группы 2 по уровню глюкозы (U=183,00; р<0,001), HbA1c (U=245,50; р<0,05), холестерина липопротеинов высокой плотности (ХС-ЛПВП) (U=316,50; р<0,05) и NT-proBNP (U=289,50; р<0,05).
Отмечена положительная динамика амбулаторного систолического АД (САД) в группе 1 (со 140 (130; 155) до 128 (120; 130) мм рт. ст. через 12 нед. (Т=34,50; р<0,001). В группе 2 изменений в офисном САД не выявлено (Т=133,0; р=0,627). Через 12 нед. в группе 1 отмечено значимое уменьшение ПАД (Т=92,50; р=0,011), в группе 2 значимых изменений не отмечалось (T=151,00; р=0,361). Таким образом, полученные данные подтверждают наличие у ипраглифлозина гипотензивного эффекта, свойственного классу иНГЛТ-2. В одном из крупнейших систематических обзоров и метаанализов 43 исследований (n=22 528), анализирующем влияние иНГЛТ2 на уровень АД у пациентов с СД2, было показано, что в сравнении с плацебо и другими ССП иНГЛТ-2 снижали САД и диастолическое АД (ДАД) соответственно на 2,46 и 1,46 мм рт. ст. [28]. В метаанализе 7 исследований с участием 2381 пациента с СД2 терапия иНГЛТ2 в течение 4–12 нед. привела к снижению 24-часового амбулаторного САД на 3,61 мм рт. ст. по сравнению с таковым при применении плацебо [29]. В нашем исследовании при оценке краткосрочной вариабельности АД по СМАД в группе 1 отмечено значимое снижение среднего САД в ночное время (Т=75,00; р=0,010) и вариабельности ДАД в дневные часы (Т=57,50; р=0,025). В группе 2 значимых изменений по СМАД не выявлено (р>0,05).
По данным ЭКГ в покое значимой динамики частоты сердечных сокращений (ЧСС) в группах не отмечалось. Медиана исходной ЧСС в группе 1 составила 74,5 (67; 81) в 1 мин, через 12 нед. терапии — 73 (68; 78) в 1 мин (Т=124,00; р=0,072). Таким образом, зарегистрированное в группе 1 снижение АД не сопровождалось приростом ЧСС. В группе 2 ЧСС исходно составила 74 (70; 80) в 1 мин, через 12 нед. — 75 (69; 81) в 1 мин (Т=64,50; р=0,856). Через 12 нед. наблюдения значимой разницы ЧСС по ЭКГ в группах не отмечалось (U=368,50; р=0,288).
При оценке параметров ЭКГ в группе 1 отмечено укорочение интервала QT с 0,390 (0,376; 0,410) до 0,380 (0,350;0,400) с через 12 нед. терапии (Т=89,00; р=0,005), показатели сохранялись в пределах референтных значений (0,320–0,450). Наше наблюдение соотносится с результатами исследований других препаратов класса иНГЛТ2, показавшими отсутствие значимого влияния иНГЛТ2 на электрическую активность сердца у пациентов с нормальным сердечным ритмом [30]. При расчете индекса электрофизиологического баланса сердца (index of cardio-electrophysiological balance, iCEB), рассчитываемого на основе стандартной ЭКГ [31], показано, что у всех пациентов iCEB находился в пределах референтного диапазона (нормальное значение показателя iCEB составляет 4,24; референтный диапазон 3,14–5,35). В настоящее время iCEB, отражающий продолжительность процессов деполяризации и реполяризации, используется для прогнозирования потенциального риска злокачественных желудочковых аритмий и внезапной сердечной смерти [32]. Через 12 нед. в группе 1 отмечено значимое снижение от исходного показателя 4,19 (4,00; 4,57) до 3,98 (3,66; 4,47) (Т=11800; р=0,019). По Холтер-ЭКГ у всех пациентов (n=60) исходно регистрировались эпизоды синусовой тахикардии и суправентрикулярных экстрасистол. Желудочковые экстрасистолы I класса (по Лауну — Вольфу) отмечались у большинства пациентов в группе 1 (28/30) и в группе 2 (24/30) (χ2=2,308; р=0,129). Через 12 нед. приема ипраглифлозина отмечалось значимое снижение количества эпизодов суправентрикулярных (Т=107,00; р=0,049) и желудочковых экстрасистол (Т=73,50; р=0,017). В группе 2 динамика не выявлена (р>0,05). При сравнении групп через 12 нед. по количеству эпизодов нарушения ритма статистически значимых изменений не выявлено (р>0,05).
При анализе временных показателей вариабельности сердечного ритма, отражающих общий тонус вегетативной нервной системы, отмечалось снижение вариабельности R-R (NN) (возрастная норма — 813–851 мс) в группе 1 (р<0,05), в группе 2 изменений не выявлено (р>0,05). Через 12 нед. терапии в группе 1 минимальная ЧСС по Холтер-ЭКГ была значимо ниже, чем в группе 2 (U=212,00; р<0,001).
По данным ЭхоКГ исходно у всех пациентов (n=60) диагностирована ДД ЛЖ I степени. При оценке ЭхоКГ-показателей в группе 1 отмечен статистически значимый прирост максимальной скорости кровотока раннего диастолического наполнения (Е) и отношения Е к максимальной скорости кровотока во время предсердной систолы (А) через 12 нед. терапии, в группе 2 изменений не отмечалось (p>0,05) (табл. 2). При сравнении двух групп исходно отмечена разница в объеме левого предсердия (ЛП) (U=263,00; р=0,006), которая сохранялась через 12 нед. наблюдения.

Через 12 нед. наблюдения критерии ДД ЛЖ не были достигнуты в группе 1 у 14/30 пациентов (χ2 Мак-Немара с поправкой Йейтса=13,018; р<0,001) и сохранялись у всех пациентов группы 2 (χ2 Мак-Немара с поправкой Йейтса=18,26; р=0,000). Также через 12 нед. наблюдения было отмечено значимое снижение уровня NT-proBNP в группе 1 (21,2 (10,0; 112,2) и 10,7 (4,1; 44,7) пг/мл соответственно, исходно и через 12 нед. терапии; Т=46,00; р<0,001). В группе 2 статистически значимой динамики показателя не отмечено (21,85 (12,0; 108,0) и 22,0 (13,0; 110,0) пг/мл соответственно, исходно и через 12 нед. наблюдения; Т=17,50; р=0,054).
Для клинического анализа возможных факторов, которые могут влиять на эффективность терапии ипра-глифлозином, мы разделили группу 1 на 2 подгруппы: подгруппу А — пациенты с устраненной ДД ЛЖ (n=14), подгруппу Б — пациенты с сохраняющимися признаками ДД ЛЖ (n=16). В подгруппе Б было значимо больше пациентов, которые курили. Статус курения в рассматриваемой группе пациентов повышал вероятность сохранения ДД ЛЖ на фоне 12-недельной терапии ипраглифлозином в 2,33 раза (относительный риск (ОР)=2,33 (95% ДИ 1,291; 4,218); р=0,003; специфичность 0,929; чувствительность 0,500) (рис. 3). В подгруппе А на фоне приема ипраглифлозина значимо снизилось ПАД с 60 (58; 69) до 50 (45; 58) мм рт. ст. (Т=4,50; р=0,004). При низких значениях ПАД (Q1<45,25 мм рт. ст. (ОР=0,099 (95% ДИ 0,010; 0,949); р=0,022) ОР сохранения ДД ЛЖ значимо снижался. В подгруппе Б динамики ПАД не было отмечено (48 (39,25; 60,25) и 50 (41,50; 50,75) мм рт. ст. соответственно исходно и через 12 нед. наблюдения; Т=54,50; р=0,756). Соответственно, подгруппы значимо различались по показателю Δ ПАД (U=51,50; р=0,013).
В подгруппе А отмечен более низкий исходный уровень СТХ (0,175 (0,125; 0,264) 0,292 (0,223; 0,426) нг/мл соответственно в подгруппах А и Б), более значимые изменения через 12 нед. терапии (Δ СТХ 0,071 (0,030; 0,135) и 0,021 (0,012; 0,042) нг/мл соответственно в подгруппах А и Б), без значимых различий через 12 нед. наблюдения (0,219 (0,128; 0,260) и 0,305 (0,216; 0,407) нг/мл соответственно в подгруппах А и Б, U=65,50; р=0,056). При анализе установлено, что ОР сохранения ДД ЛЖ повышался в 1,8 раза при верхнем квартиле исходного уровня СТХ (Q4>0,299 нг/мл, ОР=1,833) и в 2 раза при наименьшей динамике CТХ (Q1 ΔСТХ) за 12 нед. (см. рис. 3). В отдельных отечественных и зарубежных исследованиях продемонстрировано значение СТХ как перспективного показателя прогноза СН и эффектов медикаментозной терапии [33, 34]. Полученные нами данные согласуются с представлениями о роли деградации коллагена в патогенезе ремоделирования миокарда и развития ДД ЛЖ, однако для уточнения прогностической значимости определения СТХ и возможности его использования в качестве терапевтической мишени требуются дополнительные исследования с включением большего числа пациентов и оценкой динамики маркера на фоне лечения.

В исследуемой группе пациентов из 44 исходных клинических признаков классификатором TabNet были выделены 12 наиболее информативных предикторов, характеризующих статус курения, параметры диастолической функции и ремоделирования сердца (объем ЛП, конечно-диастолический объем (КДО), Е/е’, иММЛЖ, NT-proBNP), маркер деградации коллагена I типа (СТХ). Для количественной оценки вклада каждого признака в прогнозирование модели использовали метод постфактумной интерпретации — SHAP-анализ с применением LinearExplainer для логистической регрессии с последующим определением перестановочной важности (рис. 4).

Продемонстрировано, что Δ СТХ остается ведущим предиктором — перестановка его значений снижает AUC в среднем на Δ AUC=0,108 (SD=0,044); на втором месте — иММЛЖ-1 (Δ AUC=0,035), далее СТХ-1 (Δ AUC=0,024), Δ ПАД (Δ AUC=0,024) и ПАД-1 (Δ AUC=0,020); последние два признака (КДО-1 и Е/е’-1) имеют нулевое Δ AUC, что свидетельствует об их минимальном самостоятельном вкладе в дискриминирующую способность после учета остальных признаков. Положительный паттерн интерпретации Δ СТХ, полученный при SHAP-анализе (рис. 5), в прогнозной модели означает, что рост СТХ ассоциирован с вероятностью ответа на терапию в отношении ДД ЛЖ, что, по аналогии с другим, более изученным маркером резорбции коллагена I типа — СITP [35], может отражать процесс уменьшения количества сшивок коллагеновых волокон, снижение плотности межуточной ткани, уменьшение жесткости миокарда, соответствуя улучшению диастолической функции. Доминирующая роль биомаркера резорбции коллагена (Δ СТХ, СТХ-1, СТХ-2) в предиктивной модели может отражать его взаимосвязь с процессами ремоделирования сердца с развитием фиброза при СД2 и ГБ как возможной точки приложения эффектов ипраглифлозина. Показатели Δ ПАД, ПАД-1, ИММЛЖ-1 образуют второй кластер по важности, что подчеркивает роль ГБ и процесса ремоделирования ЛЖ в дифференциации ответа на терапию.

Таким образом, в нашей когорте «портрет» пациента без положительной динамики ДД ЛЖ на фоне терапии ипраглифлозином можно представить следующим образом: это пациент любого пола, курильщик, имеющий исходно высокие уровни СТХ и ПАД, в процессе терапии которого регистрируется незначительная динамика СТХ.
Полученные результаты демонстрируют высокую предсказательную ценность логистической регрессии для задачи классификации ответчиков/неответчиков на терапию. ROC AUC=0,915 при n=30 свидетельствует об эффективности используемого подхода к отбору признаков и оценке модели (рис. 6).

Прогнозная модель эффективности ипраглифлозина в 12-недельном наблюдении в группе пациентов с СД2, ГБ и ДД ЛЖ продемонстрировала точность 0,80, чувствительность 0,857 при специфичности 0,750 в условиях LOO-кросс-валидации на выборке из 30 пациентов.
Заключение
В краткосрочном сравнительном исследовании использование ипраглифлозина для лечения СД2 у коморбидных пациентов с СД2 и ГБ с ДД ЛЖ, без АССЗ сопровождалось улучшением функциональных показателей деятельности сердца, устранением эхокардиографических признаков ДД ЛЖ (46,67% пациентов), снижением уровня NT-proBNP. Также была отмечена значимая положительная динамика субъективного клинического статуса, антропометрических параметров (МТ, ИМТ, ОТ, BRI, ABSI), метаболических и функциональных показателей (глюкоза, HbA1c, ХС-ЛПВП, АЛТ, мочевой кислоты, ТГ, ТГИ). Через 12 нед. терапии была отмечена значимая разница между сравниваемыми группами по антропометрическим, метаболическим показателям и структурно-функциональным характеристикам сердечно-сосудистой системы. На фоне приема ипраглифлозина отмечено снижение офисного САД и ПАД без увеличения ЧСС, улучшение характеристик краткосрочной и долгосрочной вариабельности АД, снижение количества эпизодов суправентрикулярных и желудочковых экстрасистол, укорочение интервала QT в пределах нормального диапазона, снижение индекса электрофизиологического баланса сердца, зарегистрировано повышение уровня СТХ. Относительный риск сохранения ДД ЛЖ на фоне терапии ипраглифлозином в исследуемой группе был значимо выше при уровне СТХ >0,299 нг/мл, Δ СТХ <0,019, ПАД >45,25 мм рт. ст., положительном статусе курения.
Модель глубокого обучения TabNet позволила выделить 12 значимых показателей, из которых наибольший вклад в прогноз ответа на терапию ипраглифлозином вносили: биомаркер резорбции коллагена (Δ СТХ, СТХ-1, СТХ-2), гемодинамический показатель (Δ ПАД, ПАД-1), показатель ремоделирования ЛЖ (иММЛЖ-1). Построенная прогнозная модель характеризовалась точностью 0,80, чувствительностью 0,857 при специфичности 0,750 в условиях LOO-кросс-валидации на выборке из 30 пациентов. Данная модель может быть использована в клинической практике для повышения эффективности медикаментозной терапии ипраглифлозином в группе пациентов с СД2, ГБ без АССЗ.
С учетом того, что гетерогенность ответа на медикаментозное лечение существенно возрастает при наличии коморбидных состояний, разработка предиктивных моделей эффективности терапии на основе многомерного анализа в группе пациентов с СД2 и ГБ является важной задачей, открывающей возможности стратификации пациентов по вероятности ответа на терапию, такой как переход от эмпирических протоколов лечения к персонализированным терапевтическим стратегиям. Перспективными направлениями дальнейшего исследования прогностического моделирования эффективности терапии ипраглифлозином в группе коморбидных пациентов с СД2 и ГБ являются расширение когорты пациентов, применение методов аугментации данных, включение временны´х рядов биомаркеров, исследование нелинейных взаимодействий признаков, увеличение длительности наблюдения с возможной коррекцией значимых исходов (неблагоприятные сердечно-сосудистые события) в отдаленном периоде наблюдения.