Введение
Целиакия представляет собой хроническое, системное, аутоиммунное заболевание, развивающееся у генетически предрасположенных людей, при котором употребление глютена приводит к повреждению тонкой кишки [1, 2].
Сахарный диабет 1 типа (СД1) — это многофакторное заболевание, в основе которого лежит иммуноопосредованная или идиопатическая деструкция β-клеток поджелудочной железы, приводящая к абсолютной инсулиновой недостаточности1.
Общие средовые провоцирующие факторы, сходные гены предрасположенности и особенности патогенеза целиакии и СД1 определяют частую ассоциацию данных заболеваний [3–6]. Роль безглютеновой диеты в улучшении контроля СД1 остается предметом дискуссий. Однако не вызывает сомнений, что долгосрочные осложнения нераспознанной целиакии, такие как задержка физического и полового развития, дефицитные состояния, репродуктивные нарушения и онкологические заболевания, могут быть предотвращены при своевременной диагностике глютеновой энтеропатии и начале диетотерапии [7]. Результаты проведенных исследований свидетельствуют в пользу преимущественно малосимптомного течения целиакии в ассоциации с СД1 [8], ввиду чего единственным способом ее ранней диагностики является проведение регулярного скрининга у эндокринологических пациентов.
Цель исследования: оценить эффективность серологического скрининга на целиакию у детей с СД1.
Материал и методы
Для ретроспективного клинического исследования были отобраны истории болезни 1372 пациентов, проходивших стационарное обследование в отделении эндокринологии ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ» в период с 11.01.2022 по 30.05.2025 с основным диагнозом СД1, не имевших ранее установленного диагноза целиакии и выполнивших исследование концентрации антител (Ig) к тканевой трансглутаминазе класса A (tTG-IgA). Серологическая диагностика целиакии выполнялась с использованием иммуноферментного анализа сыворотки крови. Положительный результат фиксировался при концентрации антител более 10 Ед/мл.
Подход к ведению серопозитивных пациентов был дифференцированным. Эндоскопическое исследование (фиброэзофагогастродуоденоскопия (ФЭГДС) с забором биоптатов слизистой двенадцатиперстной кишки) рекомендовалось всем детям с наличием симптомов, настораживающих в отношении целиакии, а также бессимптомным пациентам с повышением tTG-IgA более 3 норм. В случае незначительного повышения tTG-IgA в пределах 3 норм детям было рекомендовано выполнить серологический контроль через 3 мес. пребывания на глютенсодержащей диете и провести эндоскопическое исследование при сохранении серопозитивности. Диагноз целиакии считался подтвержденным при выявлении у серопозитивных пациентов характерных гистологических изменений в виде атрофической энтеропатии с межэпителиальным лимфоцитозом в стадии Marsh 2–3 согласно классификации Marsh-Oberhuber [1]. Группу пациентов, требующих динамического наблюдения, составили дети и подростки, не выполнившие к моменту анализа данных контрольное исследование концентрации антител или отказавшиеся от проведения эндоскопического исследования.
Статистическая обработка включала методы описательной статистики при использовании программы Microsoft Office Excel и анализ выживаемости (Kaplan — Meier), оценивающий интервал от дебюта СД1 до выявления целиакии. Учитывая, что распределение данных отличалось от нормального, результаты представлены в виде медианы и 1-го и 3-го квартилей (Ме [Q1; Q3]).
Результаты исследования
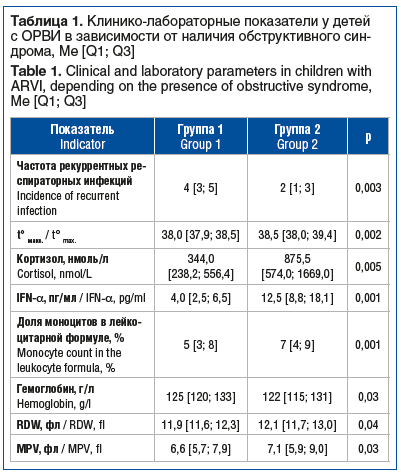
В группу исследования были включены пациенты с СД1 от 0 до 17 лет, 52,4 и 47,6% мальчиков и девочек соответственно. Возраст обследованных детей составил 8,1 [8,0; 15,2] года. 479 детей выполнили скрининг на целиакию в дебюте СД1, 893 — обследованы через 3 мес. и более после постановки диагноза СД1. Повышение уровня tTG-IgA было зафиксировано у 80 (5,84%) детей. Характеристика обследованных пациентов в зависимости от стажа СД1 представлена в таблице. Эндоскопическое и патоморфологическое исследования были выполнены 49 детям с повышением концентрации tTG-IgA, по результатам которых целиакия была верифицирована в 48 (3,6%) случаях.
По результатам нашего исследования, 30 (37,5%) пациентов продемонстрировали низкую серопозитивность с повышением концентрации tTG-IgA в пределах 3 норм. Выжидательная тактика у бессимптомных пациентов продемонстрировала нормализацию концентрации антител у 6 детей, преимущественно в группе дебюта СД1. При низкой серопозитивности ФЭГДС с забором биоптатов слизистой двенадцатиперстной кишки выполнена 1 ребенку с дебютом СД1 и 7 пациентам со стажем заболевания более 3 мес. в связи с наличием симптомов, настораживающих в отношении глютеновой энтеропатии (патологическая задержка роста, частые боли в животе, эпизоды разжиженного стула, повышенное выпадение волос). По результатам морфологического исследования диагноз целиакии был окончательно подтвержден во всех случаях в группе пациентов со стажем СД1 и не подтвержден у ребенка в дебюте СД1. В группе 14 детей с повышением tTG-IgA в пределах 4–9 норм спонтанной нормализации концентрации антител при динамическом наблюдении определено не было. ФЭГДС с биопсией была выполнена 9 (64,3%) пациентам, по результатам гистологического исследования целиакия была верифицирована в 100% случаев с равномерным распределением в группах с дебютом и стажем СД1. При повышении концентрации tTG-IgA до уровня 10 норм и более эндоскопическое исследование проведено всем пациентам при стаже диабета более 3 мес. и 76,5% больных с дебютом СД1. Во всех случаях выявленные гистологические изменения соответствовали наличию атрофической энтеропатии с межэпителиальным лимфоцитозом в стадии Marsh 2–3. Четверо детей с высокой концентрацией tTG-IgA отказались от выполнения эндоскопии ввиду отсутствия симптомов поражения желудочно-кишечного тракта и нежелания проводить инвазивное исследование.
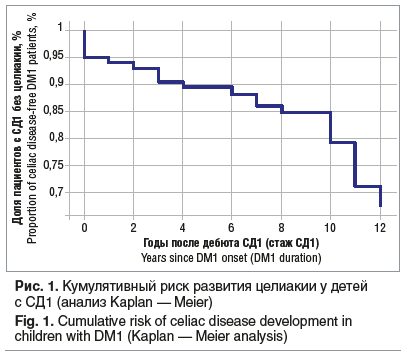
Метод анализа выживаемости (Kaplan — Meier) продемонстрировал, что большинство случаев целиакии было диагностировано в первые 5 лет от начала СД1 (рис. 1). Кумулятивный риск целиакии к 5-му году после дебюта СД1 составил около 1,6%, оставаясь выше среднепопуляционного.



Медианный возраст дебюта СД1 в группе детей с подтвержденной целиакией был статистически значимо ниже, чем у пациентов с изолированным СД1, — 6,5 [4,2; 9,1] и 8,0 [8,1; 14,08] года соответственно (р=0,012). Анализ распределения обследованных пациентов по возрасту (рис. 2) показал, что большинство случаев целиакии у пациентов с СД1 было выявлено в группе дошкольного (45,1%) и младшего школьного (43,1%) возраста. При этом обращало на себя внимание, что среди пациентов 3–6 лет статистически значимо (р<0,001) преобладали дети с ассоциированной патологией.
Обсуждение
Ассоциация между СД1 и целиакией была впервые отмечена в конце 1960-х годов и описана в различных исследованиях [9]. Частота выявления глютеновой энтеропатии у пациентов с СД1 варьирует в пределах 1,1–16,6% [10–12], что превосходит ее среднюю распространенность в популяции. В ходе нашего исследования среди 1372 детей с СД1 удалось выявить 80 (5,8%) серопозитивных пациентов, у 48 (3,59%) из которых на основании комплексного обследования был установлен окончательный диагноз целиакии.
В основе ассоциации целиакии и СД1 лежат единые генетические маркеры, сходные средовые провоцирующие факторы и общие патогенетические механизмы [13]. Известно, что целиакия ассоциирована с присутствием в генотипе пациента генов главного комплекса гистосовместимости (HLA-DQ2 и HLA-DQ8) [14]. Аналогичные гаплотипы определяют риск развития иных аутоиммунных заболеваний, включая СД1 [15, 16]. Вероятность ассоциации увеличивает наличие у пациентов определенных не-HLA-генов, расположенных на хромосомах 5 (5q31-33), 2 (2q33), 19 (19p13), 4 (4q27). Из 39 типичных не-HLA-генов, определяемых у пациентов с целиакией, 64% могут быть выявлены еще хотя бы при одном аутоиммунном заболевании [17]. Крупное исследование, включавшее более 8 тыс. человек, продемонстрировало, что пациенты с СД и целиакией имеют в генотипе 26 однотипных не-HLA-генов [18], участвующих в регуляции продукции цитокинов (фактор некроза опухоли α, интерферон γ, интерлейкин (ИЛ) 2, ИЛ-21, ИЛ-10), активации естественных киллеров, Т- и В-лимфоцитов, а также в поддержании барьерной функции слизистой оболочки тонкой кишки.
Важную роль в ассоциации аутоиммунных заболеваний играют средовые факторы, в частности перенесенные инфекционные заболевания. В 2017 г. группа исследователей под руководством B. Jabri указала на взаимосвязь реовирусной инфекции и целиакии [19]. По мнению авторов, к вероятным механизмам ассоциации можно отнести изменения иммунологического баланса на уровне слизистой оболочки тонкой кишки вследствие вирусной инфекции с последующей потерей толерантности к глиадину. Аналогичные данные были продемонстрированы в 2011 г. W.C. Yeung et al. [20] в отношении роли энтеровирусной инфекции в реализации риска формирования СД1.
Отдельным механизмом коморбидности целиакии и аутоиммунных заболеваний является перекрестная реакция аутоантител и активированных Т-лимфоцитов с аутоантигенами организма. В частности, под действием tTG может происходить деамидирование пептидов в структуре различных органов и тканей, что ведет к образованию неоантигенов и провоцирует развитие реакций иммунного ответа за пределами кишечника. Образующиеся иммунные комплексы антител к tTG с самим ферментом могут быть выявлены как в слизистой оболочке тонкой кишки, так и в других органах и тканях, включая поджелудочную железу [21].
В основе скрининга на целиакию у пациентов с СД1 лежит определение в сыворотке крови концентрации tTG-IgA1 [13, 22]. При первичном обследовании, с целью исключения ложноотрицательных результатов серологического исследования у лиц с нарушениями гуморального иммунитета, рекомендовано исследование концентрации общего IgA в сыворотке [2]. При снижении уровня общего IgA рекомендуется определение содержания IgG к tTG в крови и/или определение содержания IgG к эндомизию в крови1 [2]. Ранее было отмечено, что tTG-IgA могут временно повышаться у пациентов с СД1, а затем нормализоваться, несмотря на нахождение на глютенсодержащей диете. Как предполагают некоторые исследователи [23, 24], выжидательная тактика у детей без симптомов и с умеренным повышением содержания tTG-IgA может быть оправданной, поскольку уровень tTG-IgA имеет тенденцию к уменьшению со временем. В исследовании S. Castellaneta et al. [25] было продемонстрировано спонтанное снижение tTG-IgA в 40% случаев на фоне глютенсодержащей диеты. Принимая во внимание аналогичные результаты исследований, протокол диагностики целиакии, утвержденный Европейским обществом гастроэнтерологов, гепатологов и нутрициологов (ESPGHAN) [2], определяет возможность наблюдения за пациентами с повышением концентрации tTG-IgA в пределах ≤3 норм с динамическим контролем серологических маркеров на глютенсодержащей диете. Данной категории пациентов эндоскопическое исследование может быть рекомендовано в случае сохранения серопозитивности или повышения концентрации tTG-IgA в динамике, а также при формировании клинических проявлений целиакии [26]. В качестве дополнительного серологического маркера при низкой концентрации tTG-IgA в крови может рассматриваться исследование уровня антител к эндомизию с целью исключения неоправданного проведения биопсии, однако следует отметить, что в реальной клинической практике определение содержания антител к эндомизию менее доступно, что ограничивает возможность использования данного диагностического подхода [27].
Полученные данные позволяют сделать вывод, что повышение концентрации tTG-IgA более 3 норм независимо от сроков дебюта СД1 определяет однозначную необходимость выполнения ФЭГДС с забором биоптатов слизистой двенадцатиперстной кишки с целью своевременной диагностики целиакии, несмотря на наличие или отсутствие характерных проявлений заболевания. В то же время незначительное повышение tTG-IgA определяет возможность динамического наблюдения у бессимптомных пациентов, особенно в случае выявления низкой серопозитивности в дебюте СД1. Наши результаты дополнительно демонстрируют трудности убеждения родителей и пациентов в необходимости выполнения ФЭГДС при отсутствии симптомов целиакии. Девять пациентов с повышением tTG-IgA более 3 норм остаются в группе наблюдения, продолжая контроль tTG-IgA в динамике. Нормализации концентрации tTG-IgA в данной группе пациентов не достигнуто.
По имеющимся данным, наиболее часто целиакия диагностируется после установления диагноза СД1 [8], при этом невозможно однозначно сказать, является ли это истинным дебютом целиакии после установления диагноза СД1 или это пропущенный ранее диагноз ввиду малосимптомного течения целиакии в данной группе пациентов. Выявленные нами высокая (3,5%) частота глютеновой энтеропатии у детей в дебюте СД1, а также статистически значимые различия в возрасте пациентов с изолированным СД1 и ассоциированной патологией свидетельствуют в пользу того, что мало- или бессимптомное течение целиакии, вероятно, предшествует СД1, являясь дополнительным провоцирующим фактором аутоиммунного повреждения β-клеток поджелудочной железы.
Заключение
Таким образом, среди пациентов со стажем СД1 более 3 мес. частота выявления целиакии явилась сравнимой с группой дебюта СД1 и составила 3,5%. Полученные результаты в совокупности с данными анализа выживаемости (Kaplan — Meier) свидетельствуют о сохранении высокой частоты выявления целиакии у пациентов в течение первых 5 лет после постановки диагноза СД1, что может определять необходимость ежегодного скрининга на целиакию после дебюта СД1 независимо от симптомов заболевания. Анализ возрастной структуры пациентов позволил выделить детей с дебютом СД1 в дошкольном возрасте в группу максимального риска по ассоциированной патологии, что требует наибольшего внимания к ним в рамках диспансерного наблюдения.
1Клинические рекомендации. Сахарный диабет 1 типа. 2025. (Электронный ресурс.) URL: https://edu.endocrincentr.ru/sites/default/files/recommendation_pdf/kr287_3.pdf (дата обращения: 13.11.2025).
Сведения об авторах:
Миянова Алия Ренатовна — врач-педиатр, врач-гастроэнтеролог, аспирант кафедры педиатрии имени академика Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0009-0006-3184-1701
Дмитриева Юлия Андреевна — к.м.н., заведующая Центром лечения целиакии, врач-гастроэнтеролог ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28; доцент кафедры педиатрии имени академика Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0003-0668-7336
Коломина Ирина Геннадьевна — заведующая эндокринологическим отделением ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28; ORCID iD 0009-0009-0473-1621
Стрункина Ирина Викторовна — врач-эндокринолог консультативно-диагностического отделения ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28.
Букин Сергей Сергеевич — врач-эндокринолог эндокринологического отделения ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28; ORCID iD 0000-0003-1775-8582
Захарова Ирина Николаевна — д.м.н., профессор, заведующая кафедрой педиатрии имени академика Г.Н. Сперанского ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0003-4200-4598
Османов Исмаил Магомедович — д.м.н., профессор, главный врач ГБУЗ «ДГКБ им. З.А. Башляевой ДЗМ»; 125373, Россия, г. Москва, ул. Героев Панфиловцев, д. 28; ORCID iD 0000-0003-3181-9601
Контактная информация: Миянова Алия Ренатовна, e-mail: miyanova@yandex.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 10.12.2025.
Поступила после рецензирования 13.01.2026.
Принята в печать 30.01.2026