Введение
Болезни накопления гликогена (БНГ, гликогенозы) — это группа наследственных заболеваний углеводного обмена, обусловленных недостаточностью ферментов — участников метаболизма гликогена и характеризующихся избыточным накоплением гликогена в таргетных органах и тканях. К самым распространенным типам с поражением печени относятся типы I, III, VI и IX [1]. Частота встречаемости БНГ составляет приблизительно 1 случай на 20–43 тыс. живых новорожденных [2]. Характерной особенностью всех печеночных БНГ является развитие гипогликемии [2]. Наиболее тяжелой формой болезни считается БНГ I типа, которая связана с недостаточностью глюкозо-6-фосфатазы, вследствие чего блокируются пути как глюконеогенеза, так и гликолиза [1–3]. Это запускает каскад дальнейших нарушений обмена и приводит к формированию тяжелой гипогликемии, хроническому кетозу и лактатацидозу, дислипидемии, гиперурикемии, гепатомегалии со стеатозом, задержке физического развития. При других типах БНГ происходит нарушение синтеза ферментов, задействованных только в процессе распада гликогена, что смягчает их клиническую картину и выраженность метаболических нарушений. Избыточное накопление гликогена в клетках в свою очередь приводит к нарушению функций соответствующих тканей и органов. Для всех печеночных типов характерно откладывание гликогена в гепатоцитах, для БНГ I типа также в клетках почек и слизистой оболочке кишечника, для БНГ III типа — в миоцитах скелетной и сердечной мускулатуры.
Все формирующиеся нарушения углеводного обмена также могут влиять на метаболизм костной ткани: приводить к снижению минеральной плотности кости (МПК), развитию остеопороза (ОП) и повышению рисков возникновения переломов. Патогенез формирования данных нарушений до конца не изучен. Предполагается, что причинами могут быть: дефицит микронутриентов, недостаточный метаболический контроль заболевания (гипогликемия, хронический кетоз, гиперлипидемия), компенсация метаболических нарушений за счет костной ткани (избыточное использование депо кальция и фосфатов), дисфункция печени, повреждение мышц и гипогонадизм [4–7]. Помимо рисков, связанных с заболеванием, свою роль могут играть также внешние факторы риска развития ОП: алиментарная недостаточность макро- и микронутриентов (отсутствие в рационе или недостаточное употребление молочных продуктов, мяса, рыбы, яиц и др.), недостаточность инсоляции, невысокая физическая активность, вредные привычки (курение, избыточное употребление алкоголя) [8]. Согласно официальной позиции Международного общества клинической денситометрии (ISCD — the International Society for Clinical Densitometry) диагностика ОП у детей осуществляется на основании ряда критериев: наличие минимум одного низкоэнергетического компрессионного перелома позвонка или сочетание низкой Z-score МПК с определенным количеством переломов длинных трубчатых костей (два и более перелома до 10 лет, три и более — до 19 лет). Диагностических критериев для определения остеопении не представлено1.
Стандартным методом исследования МПК у детей является двухэнергетическая рентгеновская абсорбциометрия (ДРА), проведенная в области поясничного отдела позвоночника или комплексно всего тела (без учета головы) с нормализацией по Z-score1. У детей с низким ростом или задержкой физического развития ISCD рекомендовано проводить коррекцию Z-score МПК с помощью BMAD (bone mineral apparent density — «кажущаяся» МПК) или Z-score роста1. BMAD — это показатель, используемый для преобразования исследуемой площади в объем для каждого отдельного позвонка с целью приблизительного учета влияния толщины кости и размера тела [9]. Нормативные базы для оценки BMAD и Z-score BMAD в настоящее время находятся в стадии разработки, в свободном доступе опубликованы данные для аппаратов Lunar Medical (Великобритания) и Hologic (США) [9, 10].
Количество исследований по изучению особенностей МПК у детей с БНГ небольшое, и основная доля приходится на пациентов с БНГ I типа. Тем не менее в литературе представлены данные о снижении средних значений МПК у пациентов с БНГ I и III типов в сравнении с контрольной группой условно здоровых детей [6, 11]. Диапазон встречаемости низкой МПК относительно хронологического возраста широкий и составляет от 13 до 60% [5, 12, 13]. Распространенность переломов у пациентов с БНГ I типа, по разным данным, составляет от 25 до 35% в возрасте до 30 лет [12, 13].
Цель исследования: оценить взаимосвязь показателей МПК с результатами клинических, лабораторных и инструментальных обследований у детей с печеночными типами БНГ.
Материал и методы
В исследование включено 72 пациента в возрасте от 4 до 17 лет с БНГ с преимущественным поражением печени, наблюдавшихся в Клинике лечебного питания ФГБУН «ФИЦ питания и биотехнологии» с 2018 по 2024 г. Нозологическая структура заболеваний представлена БНГ следующих типов: I а и I b тип — 15 человек (21%, 12 девочек и 3 мальчика), III тип — 19 человек (26%, 12 девочек и 7 мальчиков), VI тип — 10 человек (14%, 3 девочки и 7 мальчиков), IX тип — 28 (39%) мальчиков. Критериями включения в исследование были: молекулярно-генетически подтвержденный диагноз БНГ с определением типа БНГ, возраст пациентов от 4 лет и рост от 100 см, подписанное информированное согласие пациентов и их законных представителей на участие в исследовании.
Информация о переломах и их характере получена анамнестически и из медицинской документации. Антропометрические показатели исследовали у всех пациентов в день госпитализации по стандартным методикам, стандартные отклонения от нормальных значений для конкретного возраста и пола оценивали согласно критериям ВОЗ. Лабораторные исследования включали в себя определение параметров, отражающих состояние печени (аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), γ-глутамилтранспептидаза (гГТП), щелочная фосфатаза (ЩФ), общий белок и его фракции), метаболический контроль течения основного заболевания (показатели кислотно-щелочного состояния (КЩС), глюкозы натощак и липидного профиля (общий холестерин (ХС), ХС липопротеинов высокой плотности (ХС ЛПВП), ХС липопротеинов низкой плотности (ХС ЛПНП), триглицериды), минерального обмена и витаминного статуса. Уровень витамина D в крови оценивали по концентрации 25-гидроксивитамина D3 в сыворотке (25(OH)D3, норма 30–100 нг/мл).
Двухэнергетическая рентгеновская абсорбциометрия проведена в области поясничных позвонков (L1–L4) на денситометре STRATOS (DMS, Франция). Коррекция на пол и возраст — согласно Z-score на основании базы данных используемого денситометра. Показатели Z-score МПК ≤-2,0 расценивали как низкую МПК относительно хронологического возраста, Z-score МПК >-2,0 — как нормальную. Критерии диагностики ОП применены согласно официальной позиции ISCD. Уровень BMAD рассчитывали по формуле: BMC / (V1 + V2 + V3 + V4), где BMC (bone mineral content) — содержание минеральных веществ в костях, Vn — площадь конкретного позвонка в степени 1,5 [9]. Неинвазивную транзиентную эластографию печени (ТЭП) выполняли на аппарате Echosens FibroScan 502 Touch (Франция). Степень фиброза оценивали по шкале METAVIR (F0–F4) согласно значениям медианы эластичности (кПа), а степень стеатоза (S0–S3) — на основании базы данных аппарата согласно значениям контролируемого параметра затухания (САР, Controlled Attenuation Parameter, дБ/м), минимальное количество измерений — 12. Доступность оценки САР используемого аппарата ограничена размерами датчика, в связи с чем данный параметр определен только у 60 пациентов.
Программа исследования одобрена комитетом по этике ФГБУН «ФИЦ питания и биотехнологии». Исследование проведено с соблюдением этических норм в соответствии с Хельсинкской декларацией.
Статистическая обработка результатов проведена с помощью программ IBM SPSS Statistics v.23 и Microsoft Office Excel 2013. Проверку выборок на нормальность распределения проводили с помощью критерия Колмогорова — Смирнова и критерия Шапиро — Уилка. В случае, если полученные данные подчинялись законам нормального распределения, их представляли как среднее и стандартное отклонение (M±SD), с целью сравнения выборок применяли однофакторный дисперсионный анализ (ANOVA) и апостериорный критерий Тьюки, уровень статистической значимости — p<0,05. Если распределение отличалось от нормального, данные представляли как Me [Q1; Q3], для сравнения применяли метод Краскела — Уоллиса, а для множественного сравнения — метод Манна — Уитни с учетом поправки Бонферрони (р≤0,008). В случае положительной аппроксимации на нормальность использовали частотный дисперсионный анализ, при невозможности — тест Фишера. Корреляционный анализ осуществляли с помощью коэффициентов Пирсона (rp) и Спирмена (rs), для оценки силы связи коэффициентов корреляции использовали шкалу Чеддока. Для учета перекрестного коррелирования применен метод множественной линейной регрессии.
Результаты исследования
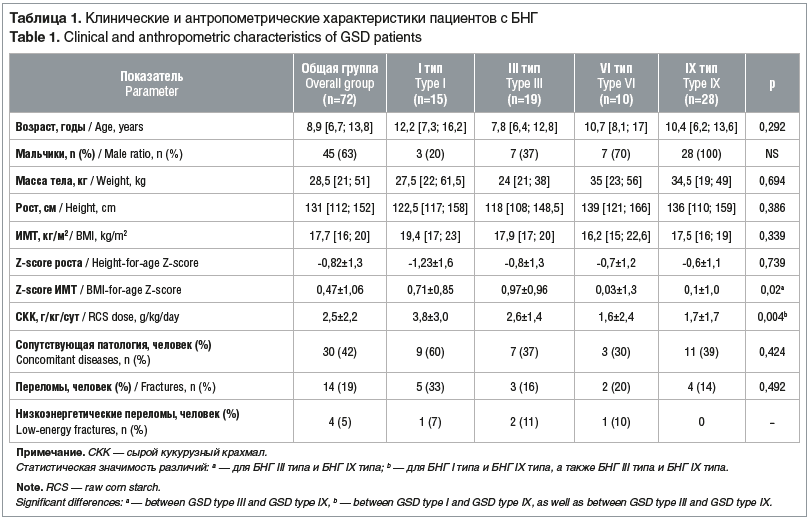
В исследование включено 72 пациента с БНГ в возрасте от 4 до 17 лет (Ме 8,9 [6,7; 13,8] года). Доля мальчиков составила 63% (n=45). Подробная характеристика групп обследуемых детей представлена в таблице 1. Группы были сопоставимы по основным показателям: возрастные и антропометрические различия между типами БНГ практически отсутствовали, за исключением пациентов с БНГ III типа, у которых тенденция к избыточной массе тела была более выражена, чем у пациентов с БНГ IX типа (р=0,02). В общей выборке недостаточность питания умеренной степени отмечалась у 3% (n=2) детей, у 26% (n=19) была избыточная масса тела и еще у 6% (n=4) — ожирение 1-й и 2-й степени. Выраженная задержка роста зарегистрирована у двоих пациентов (Z-score рост/возраст — 5,88 и -3,18), задержка роста — у 8% (n=6). Физическое развитие ниже среднего наблюдалось практически у 40% (n=27) обследуемых, выше среднего — у 7% (n=5). Высокого физического развития и высокорослости не зафиксировано ни в одном случае. Между девочками и мальчиками различий в показателях возраста и антропометрии не отмечено.

На протяжении всей госпитализации пациенты придерживались индивидуальной диеты, назначенной в соответствии с рекомендациями по ведению детей с БНГ и с учетом отягощенности аллергического анамнеза. Дополнительно практически все пациенты (95%) употребляли СКК в среднесуточной дозировке 2,37±2,2 г/кг массы тела. Среди девочек среднесуточная доза СКК была достоверно выше (3,3±2,5 г/кг и 2,1±1,9 г/кг, р=0,015). Обогащение рациона лечебными смесями осуществлялось у 11% (n=8) пациентов, коррекция метаболических нарушений — у 33% (n=24), гепатопротективная терапия — у 40% (n=29). Четырем пациентам из группы БНГ I типа во время госпитализации в связи с наличием нейтропении был введен стимулятор лейкопоэза — филграстим.
Среди сопутствующей патологии встречались некоторые заболевания, которые могут быть ассоциированы с развитием вторичного ОП. У 20% (n=14) детей подтверждены аллергические заболевания в стадии обострения или неполной ремиссии (бронхиальная астма, поллиноз, гастроинтестинальная форма пищевой аллергии, атопический дерматит), в 7% (n=5) случаев отмечался гипотиреоз с необходимостью назначения левотироксина, в 1,5% (n=1) — гипогонадизм (медикаментозно скомпенсированный) и гипопаратиреоз. Также у 3% (n=2) детей имели место хронические воспалительные заболевания верхних отделов желудочно-кишечного тракта (гастродуодениты, эзофагиты) и сопутствующая длительная терапия ингибиторами протонной помпы и антацидами, у 1 ребенка — хронический тубулоинтерстициальный нефрит в стадии частичной клинико-лабораторной ремиссии, и еще у одного — ювенильный артрит. У 7,5% (n=2) девочек диагностирована дисфункция яичников.
У 19% (n=14) детей к моменту включения в исследование имелись переломы костей конечностей, переломов позвонков не зафиксировано. У большинства (71,5%, n=10) детей отмечался один перелом, у 21,5% (n=3) — 2 перелома и у 7% (n=1) — 3. Все случаи переломов отмечались в возрасте до 12 лет, медиана возраста составила 5 [3; 6] лет. Медиана возраста возникновения первого перелома — 4 [2,3; 6,0] года. Около трети обстоятельств всех переломов носили характер низкоэнергетической травмы и встречались у 5% (n=4) пациентов, причем у одного из них такие переломы случились дважды. У девочек наличие хотя бы одного перелома отмечалось чаще, чем у мальчиков (33% против 11%, р=0,039). Разница медиан возрастов детей с переломами (13,2 [8,3; 14,8] года) и без переломов (8,5 [6,4; 13,4] года) составила 4,7 года.
Показатели ДРА достоверных отличий по типам БНГ не имели, средние значения Z-score МПК как в общей выборке, так и по типам БНГ лежали в пределах нормальных значений в соответствии с возрастом (табл. 2). У девочек отмечались более высокие значения BMAD по сравнению с мальчиками (0,2 [0,18; 0,25] и 0,19 [0,17; 0,21] г/см3 соответственно, р=0,05) при сопоставимости возрастных и антропометрических показателей, а также Z-score МПК. Снижение МПК относительно хронологического возраста встречалось у 4% (n=3) детей. Критериям диагностики ОП ISCD не соответствовал ни один случай: не зафиксировано ни одного перелома позвонка (анамнестически), а у 3 детей со сниженной МПК количество переломов в соответствии с возрастом не достигло диагностически значимого (у двоих было по одному перелому, а у одного переломов не было).

Умеренная положительная корреляционная связь с высоким уровнем значимости отмечалась между показателями Z-score МПК и Z-score роста (rp=0,461, p<0,001) и слабая взаимосвязь — между Z-score МПК и Z-score ИМТ (rp=0,281, p=0,017). При построении множественной линейной регрессии выявлена умеренная отрицательная связь Z-score МПК с возрастом (β=-0,331, р=0,002) вне зависимости от связи Z-score МПК и Z-score роста (β=0,542, р<0,001). В то же время Z-score роста при контроле Z-score МПК был положительно связан с возрастом (β=0,314, р=0,004). Ассоциаций Z-score МПК с полом, средней дозировкой СКК, наличием переломов и сопутствующей патологией не выявлено.
Наиболее четко тенденция к снижению Z-score МПК по возрасту обнаруживается при учете всех измерений Z-score МПК за 6 лет наблюдения обследуемых пациентов. У 50 из 72 человек ДРА проводили неоднократно с разными временными интервалами. Таким образом, все имеющиеся измерения Z-score МПК разделены по возрастным группам с шагом в 4 года: 1-я группа — проведение ДРА детям от 4 до 7 лет (39 измерений); 2-я группа — от 8 до 11 лет (31 измерение); 3-я группа — от 12 до 15 лет (25 измерений); 4-я группа — от 16 до 19 лет (18 измерений). В случае, если у одного пациента было два и более измерений, проведенных в период, входящий в одну возрастную группу, показатели Z-score МПК усредняли. При сравнении возрастных групп выявлено, что уровни Z-score МПК в 1-й возрастной группе были статистически значимо выше, чем Z-score МПК в 4-й возрастной группе (0,33±1,27 против -0,9±1,34, р=0,003) (рис. 1).

Метаболический контроль течения БНГ подразумевал под собой контроль показателей КЩС, глюкозы натощак и липидного профиля (табл. 3). Средние показатели КЩС находились в пределах нормальных значений (рН крови 7,35 [7,32; 7,37], НСО3 24,7±2,7 ммоль/л и ВЕ (base excess, показатель избытка или дефицита оснований) -1,3±2,5 ммоль/л), однако стандартные отклонения достаточно большие, что отражает широкую вариативность данных параметров. Уровень лактата у пациентов с БНГ был повышен и равен 1,8 [1,2; 3,0] ммоль/л, лактат в группе пациентов с БНГ I типа был статистически значимо выше, чем у пациентов с другими типами БНГ. У 43% (n=31) пациентов фигурировал диагноз дислипидемии, подразумевающий под собой изменения уровней показателей липидного профиля. Медианы уровней ХС, ХС ЛПВП и триглицеридов лежали в пределах референтных значений. Уровень триглицеридов у детей с БНГ I и III типов был достоверно выше, чем у детей с БНГ IХ типа (р<0,001), а уровень ХС ЛПВП у пациентов с БНГ III типа ниже, чем у пациентов с БНГ VI и IХ типов (р=0,004).

При проведении простого корреляционного анализа Z-score МПК был ассоциирован с показателями КЩС (рН rp=0,26 и лактат rp=-0,25, р<0,05, BE rs=0,39 и HCO3 rs=0,33, p<0,01), уровнем глюкозы натощак (rp=0,352, p=0,002) и триглицеридов (rp=-0,237, p=0,045). Однако при коррекции на возраст и Z-score роста значимые взаимосвязи сохранил уровень ВЕ (β=0,266, р=0,02), обнаружилась положительная ассоциация Z-score МПК с уровнем ХС ЛПВП (β=0,221, р=0,034), а уровень глюкозы натощак показал тенденцию к статистически значимому влиянию (β=0,183, р=0,088).
Состояние печени оценивали по некоторым основным параметрам биохимического анализа крови (наличие синдромов цитолиза, холестаза, печеночно-клеточной недостаточности) и данным ТЭП (табл. 4). У 43% обследованных отмечался синдром цитолиза, из них у большинства (80%) цитолиз был умеренный и не превышал 5 норм, еще у 16% (n=5) — выраженный цитолиз (от 5 до 10 норм) и только у одного пациента — высокий цитолиз (более 10 норм). Основная доля пациентов с повышением концентрации трансаминаз в крови приходилась на детей с БНГ III типа, медианы АЛТ и АСТ этой группы значимо отличались от показателей других типов БНГ (р<0,001). Синдром холестаза в общей выборке отмечен не более чем в 10% случаев. Уровень общего белка в крови среди пациентов с БНГ I типа был значимо выше относительно других типов. При этом уровень альбумина не отличался по группам, а уровень глобулинов у пациентов с БНГ I типа был достоверно выше, чем у пациентов с БНГ IХ типа (р=0,006).

Медиана эластичности печени в общей группе составила 4,4 [3,0; 5,9] кПа, что лежит в пределах F0–F1 по METAVIR. У 31% детей при ТЭП выявлен фиброз (F) печени, из них большая часть имела степень F1 (68%, n=15), около 20% — степень F2, у 5% (n=1) — степень F3 и еще у 9% (n=2) — степень F4 (у одного из них выявлены признаки цирроза при УЗИ печени, у второго признаков цирроза не было, но отмечался выраженный цитолиз до 9 норм). Среди 60 пациентов с наличием показателей САР у 35% (n=21) выявлен стеатоз (S): S1 — у 20% (n=12) человек, S2 — у 3% (n=2), S3 — у 12% (n=7).
Показатели Z-score МПК с учетом возраста и Z-score роста с высокой значимостью отрицательно коррелировали с уровнем АЛТ (β=-0,224, р=0,031) и АСТ (β=-0,229, р=0,028), а также с уровнем ЩФ (β=-0,312, р=0,009). Ни один из параметров ТЭП не достиг статистически значимой взаимосвязи с Z-score МПК, за исключением крайне слабой отрицательной связи между Z-score МПК и наличием фиброза печени (rs=-0,236, p=0,049). Тем не менее если разделить общую группу детей с БНГ на детей с фиброзом печени (n=22, медиана эластичности 6,4 [6,0; 7,9] кПа) и без фиброза печени (n=48, медиана эластичности 3,7 [2,8; 4,5] кПа), то в первой группе уровни Z-score МПК будут достоверно ниже (-0,56±1,35 в сравнении с 0,03±1,22, р=0,049), а доля переломов — выше (36% в сравнении с 12,5%, р=0,02). При этом группы не отличаются по возрасту, полу, антропометрическим показателям и долевой составляющей сопутствующей патологии.
Помимо основных показателей контроля течения БНГ были исследованы параметры кальциево-фосфорного обмена и витаминный статус (табл. 5). Средние уровни кальция общего, ионизированного кальция, фосфора и паратиреоидного гормона (ПТГ) находились в пределах референтных значений. Статистически значимых корреляций показателей кальциево-фосфорного обмена с Z-score МПК не выявлено.

Уровень 25(OH)D3 в крови более чем у половины (61%) детей с БНГ был ниже адекватных значений, а медиана его концентрации в общей группе (n=72) составила 27 [20; 39] нг/мл. Зависимости уровня витамина D от времени года выполнения анализа не отмечено. У одного ребенка выявлен выраженный дефицит витамина D, у 22% (n=15) детей — дефицит витамина D и еще у 38% (n=26) — его недостаточность. Уровень 25(OH)D3 от 50 до 100 нг/мл зафиксирован у 7% (n=5) пациентов. Распределение уровней 25(OH)D3 в крови по типам БНГ отражено на рисунке 2. Взаимосвязи между показателями 25(OH)D3 в крови и Z-score МПК не отмечалось.

Обсуждение
В нашем исследовании изучены особенности МПК у 72 детей с БНГ, протекающими с преимущественным поражением печени. Проведено обследование пациентов как с тяжелыми типами БНГ (I и III типы), так и с более легкими (VI и IX типы). Группы сравнения по типам БНГ различались по половому признаку: большую долю детей с БНГ I типа составляли девочки, а БНГ IX типа встречалась только среди мальчиков. Это связано с Х-сцепленным характером наследования БНГ IXа типа. Несмотря на это, сравниваемые типы БНГ практически не отличались по возрастным и антропометрическим показателям, за исключением большей предрасположенности к избыточной массе тела детей с БНГ III типа по сравнению с мальчиками с БНГ IX типа (р=0,02). Разница в течении БНГ по типам исследовалась исключительно в контексте МПК и поиска возможных взаимосвязей с ее изменениями. Однако ни один из параметров ДРА (МПК, BMC, Z-score МПК, BMAD) не имел достоверных отличий между типами БНГ. Исключение малочисленной группы (дети с VI типом БНГ) из сравнительного анализа между типами БНГ не выявило различий в результатах, полученных при анализе четырех нозологических групп, поэтому было решено сохранить ее как отдельную группу в рамках данной работы.
Средние показатели Z-score МПК общей группы и внутри типов БНГ лежали в пределах референтных значений (Z-score МПК общей группы -0,13±1,3). Схожие результаты получили J.T. Jacoby et al. [5], однако в их выборке отмечались более высокие значения ИМТ. В исследованиях D. Melis [6, 11] средние значения Z-score МПК были ниже -1, а в исследовании S. Vai [13] — менее -2, что очевидно ниже полученных нами. Однако стоит отметить, что в данных работах ДРА выполнена на других анализаторах (Lunar Medical, Hologic). Снижение МПК относительно хронологического возраста в нашей выборке регистрировали достаточно редко, у 4% (n=3) обследованных, среди них 13% (n=2) пациентов с БНГ I типа и 3,5% (n=1) — с БНГ IХ типа. Наиболее близкие результаты получены J.T. Jacoby [5] — 13% (n=3), из них двое с БНГ III типа и один с БНГ I типа. В исследованиях N. Kaiser [12] и S. Vai [13] доля пациентов с БНГ I типа была значительно выше — 47 и 60% соответственно.
Таким образом, в связи с отсутствием влияния типа БНГ на параметры ДРА, внутри общей выборки детей с БНГ оценивали потенциальные взаимосвязи показателей Z-score МПК с результатами клинических, лабораторных и инструментальных обследований. Поскольку показатель Z-score МПК является стандартизованным по полу, возрасту и расе, он взят за основной параметр состоятельности плотности кости. Отсутствие программного обеспечения и научных баз данных для используемого денситометра не позволило нам провести коррекцию Z-score МПК по росту и рассчитать Z-score BMAD. Результаты BMAD представлены для теоретических и научных целей дальнейших исследований в данной области. Несмотря на это, для уменьшения искажения результатов наблюдений мы осуществляли поиск взаимосвязей между исследуемыми параметрами и Z-score МПК с учетом влияния Z-score роста с помощью модели множественной линейной регрессии.
В общей группе детей с БНГ прослеживалась положительная ассоциация Z-score МПК и Z-score роста с высокой значимостью (rp=0,461, p<0,001). Данная связь сохранялась вне зависимости от других предикторов множественной линейной регрессии, что говорит о ее устойчивости и невозможности оценки Z-score МПК без учета влияния Z-score роста. Учитывая данные особенности, нами выявлена отрицательная взаимосвязь показателей Z-score МПК и возраста (р=0,002), которая не прослеживалась при проведении простого корреляционного анализа. Более отчетливо тенденция к снижению Z-score МПК с возрастом определялась при учете многолетних наблюдений показателей ДРА у детей с БНГ. Достоверно средние значения Z-score МПК в возрастной группе измерений, проведенных у детей от 16 до 19 лет, были ниже, чем значения Z-score МПК в группе измерений, проведенных у детей в возрасте от 4 до 7 лет включительно (-0,9±1,34 в сравнении с 0,33±1,27, р=0,003). По мере увеличения возрастной группы отчетливо видно постепенное снижение медианы и квартилей Z-score МПК.
Теоретически данная ассоциация может быть связана с длительностью воздействия на костную ткань патологических факторов, формирующихся из-за течения хронического заболевания. Также не исключена роль большей физической активности, лучшей комплаентности при лечении основного заболевания и дотации всех необходимых макро- и микронутриентов среди пациентов младшей группы с учетом большего контроля со стороны родителей. Мы не изучали эти параметры у пациентов, поскольку большинство из них анализировались ретроспективно на основании данных истории болезни. В литературе встречается информация, косвенно подтверждающая такие предположения. Так, например, D. Melis et al. [11] в своем исследовании выявили значительное снижение Z-score МПК у пациентов с БНГ Ia типа с плохой комплаентностью по сравнению с пациентами с хорошей комплаентностью (Z-score МПК -1,7 и -0,3 соответственно, p=0,006). В исследовании S. Vai et al. [13] схожая картина наблюдалась при учете встречаемости переломов среди пациентов с БНГ I типа. Tак, дети в группе с наличием переломов были достоверно старше, чем в группе без переломов (14,1±3,4 и 10,1±4,4 года, р=0,049), что может свидетельствовать о повышении хрупкости костей и увеличении тяжести метаболических нарушений с возрастом.
В нашем исследовании встречаемость хотя бы одного перелома составила 19% среди всех пациентов с БНГ, а переломов вследствие низкоэнергетической травмы — 5%. Преимущественно переломы встречались у девочек (р=0,039), достоверных различий между типами БНГ не выявлено. Схожие данные в своем исследовании получили N. Kaiser et al. [12] — частота встречаемости переломов в их выборке пациентов с БНГ I типа в возрасте от 14 до 29 лет составила 25%, и 4% классифицированы как обусловленные ОП. У пациентов старшей возрастной группы (10,5–54,0 года) в исследовании L.A. Minarich [14] доля низкоэнергетических переломов составила 11%. В то же время S. Vai et al. [13] описывают 35% встречаемость низкоэнергетических переломов у пациентов с БНГ I типа в возрасте от 3 до 20 лет.
Считается, что снижение МПК у детей с БНГ может быть следствием метаболических нарушений и реакций их компенсации. Отрицательная взаимосвязь Z-score МПК с уровнем лактата подтверждается в некоторых исследованиях среди пациентов с БНГ Ia типа, причем значимость и сила данных ассоциаций достаточно высокие (r>0,7, p≤0,03) [11, 12]. В нашем исследовании среди всех пациентов с БНГ с учетом предиктора Z-score роста и возраста данной связи не обнаружено. Однако выявлена положительная ассоциация с уровнем ВЕ (р=0,02) и тенденция к статистически значимому влиянию с уровнем глюкозы натощак (р=0,088).
Данные о наличии взаимосвязи МПК с уровнем триглицеридов противоречивы. В части исследований связь не обнаруживается в выборках среди пациентов c БНГ I типа [11, 12], другая часть исследований подтверждает отрицательный характер ассоциации у пациентов с БНГ Iа и III типов [6, 14]. В нашем случае данная ассоциация теряла статистическую значимость с учетом предикторов Z-score роста и возраста. Однако на этом фоне нами выявлена положительная взаимосвязь Z-score МПК с уровнем ХС ЛПВП (р=0,034). Схожих данных среди пациентов с БНГ в литературе нет, однако в последние годы публикуются наблюдения о связи ХС ЛПВП с МПК среди здорового населения. Так, например, R. Xie et al. [15] в исследовании населения США от 20 до 59 лет (n=10 635) установили, что более высокий уровень ХС ЛПВП связан с более высокой МПК в поясничном отделе позвоночника у большинства людей. В то же время G.X. Wang et al. [16] выявили отрицательную корреляцию между уровнем ХС ЛПВП и МПК у подростков мужского пола в возрасте от 12 до 19 лет и отсутствие взаимосвязи у девочек того же возраста (n=3770).
Остеопороз достаточно часто возникает у пациентов с хроническими заболеваниями печени, однако патогенез его формирования до конца не ясен [17]. К основным факторам, задействованным в нарушении костного метаболизма при дисфункции печени, могут относиться: нарушение синтеза инсулиноподобного фактора роста 1 (ИФР-1), стероидных гормонов, витамина D, хроническое воспаление, повышение синтеза склеростина и мальабсорбция витамина К, формирующиеся при хроническом холестазе, изменение продукции фибронектина [17, 18]. В наши цели не входило уточнение механизмов формирования ОП, мы оценивали наличие взаимосвязи с лабораторными и инструментальными проявлениями патологии печени. Таким образом, при контроле возраста и Z-score роста показатели Z-score МПК отрицательно коррелировали с уровнями ЩФ (р=0,009), АЛТ (р=0,031) и АСТ (р=0,028). То есть у пациентов с более выраженным цитолизом отмечался более низкий уровень Z-score МПК. В исследовании D. Melis [6] среди пациентов с БНГ III типа уровни АЛТ и АСТ достаточно сильно отрицательно коррелировали с уровнем ИФР-1 (r=-0,64 и -0,74, р<0,05), что теоретически может объяснять пути воздействия цитолиза на процесс костного ремоделирования. Связь Z-score МПК с ЩФ неоднозначна, поскольку мы исследовали общую концентрацию ЩФ, а не уровень ее изоформ (костной или печеночной). В случае, если в крови преобладает костная изоформа ЩФ, то повышение уровня общей ЩФ, вероятно, обусловлено снижением Z-score МПК с целью повышения минерализации кости. Однако в случае повышения содержания печеночной изоформы ЩФ Z-score МПК может быть снижен в связи с наличием холестаза. В то же время связи Z-score МПК и гГТП, другим показателем холестаза, в нашем исследовании не выявлено.
Также в нашей выборке прослеживается негативное влияние развития фиброза печени на состоятельность костной ткани. Так, уровень Z-score МПК в группе детей с БНГ с фиброзом печени был достоверно ниже, чем у детей без фиброза (-0,56±1,35 в сравнении с 0,03±1,22, р=0,049), а доля переломов — выше (36% в сравнении с 12,5%, р=0,02). Других исследований, изучающих данные взаимосвязи, среди пациентов с БНГ нами не обнаружено. В Китае проведена работа среди пациентов с фиброзом печени различной этиологии (F0–F4 по METAVIR) в возрасте от 28 до 87 лет, где выявлена отрицательная корреляция между МПК и степенью фиброза от F2 до F4 [19]. В то же время есть ряд наблюдений среди взрослых пациентов с метаболически ассоциированной жировой болезнью печени, где данная связь не подтверждается [20, 21].
Снижение уровня витамина D довольно широко распространено у пациентов с БНГ и составляет, по разным данным, примерно от 62 до 78% [3, 22]. В нашем исследовании доля таких пациентов составила 61%. Взаимосвязи между показателями 25(OH)D3 в крови и Z-score МПК не отмечалось, так же как и в наблюдениях J.T. Jacoby, D. Melis и N. Kaiser [5, 11, 12].
Следует отметить, что, учитывая все показатели, обнаружившие связь с Z-score МПК, наибольшую предрасположенность к снижению МПК имеют пациенты с БНГ III типа. Так, среди них отмечались значительно более высокие значения АЛТ и АСТ в сопоставлении со всеми типами БНГ (р<0,001), более низкие значения глюкозы натощак (p=0,004) и ХС ЛПВП (p=0,008) в сравнении с IX типом БНГ и наибольшая распространенность фиброза печени в сравнении с VI типом БНГ (p=0,004).
Заключение
Наше исследование показало, что некоторые клинические, лабораторные и инструментальные параметры течения БНГ могут быть связаны с состоятельностью костной ткани. Старший возраст детей, снижение Z-score роста, показателей ВЕ, ХС ЛПВП, глюкозы натощак, выраженность цитолиза и наличие фиброза печени могут быть факторами риска снижения МПК у пациентов с печеночными типами БНГ. Пациенты женского пола и пациенты с фиброзом печени более предрасположены к переломам.
Полученные результаты говорят о многофакторности проблемы костного здоровья у пациентов с БНГ и необходимости проведения более масштабных исследований в данной области. Исследование перечисленных показателей целесообразно включать в перечень сопутствующих обследований при проведении ДРА, в том числе в динамике, с целью оценки их как диагностически, прогностически и профилактически значимых.
1ISCD, June 2019. Supersedes all prior “Official Positions” publications. Approved and Accepted by the ISCD Board on May 28, 2019. (Electronic resource.) URL: https://iscd.org/wp-content/uploads/2021/09/2019-Official-Positions-Pediatric-1.pdf (access date: 20.12.2024).
Сведения об авторах:
Рахманина Ксения Юрьевна — аспирант отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; ORCID iD 0000-0003-3741-1877
Тин Ирина Феликсовна — к.м.н., врач — детский эндокринолог отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; ORCID iD 0000-0001-7663-4382
Павловская Елена Вячеславовна — д.м.н., ведущий научный сотрудник отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; профессор кафедры диетологии и нутрициологии ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; ORCID iD 0000-0002-4505-397X
Таран Наталия Николаевна — к.м.н., старший научный сотрудник отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; ассистент кафедры гастроэнтерологии и диетологии ФДПО ФГАОУ ВО РНИМУ им. Н.И. Пирогова
Минздрава России (Пироговский Университет); 117513, Россия, г. Москва, ул. Островитянова, д. 1, стр. 6; ORCID iD 0000-0001-9557-387X
Багаева Мадлена Энверовна — к.м.н., старший научный сотрудник отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; доцент кафедры гастроэнтерологии и диетологии ФДПО ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (Пироговский Университет); 117513, Россия, г. Москва, ул. Островитянова, д. 1, стр. 6; ORCID iD 0000-0002-1752-6901
Абдулманапова Маржанат Асилдеровна — аспирант отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; ORCID iD 0000-0002-0133-2715
Зубович Андрей Игоревич — к.м.н., научный сотрудник отделения педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; ORCID iD 0000-0002-2966-5618
Строкова Татьяна Викторовна — д.м.н., профессор РАН, заведующая отделением педиатрической гастроэнтерологии, гепатологии и диетотерапии ФГБУН «ФИЦ питания и биотехнологии»; 109240, Россия, г. Москва, Устьинский пр-д, д. 2/14; заведующая кафедрой гастроэнтерологии и диетологии ФДПО ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (Пироговский Университет); 117513, Россия, г. Москва, ул. Островитянова, д. 1, стр. 6; ORCID iD 0000-0002-0762-0873
Контактная информация: Рахманина Ксения Юрьевна, e-mail: ks.2394@mail.ru
Источник финансирования: работа проводилась в рамках выполнения темы государственного задания ФГБУН «ФИЦ питания и биотехнологии» № FGMF-2023-0008 «Разработка медицинских технологий диагностики и коррекции недостаточности питания у больных неинфекционными заболеваниями».
Конфликт интересов отсутствует.
Статья поступила 21.01.2026.
Поступила после рецензирования 28.01.2026.
Принята в печать 30.01.2026.