Введение
Деструктивная (некротизирующая) пневмония представляет собой жизнеугрожающее осложнение внебольничной пневмонии (ВП) у детей, характеризующееся формированием множественных очагов некроза легочной паренхимы, которые могут прогрессировать до абсцесса или гангрены [1]. Несмотря на относительную редкость (около 1–5% госпитализированных по поводу ВП), данная патология отличается тяжелым, часто молниеносным течением, высоким риском необратимых изменений и летального исхода, что определяет ее как значимую медико-социальную проблему [2, 3].
В России, как и во всем мире, отмечается тенденция к увеличению частоты регистрации деструктивных форм ВП, преимущественно у детей дошкольного возраста [4]. Этиологическая структура остается связанной с бактериальными патогенами, где ведущая роль принадлежит Streptococcus pneumoniae (60–80% случаев), в особенности его высоковирулентным серотипам, таким как серотип 3, который ассоциирован с наиболее тяжелыми и инвазивными формами инфекции даже у вакцинированных детей [5].
Ключевым звеном патогенеза деструкции является нарушение перфузии в очаге воспаления, обусловленное иммунотромбозом легочных сосудов. Возможная полная ишемия ткани с последующим некрозом объясняет первоначальную неэффективность антибактериальной терапии [6, 7]. В отечественной и зарубежной литературе до сих пор недостаточно сведений о ведении таких пациентов, отсутствуют унифицированный подход и четкие критерии для выбора между консервативной и оперативной тактикой.
Представляем клиническое наблюдение крайне тяжелого течения пневмококковой деструктивной пневмонии у ребенка 3 лет 8 мес., осложненной тотальным поражением легкого и формированием бронхоплевральных свищей. Целью публикации являются анализ успешного опыта мультидисциплинарного подхода к выбору методов консервативно-хирургического лечения, а также обсуждение современных аспектов диагностики, патогенеза и тактики ведения подобных пациентов.
Клиническое наблюдение
Мальчик С., 3 года 8 мес. (30.08.2020 г. р.), поступил в инфекционную клиническую больницу с диагнозом «Острый бронхит. Внебольничная пневмония?».
Анамнез заболевания: 23.05.2024, через 4 дня после возвращения из Таиланда, у ребенка повысилась температура до 39,7 °C, появились кашель и насморк. При осмотре педиатром диагностирована острая инфекция верхних дыхательных путей, назначена симптоматическая терапия. В течение нескольких дней состояние ребенка прогрессивно ухудшалось: на фоне продолжающейся лихорадки мальчик отказался от еды и питья, отмечалась выраженная слабость, появилась одышка. В связи с отрицательной динамикой на 5-е сутки заболевания госпитализирован в инфекционное отделение в тяжелом состоянии.
Анамнез жизни: мальчик от первой беременности, протекавшей на фоне анемии, от первых самостоятельных родов в срок. Масса тела при рождении 3650 г, длина тела 56 см. Оценка по шкале Апгар 7/8 баллов. Раннее развитие без особенностей. В возрасте 1 года перенес острый тонзиллит, наблюдается оториноларингологом в связи с увеличением аденоидов до 3-й степени. Вакцинирован по календарю, в том числе полностью против гриппа и пневмококковой инфекции (капсулярные полисахариды 13 серотипов пневмококка; в возрасте 2, 11 и 17 мес.).
Физикальная диагностика: при поступлении в инфекционный стационар состояние тяжелое, в сознании, стонет. Масса тела 16 кг (0,37z), рост 105 см (0,65z). Кожа бледная, цианоз носогубного треугольника. Малопродуктивный кашель. Одышка смешанного характера с втяжением уступчивых мест грудной клетки. Частота дыхательных движений (ЧДД) 55 в 1 мин, SpO2 92%. Отмечается притупление перкуторного звука справа, аускультативно справа на фоне ослабленного дыхания выслушиваются мелкопузырчатые хрипы. Тоны сердца ясные, частота сердечных сокращений (ЧСС) 145 в 1 мин, артериальное давление (АД) 90/60 мм рт. ст.
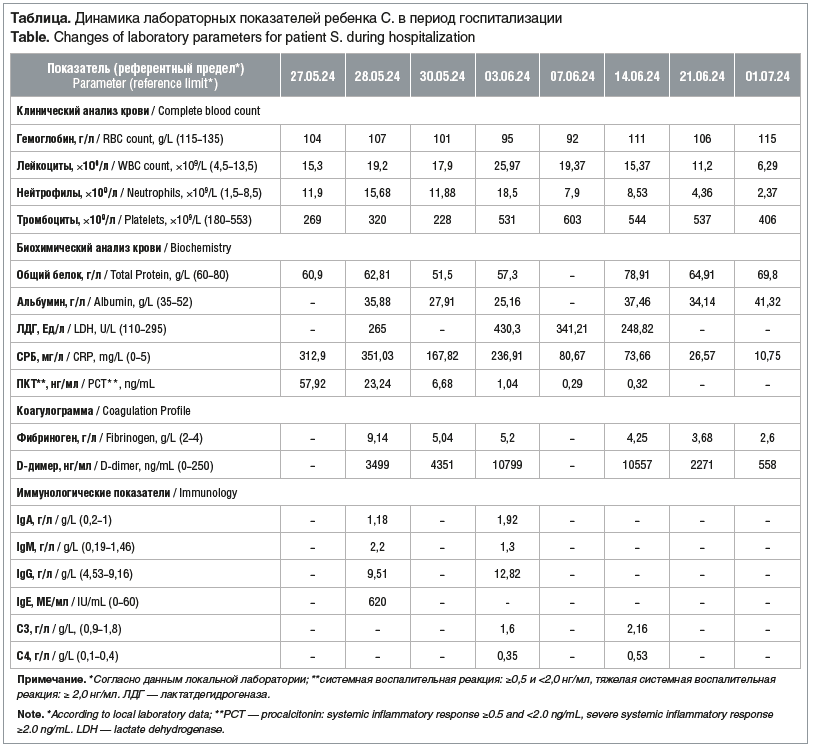
Лабораторные исследования: при поступлении выявлены лейкоцитоз до 15,3×109/л с нейтрофилезом (77,3%), небольшое снижение уровня гемоглобина (104 г/л), повышение уровней С-реактивного белка (СРБ, 312,9 мг/л) и прокальцитонина (ПКТ, 57,92 нг/мл) (см. таблицу). Экспресс-тесты на грипп А и В, SARS-CoV-2 отрицательные.

Инструментальные исследования: по данным мультиспиральной компьютерной томографии (МСКТ) органов грудной полости (ОГП) визуализирована правосторонняя полисегментарная пневмония (рис. 1).

На 6-е сутки заболевания ребенок был переведен в ОРИТ ДКГБ св. Владимира с диагнозом «внебольничная правосторонняя полисегментарная пневмония, тяжелое течение, экссудативный плеврит справа, дыхательная недостаточность 2-й степени».
Динамика и исходы. Состояние при переводе 28.05.2024 тяжелое за счет инфекционного токсикоза и дыхательной недостаточности (ДН). В сознании, выраженная слабость. Проводилась кислородотерапия FiO2 30% 4 л/мин, на фоне которой SpO2 составляла 98%. ЧДД 42 в 1 мин, аускультативно справа дыхание ослаблено. Тоны сердца приглушены, ЧСС 122 в 1 мин, АД 106/73 мм рт. ст. Динамика лабораторных показателей в период госпитализации представлена в таблице. Помимо лейкоцитоза (19,2×109/л) со сдвигом влево (81,7% нейтрофилов, 14% палочкоядерных), значительного повышения уровня СРБ (351,03 мг/л) и ПКТ (23,24 нг/мл), воспалительный ответ характеризовался возросшим содержанием интерлейкина 6 (139,0 пг/мл при норме 0–5,9 пг/мл) и ферритина (268,21 мкг/л при норме 6–60 мкг/л).
На рентгенограмме ОГП картина правосторонней полисегментарной пневмонии. При УЗИ ОГП 28.05.2024 (6-е сутки заболевания) — правое легкое тотально безвоздушно, паренхима верхней и средней долей значительно диффузно изменена с неравномерным повышением эхогенности. Воздушная бронхограмма отсутствует. Эхопризнаки выпота в правой плевральной полости. Выявленные признаки свидетельствуют о высоком риске развития деструкции.
Ребенку была назначена комбинированная антибактериальная терапия: цефалоспорины III поколения и гликопептиды. При пункции правой плевральной полости 28.05.2024 было получено 350 мл серозно-геморрагического мутного выпота светло-розового цвета: белок 6,6 г/л, глюкоза 0,06 ммоль/л, цитоз 21875 кл/мкл, нейтрофилы 89%, лимфоциты 10%, плазматические клетки 1%. Плевральная полость дренирована. С целью восстановления бронхиальной проводимости была выполнена серия санационных бронхоскопий. Бронхоскопически визуализировались гнойные пробки в долевых бронхах (рис. 2). С целью восстановления микроциркуляции в зоне воспаления начата терапия низкомолекулярными гепаринами. 29.05.2024 (7-е сутки заболевания) была проведена торакоскопическая УЗ-санация правой плевральной полости с раствором антибиотика.

30.05.2024 (8-е сутки заболевания) — при УЗИ ОГП верхняя и средняя доли легкого консолидированы, неструктурны, с чередованием участков понижения и повышения эхогенности без четких контуров. Воздух прослеживается только в проекции корня легкого. Сосудистый рисунок резко обеднен. Констатированы массивные некротические изменения верхней и средней долей правого легкого (рис. 3). 31.05.2024 (9-е сутки заболевания) — мальчик в стабильно тяжелом состоянии переведен в отделение торакальной хирургии, где было продолжено проведение дренирования плевральной полости, санационные бронхоскопии. К 03.06.2024 (12-е сутки заболевания) по данным УЗИ ОГП на фоне безвоздушной ткани правого легкого в задних отделах появились множественные неправильной формы включения газа — дренированные зоны некроза легочной паренхимы. В передневерхней части легкого трансбронхиальное дренирование участков некроза отсутствовало. Справа визуализировались эхопризнаки пневмофибриноторакса. В этот период состояние ребенка оставалось тяжелым, начинающееся дренирование очагов деструкции сопровождалось подъемом температуры до 39,5 °С, повторным повышением уровней лейкоцитов (25,97×109/л), СРБ (236,91 мг/л), D-димера (10 799 нг/мл). Кроме того, отмечалось увеличение уровня ЛДГ (430,3 Ед/л при норме 110–295 Ед/л) как маркера повреждения тканей. В то же время уровень ПКТ продолжал снижаться (1,04 нг/мл). При МСКТ определялась тотальная консолидация верхней доли правого легкого, сегментарные бронхи прослеживались фрагментарно, визуализировались разнокалиберные воздушные полости от 1 до 9 мм, некоторые из них были сливными. Отмечена негомогенная консолидация средней и нижних долей. В средней доле выявлена полость с пенистым содержимым 29×31×9 мм, сообщающаяся с плевральной полостью (рис. 4).


05.06.2024 (14-е сутки заболевания) при УЗИ ОГП определялись множественные (без счета) включения газа 5–7 мм в диаметре во всех отделах легкого, сохранялись единичные недренированные зоны деструкции (рис. 5А). В нижнебоковом отделе достоверно прослеживалось формирование бронхоплевральных свищей (рис. 5В). Таким образом, повышение лабораторных маркеров воспаления было ассоциировано с начинающимся трансбронхиальным дренированием очагов некроза и формированием свищей. В связи с массивным сбросом воздуха по плевральному дренажу 10.06.2024 в правый главный бронх был установлен бронхоблокатор.
При микробиологическом исследовании плевральной жидкости получен рост S. pneumoniae, чувствительного к назначенным антибиотикам. В посеве крови рост микроорганизмов не выявлен. При исследовании методом полимеразной цепной реакции в реальном времени (ПЦР-РВ) в лаборатории молекулярной диагностики и эпидемиологии инфекций дыхательных путей ФБУН ЦНИИ Эпидемиологии Роспотребнадзора в плевральной жидкости и жидкости бронхоальвеолярного лаважа выявлена ДНК S. pneumoniae серотипа 3.
Постепенно на фоне проводимой терапии состояние ребенка улучшилось. Бронхоблокатор удален 24.06.2024 (33-и сутки заболевания). По данным МСКТ ОГП 04.07.2024 (38-е сутки госпитализации) сохранялась консолидация сегментов S1 и S3 справа, а также субплевральная консолидация сегментов S2, S4, S6. Воздушные полости с уменьшением в динамике. Неравномерное сужение верхнедолевого и сегментарных бронхов справа (рис. 6). Мальчик был выписан домой в удовлетворительном состоянии, продолжительность госпитализации составила 38 дней. За время болезни ребенок похудел на 4 кг (масса тела при выписке 12 кг). При выписке сохранялись редкий кашель, чувствительность в месте стояния дренажной трубки после ее удаления. Хронология течения болезни представлена на рисунке 7.



Ребенок осмотрен через 4 мес. после выписки из стационара. Состояние и самочувствие мальчика удовлетворительные. При контрольной МСКТ ОГП от 16.09.2024 (через 2,5 мес. после перенесенного заболевания) в верхней доле правого легкого определяются фиброзные спайки с формированием перибронхиальных воздушных полостей до 2 мм в диаметре (рис. 8). При повторной МСКТ ОГП в октябре 2025 г. сохраняются описанные поствоспалительные изменения без клинических проявлений.

Ребенку было проведено иммунологическое обследование: исследован уровень общих иммуноглобулинов А, M, G, E в сыворотке крови, выполнено иммунофенотипирование субпопуляций лимфоцитов. Согласно заключению врача-иммунолога нарушения показателей гуморального и клеточного звеньев иммунитета отсутствуют.
В течение 1 года после госпитализации трижды перенес ОРВИ в нетяжелой форме. Признаков ДН нет. Мальчик активен, занимается плаванием. Сохраняются постгоспитальные психологические нарушения в виде тревожности и крайне негативного отношения к любому виду обследования и медицинскому персоналу.
Обсуждение
В последнее время отмечается увеличение заболеваемости деструктивной пневмонией детей в возрасте преимущественно до 7 лет, ассоциированной с серотипами 3, 14, 19А S. pneumoniae, реже со Staphylococcus aureus, Streptococcus pyogenes и Haemophilus influenzae [4]. Однако в отечественной и зарубежной литературе недостаточно сведений о гнойной деструкции легких в детском возрасте, отсутствуют утвержденная классификация, унифицированный подход к ведению таких пациентов, нет единого мнения о необходимости инвазивных вмешательств и показаниях к ним. Представленное наблюдение демонстрирует крайне тяжелое течение пневмококковой ВП с тотальным поражением правого легкого, быстрым развитием мультифокальной деструкции и формированием бронхоплевральных свищей. Своевременная рациональная антибактериальная терапия в сочетании с антикоагулянтами и инвазивными манипуляциями позволила минимизировать неблагоприятные последствия тяжелейшего поражения правого легкого.
Деструкция легкого — нечастое серьезное осложнение ВП у детей, характеризующееся некрозом и гнойным расплавлением ткани легкого, нередко с присоединением плевральных осложнений [2]. К формам деструкции относят деструктивную (некротизирующую) пневмонию, абсцесс и гангрену легкого, причем с точки зрения патогенеза эти состояния в настоящее время рассматривают как единый патологический процесс [8, 9]. Наиболее тяжелым осложнением является гангрена легкого — крайняя степень некротизирующего повреждения легких, которая представляет собой бурно прогрессирующий и несклонный к отграничению от жизнеспособной легочной ткани гнойный или гнилостный некроз всего легкого или отделенной плеврой анатомической структуры (доли), в котором перемежаются зоны гнойного расплавления и неотторгнутого некроза. Основным признаком, определяющим тяжесть и распространенность некроза, является степень поражения сосудов с формированием микротромбов в микроциркуляторном русле [9].
У взрослых деструктивный процесс в легких нередко ассоциирован с такими отягощающими факторами, как алкоголизм, неконтролируемый сахарный диабет или интенсивное курение. Эти факторы могут быть причиной прогрессирования некроза паренхимы легкого вплоть до развития гангрены и необходимости хирургического удаления доли или целого легкого. Известно о роли как грам-отрицательных (Klebsiella pneumoniae, H. influenzae, Pseudomonas aeruginosa), так и грамположительных (S. pneumoniae, S. aureus, S. pyogenes) микроорганизмов в реализации гангрены легкого [7, 10]. По данным литературы, абсцесс и гангрена легкого у взрослых вызываются ассоциациями микроорганизмов, среди которых обязательно присутствует анаэробная и условно-анаэробная микрофлора [11, 12].
Гангрена легкого у детей описана как наиболее тяжелый вариант осложнения пневмонии, однако данные литературы ограничены редкими описаниями клинических случаев. Так, J. Hrubovčák et al. [13] описали случай у 5-летней девочки, госпитализированной на 6-е сутки заболевания с клиническими признаками инфекционно-токсического шока и ДН. Была диагностирована левосторонняя пневмония с поражением левого легкого, пиотораксом слева. Уровень маркеров воспаления был повышенным: СРБ 407 мг/л, ПКТ 10 мкмоль/л. Несмотря на применение антибиотиков широкого спектра действия, проведение торакоскопии, улучшения не было. Методом ПЦР в плевральной жидкости был выделен S. pneumoniae. Отсутствие улучшения, прогрессирующий пиоторакс позволили думать о развивающейся гангрене легкого. Было принято решение о лобэктомии, которая была проведена на 11-е сутки госпитализации. Интраоперационно была визуализирована абсцедирующая пневмония с гангреной нижней доли левого легкого, что потребовало ее резекции.
В статье G. Petrova et al. [14] представлен случай гангрены легкого у 4-летней девочки с неотягощенным анамнезом. Она была госпитализирована с жалобами на лихорадку, кашель, боль в грудной клетке справа. При поступлении обращали на себя внимание выраженная интоксикация, притупление перкуторного звука справа, влажные хрипы в этой области при аускультации. На рентгенограмме ОГП подтверждена правосторонняя нижнедолевая пневмония, небольшой выпот в правой плевральной полости. Назначенная антибактериальная терапия оказалась неэффективна. На фоне смены терапии отмечалось временное клиническое улучшение, однако на 7-й день госпитализации состояние девочки резко ухудшилось, вырос уровень лабораторных маркеров воспаления. Дренирование плевральной полости не дало ожидаемого результата. Была проведена лобэктомия справа с гистологическим подтверждением гангрены. Посевы всех исследованных сред были отрицательными.
Приведенные наблюдения схожи с описываемым нами случаем манифестации заболевания (симптомы респираторной инфекции), быстрым нарастанием инфекционного токсикоза, ДН. Из-за отсутствия эффекта от проводимой терапии даже при смене антибиотиков в описанных примерах потребовалось оперативное вмешательство, были подтверждены гангренозные изменения легкого. Исход в обоих случаях был благоприятным.
Представленное нами наблюдение также иллюстрирует быстрое развитие тяжелейшего некротического процесса в легких, несмотря на адекватную терапию с момента госпитализации. На риск реализации гангрены легкого у нашего пациента указывали как клинические данные в виде бурно развивающегося инфекционного процесса с выраженным токсикозом в сочетании с крайне высоким уровнем маркеров воспаления, так и данные инструментальных исследований. Рентгенологически в день госпитализации (6-е сутки заболевания) визуализировалось тотальное затемнение правого легкого. На 7-е сутки госпитализации (13-е сутки заболевания) на фоне уплотненного легкого прослеживались воздушные включения — полости, размером 1–9 мм, некоторые сливные, впоследствии увеличивающиеся в размере. Ряд авторов отмечает высокую корреляцию между характеристиками УЗИ легких и МСКТ в распознавании деструктивных изменений при ВП у детей, особенно при массивном некрозе. Нарушение перфузии или гипоэхогенные очаги при УЗИ легких являются предиктором массивного некроза [15]. Мы располагаем эхографическими данными развития патологического процесса в представленном наблюдении. При поступлении в профильный стационар на 6-е сутки заболевания эхографически визуализировалось тотальное поражение легкого с блоком воздушной проводимости и нарушением кровотока в зонах поражения с отсутствием отграничения от здоровых тканей. Структурность паренхимы легкого не прослеживалась. Антибиотики широкого спектра действия, антикоагулянтная терапия, бронхоскопическая санация, дренирование плевральной полости в данном случае не предотвратили развития деструкции. Неэффективность лечения в первую неделю госпитализации объясняется девитализацией всех структур легкого (паренхимы, сосудов, бронхов) в период поступления ребенка в стационар и невозможностью проникновения антибактериальных препаратов в некротизированную зону [16]. Нарушение кровоснабжения легкого и блок воздушной проводимости по данным УЗИ легких сохранялись в первые 7 дней пребывания в стационаре. В течение этого времени состояние мальчика оставалось тяжелым, маркеры воспаления медленно снижались (см. таблицу). Улучшение состояния было ассоциировано с началом дренирования некротизированных очагов трансбронхиально и в плевральную полость из-за формирования бронхоплевральных свищей. В этот период постепенное восстановление кровотока в очаге воспаления было ассоциировано с увеличением уровней лейкоцитов, СРБ при снижении уровня ПКТ в крови. Значительное повышение уровня D-димера отражало активацию фибринолиза в условиях эндотелиального повреждения и тромбообразования в сосудах легких. Примененная хирургическая тактика в сочетании с медикаментозной терапией минимизировали последствия обширного некротического процесса.
Тромбоз легочных сосудов является одной из патологических характеристик деструктивной пневмонии и может привести к формированию обширных зон некроза. По данным литературы [17], МСКТ ОГП с контрастированием при деструкции подтверждает облитерацию сосудов пораженного сегмента, нарушение кровообращения в тканях и отсутствие накопления контрастного вещества в пораженном сегменте. Y.C. Hsieh et al. [18] сообщают, что у 90% пациентов, подвергшихся хирургической резекции легкого при деструкции, патологической находкой оказались инфарктные изменения. Однако при гангрене именно тромбоз сосудов является ведущим фактором патогенеза, и именно выраженность тромбообразования отличает гангрену легкого от некротизирующей пневмонии и абсцесса. Степень нарушения перфузии, необратимость изменений кровотока в легочных и бронхиальных сосудах определяют тяжесть и характер изменений газообмена и гемодинамики. Полное прекращение кровотока и оксигенации создает условия для размножения бактерий. Основной причиной развития гангрены легкого становится глубокий необратимый блок перфузии с последующим гнойным расплавлением тканей [8]. Y.C. Hsieh et al. [18] также отмечают, что патологические признаки гангрены легкого определялись у большинства наблюдавшихся пациентов при формировании бронхоплевральной фистулы.
Этиологическим фактором, вызвавшим тяжелейшую пневмонию, оказался S. pneumoniae, что было подтверждено микробиологически, методом ПЦР-РВ был определен серотип 3 пневмококка, характеризующийся высокой вирулентностью и ассоциированный с наиболее тяжелым течением заболевания даже у привитых [19]. В то же время большое значение имели особенности ответа организма. Хотя иммунологическое исследование не выявило явных изменений гуморальных и клеточных факторов защиты в наблюдаемом случае, крайне высокие уровни маркеров воспаления в разгар заболевания свидетельствовали о гиперергическом характере ответа организма на инфекцию. Дисбаланс про- и противовоспалительных факторов с гиперцитокиновым ответом, гиперкоагуляционной направленностью, приводящими к локальному тромбообразованию в зоне воспаления, явились причиной тяжелых осложнений ВП.
При обширном некрозе легкого практически всегда требуется хирургическое лечение. Отсроченное вмешательство может привести к необратимым последствиям: системной воспалительной реакции и летальному исходу в результате септического шока [20, 21]. Однако возможны случаи восстановления проходимости бронха, ведущего к полости, и удаления некротизированных тканей трансбронхиально [22].
Приведенное клиническое наблюдение следует трактовать как обширный некроз легкого с тяжелейшим поражением органа и бурным развитием патологического процесса на фоне системной воспалительной реакции, неизбежной деструкцией обширной зоны с быстрым и предсказуемым формированием бронхоплевральных свищей, несмотря на адекватную терапию. Слаженная работа команды специалистов с участием торакальных хирургов, пульмонологов, реаниматологов, специалистов лучевой диагностики позволила успешно курировать пациента с крайне тяжелой формой пневмококковой деструкции легких. Однако обширный некроз легкого привел к необратимым изменениям в виде фиброзных спаек с формированием единичных перибронхиальных воздушных полостей в верхней доле правого легкого.
Заключение
Деструктивная пневмония представляет собой жизнеугрожающее осложнение ВП у детей. Представленное клиническое наблюдение демонстрирует стремительное развитие крайне тяжелого варианта осложненной ВП с тотальным поражением правого легкого с неизбежным формированием деструкции и бронхоплевральных свищей. Бурное развитие деструкции и прогрессирование процесса, несмотря на комплексную терапию, дают основание для клинической настороженности в отношении формирования обширных зон некроза и бронхоплевральных свищей, что зависит от возбудителя и определяется степенью нарушения кровотока.
Рациональная антибиотикотерапия, своевременное малоинвазивное хирургическое вмешательство, использование антикоагулянтов позволили минимизировать неблагоприятные последствия заболевания. В таких случаях основой успешного лечения является мультидисциплинарный подход с участием команды специалистов. Актуальным направлением остается поиск причин и факторов риска реализации тяжелых осложнений ВП у детей.
Сведения об авторах:
Толстова Евгения Михайловна — к.м.н., доцент кафедры педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0001-8340-3064
Кузина Софья Романовна — аспирант кафедры педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0002-8565-266X
Беседина Марина Валерьевна — к.м.н., доцент кафедры педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0003-1160-7855
Эмирова Хадижа Маратовна — д.м.н., профессор кафедры педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0002-7523-5889
Зайцева Ольга Витальевна — д.м.н., профессор, заведующая кафедрой педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0003-3426-3426
Зайцева Надежда Станиславовна — к.м.н., доцент кафедры педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0000-0003-1868-1396
Елькина Мария Александровна — м.н.с. лаборатории молекулярной диагностики и эпидемиологии инфекций дыхательных путей ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0003-4769-6781
Яцышина Светлана Борисовна — к.б.н., заведующая лабораторией молекулярной диагностики и эпидемиологии инфекций дыхательных путей ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0003-4737-941X
Аминова Азиза Алишеровна — клинический ординатор кафедры педиатрии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; ORCID iD 0009-0004-3040-9883
Турищев Илья Владимирович — заведующий отделением реанимации и интенсивной терапии ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0000-0002-5277-9808
Хаспеков Дмитрий Викторович — к.м.н., заведующий торакальным хирургическим отделением ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0000-0002-6808-7670
Сар Артур Саратович — врач — торакальный хирург ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0000-0002-8959-2457
Ганиева Алла Маратовна — врач-рентгенолог ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0009-0002-5435-1204
Шолохова Наталия Александровна — д.м.н., профессор кафедры лучевой диагностики ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1, стр. 1; заведующая отделением лучевой диагностики ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0000-0002-0412-4938
Ткаченко Надежда Витальевна — врач-пульмонолог ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0000-0003-4240-0072
Ольхова Елена Борисовна — д.м.н., профессор кафедры лучевой диагностики ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; заведующая отделением ультразвуковой диагностики ГБУЗ «ДГКБ св. Владимира ДЗМ»; 107014, Россия, г. Москва, ул. Матросская Тишина, д. 12А; ORCID iD 0000-0003-3757-8001
Горелов Александр Васильевич — академик РАН, д.м.н., заведующий кафедрой инфекционных болезней и эпидемиологии ФГБОУ ВО «Российский университет медицины» Минздрава России; 127006, Россия, г. Москва, ул. Долгоруковская, д. 4; заместитель директора по научной работе ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; профессор кафедры детских болезней Клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-9257-0171
Контактная информация: Толстова Евгения Михайловна, e-mail: tepec@yandex.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 23.12.2025.
Поступила после рецензирования 12.01.2026.
Принята в печать 30.01.2026.