Введение
Острые респираторные инфекции (ОРИ) являются актуальной проблемой современной медицины [1]. Согласно данным Государственного доклада «О состоянии санитарно-эпидемиологического благополучия населения Российской Федерации в 2024 году» зафиксировано 31,4 млн случаев ОРИ, что представляет наибольшую экономическую значимость среди инфекционных заболеваний1.
Нередко ОРИ протекают с клиникой острого тонзиллофарингита, под этим термином понимают острое воспаление лимфоидной ткани небных миндалин и лимфоидных элементов задней стенки глотки [2]. Несмотря на отсутствие термина в Международной классификация болезней 10-го и 11-го пересмотра, он часто используется в медицинской литературе в качестве объединения терминов «острый фарингит» и «острый тонзиллит».
В зависимости от возраста острый тонзиллофарингит имеет разную этиологию. До 4–5 лет у детей преобладает вирусная и вирусно-бактериальная этиология острого тонзиллофарингита, которая нередко ассоциирована с вирусами герпеса человека. После 5 лет важное этиологическое значение приобретает Streptococcus pyogenes, который вызывает до 75% острых тонзиллофарингитов [2]. Однако, помимо патогенных бактерий, условно-патогенная флора также может быть причинно-значимым фактором воспаления, в особенности при обнаружении нескольких ее представителей у одного больного. По данным литературы, S. pyogenes занимает первое место среди бактериальных возбудителей острого тонзиллофарингита, на втором месте идут стрептококки других групп (в том числе условно-патогенные), на третьем и четвертом месте — Staphylococcus aureus и Haemophilus influenzae [3].
Особую этиологическую значимость имеет носительство условно-патогенных и патогенных микроорганизмов в рото- и носоглотке у детей с рекуррентными респираторными заболеваниями. Данная группа детей зачастую необоснованно получает повторные курсы антибактериальной терапии, что вносит свой вклад в развитие антибактериальной резистентности микроорганизмов [4].
Современная медицина столкнулась с глобальной проблемой стремительного роста антибиотикорезистентности патогенных бактерий, что существенно ограничивает возможности лечения инфекционных заболеваний. По данным последних исследований, ежегодно растет смертность, обусловленная резистентностью бактериальных респираторных возбудителей, что делает эту проблему одной из наиболее актуальных в здравоохранении [5].
Особую тревогу вызывает распространение полирезистентных штаммов таких бактерий, как Pseudomonas aeruginosa, Klebsiella pneumoniae, Acinetobacter baumannii и S. aureus, которые не только устойчивы к большинству антибиотиков, но и способны формировать биопленки, защищающие их от воздействия антибактериальных препаратов, усложняя их эрадикацию2 [6]. В условиях ограниченного арсенала новых антибактериальных препаратов возрастает интерес к альтернативным методам терапии, среди которых перспективным направлением является применение бактериофагов.
Бактериофаги — это вирусы, избирательно уничтожающие бактериальные клетки, что делает их эффективным инструментом в борьбе с инфекциями. В отличие от антибиотиков, фаги обладают высокой специфичностью, минимизируя воздействие на нормальную микрофлору, а также способны проникать через биопленки и ресенсибилизировать бактерии к антибактериальным препаратам. Современные исследования демонстрируют значительную эффективность и безопасность фаготерапии при лечении респираторных инфекций, включая случаи с антибиотикорезистентными штаммами бактерий [7].
Одним из перспективных подходов к лечению рекуррентных респираторных инфекций у детей с проявлениями тонзиллофарингита является включение бактериофагов/фагов в комплексную терапию для безопасной элиминации патогенной и условно-патогенной микрофлоры носоглотки. Частые эпизоды ОРИ и необоснованное назначение антибиотиков способствуют формированию устойчивости микроорганизмов, что усугубляет течение заболеваний и повышает риск осложнений. В этой связи использование поливалентного препарата Секстафаг® (Пиобактериофаг), содержащего несколько фагов, активных против широкого спектра бактериальных патогенов, представляется перспективным направлением в комплексной терапии таких состояний [4, 8].
Настоящая наблюдательная программа направлена на изучение опыта применения препарата Секстафаг® у детей с рекуррентными респираторными заболеваниями и эпизодами ОРИ, сопровождающейся тонзиллофарингитом. Полученные данные позволят расширить возможности лечения респираторных инфекций в педиатрической практике, минимизировать риск развития резистентности, а также снизить риски развития побочных эффектов от антибиотикотерапии.
Цель исследования: оценка эффективности и без-опасности Пиобактериофага поливалентного в терапии ОРИ с явлениями тонзиллофарингита у детей с рекуррентными респираторными заболеваниями.
Материал и методы
Задачи исследования
Оценить клиническую эффективность препарата Секстафаг® Пиобактериофаг поливалентный в лечении ОРИ с явлениями тонзиллофарингита у детей с рекуррентными респираторными заболеваниями.
Оценить частоту развития нежелательных явлений (НЯ) при применении препарата Секстафаг® Пиобактериофаг поливалентный для лечения ОРИ с явлениями тонзиллофарингита у детей с рекуррентными респираторными заболеваниями.
В исследование было включено 46 детей обоих полов в возрасте от 1 года до 17 лет (медиана (Ме) 5 лет), из них 28 мальчиков и 18 девочек. Исследование проведено в дизайне проспективной наблюдательной программы в рамках амбулаторного приема на базе клинического отдела инфекционной патологии ГБУЗ Московской области «Химкинская клиническая больница» и включало в себя оценку 2 визитов.
Критерии включения: установленный диагноз ОРИ с явлениями тонзиллофарингита; длительность симптомов 3–5 дней; отрицательный стрептатест на момент включения в исследование; температура тела, измеренная в подмышечной впадине, за период заболевания до момента скрининга не превышала 38 °С; наличие 8 и более эпизодов респираторных инфекций в год у детей в возрасте до 3 лет или 6 и более эпизодов у детей старше 3 лет в анамнезе; наличие нескольких курсов антибактериальной терапии за последние 6 мес.; подписанное пациентом добровольное информированное согласие на участие в исследовании.
Критерии исключения: возраст пациентов моложе 1 года и старше 17 лет; наличие у пациентов гиперчувствительности, аллергических реакций на любые компоненты препарата исследования; применение системных или местных глюкокортикостероидных препаратов в течение 30 дней до начала исследования; повышение температуры тела более 38 °C в течение 3 сут и более с момента манифестации заболевания и на скрининге до применения жаропонижающих препаратов; низкая приверженность пациента лечению или неспособность выполнения процедур и соблюдения ограничений согласно протоколу исследования; состояния или заболевания, которые, по мнению исследователей, могли привести к тому, что участие в исследовании для пациента будет небезопасным (в том числе первичные и вторичные иммунодефициты, орфанные заболевания и т. п.); вакцинация пациента в течение 14 дней до включения в исследование; участие в каком-либо другом клиническом исследовании в течение последних 3 мес.
Все пациенты получали Секстафаг® Пиобактериофаг поливалентный в составе комплексной терапии ОРИ согласно инструкции по применению лекарственного средства в возрастной дозировке, местно в виде орошения зева 2 р/день, а также в виде капель в носовые ходы на чистые слизистые 3 р/день в течение 10 дней. Комплексная терапия включала жаропонижающие средства, препараты для элиминационно-ирригационной терапии (изотонические солевые растворы), топические деконгестанты (местно, в виде носовых капель, аэрозоля, геля или мази), антигистаминные препараты, согласно клиническим рекомендациям, а также противовирусные препараты с прямым и непрямым механизмом действия при наличии сопутствующей активной герпесвирусной инфекции.
Для оценки эффективности применения препарата Секстафаг® Пиобактериофаг поливалентный проводился анализ динамики клинической симптоматики по специально разработанным балльным шкалам на 1-м визите (1-й день включения) и 2-м визите (10-й день). Оценивались следующие клинические показатели: катаральные явления в зеве, отек и гиперемия носовых ходов при риноскопии, выраженность гранулезного фарингита, лимфоаденопатия и состояние небных миндалин. Выраженность гранулярного фарингита, лимфоаденопатии, гипертрофии небных миндалин оценивалась по балльной системе (от 0 до 3 баллов, где 0 — отсутствие симптома, а 3 балла — симптом максимально выражен). Кроме того, оценивались результаты клинического анализа крови, бактериологического исследования материала мазков из ротоглотки, а также определения лабораторных маркеров вирусов герпеса человека, которые назначались пациентам по показаниям.
Статистическая обработка данных проводилась с использованием программного обеспечения StatTech v.4.8.11 (ООО «Статтех», Россия). Проверка количественных данных на нормальность распределения осуществлялась с помощью критерия Шапиро — Уилка. Данные с нормальным распределением представлены как M (SD), данные без нормального распределения — как Me [Q1; Q3]. Категориальные переменные описаны в виде абсолютных значений и процентов (n, %). Для сравнения связанных выборок применялись: парный t-критерий Стьюдента (для нормально распределенных количественных данных), критерий Уилкоксона (для количественных данных без нормального распределения) и тест Макнемара (для бинарных и категориальных данных). Статистическая значимость различий определялась при p<0,05.
Результаты исследования
На момент включения в исследование субфебрильная лихорадка зафиксирована у 17 пациентов (10 мальчиков и 7 девочек), боли в горле отмечали все дети.
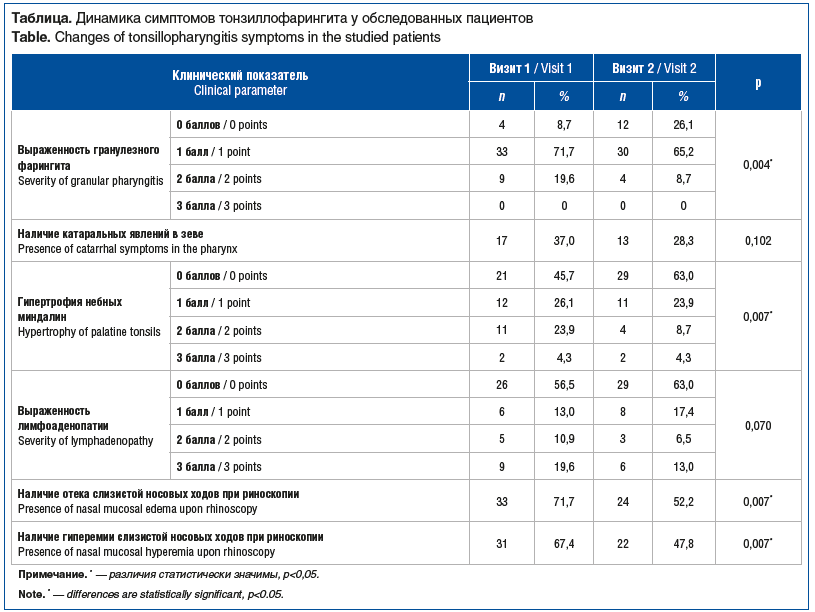
В результате проведенной терапии нормализация температуры отмечалась у всех детей в течение первых 5 дней наблюдения, отсутствие боли в горле у 98% пациентов через 10 дней, положительная динамика ряда клинических показателей (см. таблицу).

При анализе динамики фарингоскопической картины выраженность явлений гранулезного фарингита до лечения в 2 балла наблюдалась у 9/20% детей, а после лечения — только у 4/9% детей. Выраженность гранулезного фарингита на 1 балл до лечения зафиксирована у 33/72% пациентов, а после лечения — у 30/65%. Не зафиксировано изменений задней стенки глотки по типу гранулезного фарингита (0 баллов) до терапии у 4/9% детей, после лечения количество таких детей увеличилось до 12/26% (p=0,004). Наличие катаральных явлений в зеве до лечения отмечено у 17/37% детей, после лечения — у 13/28% (р=0,102).
Гипертрофия небных миндалин до лечения зафиксирована у 25/54% детей, при этом гипертрофия 1-й степени — у 12/26%, 2-й степени — у 11/24%, 3-й степени — у 2/4% пациентов. После лечения размер небных миндалин достиг нормы у 29/63% детей, тогда как гипертрофия 1-й степени сохранялась у 11/24%, гипертрофия 2-й степени — у 4/9% и гипертрофия 3-й степени — у 2/4% пациентов (p=0,007).
Выраженность регионарной лимфоаденопатии до лечения была максимальной (3 балла) у 9/20% детей, после лечения — у 6/13%, оценка в 2 балла до лечения отмечена у 5/11% детей, после лечения — у 3/7%, оценка в 1 балл до лечения — у 6/13%, после лечения — у 8/17% пациентов. Регионарной лимфоаденопатии до лечения не выявлено у 26/57% пациентов, после лечения — у 29/63% (р=0,070).
Отек и гиперемия слизистой носовых ходов при проведении риноскопии на 1-м визите отмечались у 33/72% и 31/67% пациентов соответственно. На 2-м визите количество детей, у которых определялись отек и гиперемия слизистой носовых ходов при риноскопии, уменьшилось до 24/52% и 22/48% (р=0,007 и р=0,007 соответственно).
Клинический анализ крови был назначен по показаниям 31/67% пациентов, при анализе динамики лабораторных маркеров не было выявлено статистически значимых изменений. На 1-м визите медиана уровня лейкоцитов составила 7,46 [5,74; 8,68]×109/л, на 2-м визите медиана данного показателя уменьшилась до 6,71 [5,10; 9,00]×109/л, (р=0,146). Медиана уровня нейтрофилов и лимфоцитов до лечения составила 3,07 [2,23; 4,64]×109/л и 3,00 [2,62; 3,89]×109/л, после лечения — 2,46 [1,97; 3,63]×109/л и 2,83 [2,24; 4,12]×109/л соответственно (р=0,090 и р=0,337 соответственно).
До терапии в материале мазков из ротоглотки у 96% пациентов обнаружены S. aureus, Moraxella catarrhalis, H. influenzae, Streptococcus pneumoniae, K. pneumoniae, Streptococcus viridans, Staphylococcus epidermidis, Candida albicans, после лечения — только у 67% (р=0,011). Соотношение обнаруженных возбудителей у детей до и после лечения показано на рисунке. У 6 пациентов до лечения и 4 пациентов после лечения обнаружена условно-патогенная микрофлора без точной идентификации вида бактерии.
Максимальное количество у одного пациента в материале мазков из ротоглотки при бактериологическом исследовании до лечения — 3 вида микроорганизмов (у 3/11% детей). После окончания курса лечения 3 бактерии обнаруживались только у 1/4% детей. Выявление 2 бактерий в одном материале мазков из ротоглотки до лечения было зафиксировано у 11/41% пациентов, после лечения — у 8/30%. Один возбудитель обнаруживался до лечения у 12/44% пациентов, после лечения — у 9/33%. На момент включения в исследование бактериальные агенты в ротоглотке не были обнаружены только у одного пациента (4%), после лечения — у 1/3 (9/33%) обследованных, р=0,020.
У 9/20% пациентов по показаниям проводилось определение лабораторных маркеров вирусов герпеса человека, а именно вируса Эпштейна — Барр (ВЭБ), цитомегаловируса (ЦМВ), вируса герпеса человека типа 6 А/В (ВГЧ-6А/В).
До лечения лабораторные маркеры ВГЧ-6А/В отсутствовали у 1/11% детей, латентные формы инфекции диагностированы у 7/78%, активные формы — у 1/11% пациентов. После лечения лабораторные маркеры также отсутствовали у 1/11% детей, латентная ВГЧ-6-инфекция определялась у 8/89% детей, активной ВГЧ-6-инфекции не было (p=0,785).
Лабораторные маркеры ВЭБ до лечения не зафиксированы у 2/22% детей, латентная инфекция была у 3/33% пациентов, активная ВЭБ-инфекция — у 4/44% детей. После лечения лабораторные маркеры ВЭБ отсутствовали у 1/11% пациентов, латентная ВЭБ-инфекция определялась у 6/67% детей, активная инфекция — у 2/22% (р=0,102).
Латентная ЦМВ-инфекция до терапии выявлена у 2/22% пациентов, лабораторные маркеры ЦМВ отсутствовали у 7 пациентов, после терапии результаты обследования пациентов не поменялись.
Нежелательных явлений и серьезных НЯ (СНЯ) зарегистрировано не было.
Таким образом, подключение препарата Секстафаг® Пиобактериофаг поливалентный к комплексной терапии острого тонзиллофарингита у детей даже с рекуррентными респираторными заболеваниями способствовало как купированию системных симптомов (лихорадки, синдрома интоксикации, болевого синдрома), так и нормализации фарингоскопической картины. Кроме того, продемонстрирован превосходный профиль безопасности.

Обсуждение
Поражение ротоглотки при ОРИ у детей — один из наиболее частых симптомов, с которыми сталкивается врач-педиатр в своей повседневной практике. Подобные изменения, возникающие у детей с повторными респираторными эпизодами, часто являются причиной необоснованного назначения системной антибактериальной терапии и развития хронической патологии ЛОР-органов, связанной с персистенцией условно-патогенных микроорганизмов. В связи с этим эффективная и безопасная терапия эпизода ОРИ, протекающего с явлениями тонзиллофарингита у детей с рекуррентными респираторными заболеваниями, становится важной педиатрической проблемой, требующей новых подходов к ее решению.
Нами продемонстрировано, что подключение комплексного бактериофага в качестве местной терапии эпизода ОРИ, начиная с 3-го дня от начала заболевания, приводило как к купированию общего интоксикационного синдрома и болей в горле в течение 5 дней, так и к улучшению фарингоскопической картины.
Важным аспектом является то, что при политопности поражения органов респираторного тракта, характерного для ОРИ, применение бактериофага способствовало достоверному уменьшению симптомов как со стороны ротоглотки, так и со стороны носоглотки.
Важным аспектом является этиологическая структура выявленных возбудителей острого тонзиллофарингита. В нашем исследовании у 96% пациентов при первичном обследовании в мазках из ротоглотки были обнаружены различные бактериальные агенты, среди которых доминировали S. aureus, S. pneumoniae, H. influenzae и M. catarrhalis. Данная структура полностью соответствует современным данным литературы о ведущей роли условно-патогенной микрофлоры при тонзиллофарингитах нестрептококковой этиологии [3, 9]. Частая регистрация нескольких возбудителей в материалах мазков из ротоглотки подчеркивает неоднородность микробного пейзажа у данной категории детей и объясняет сложность подбора эффективной стандартной терапии.
Применение исследуемого препарата привело к статистически значимому снижению как частоты выделения бактерий (с 96 до 67%, p=0,011), так и микробной нагрузки, что подтверждено уменьшением количества видов микроорганизмов, выделяемых в биологическим материале от одного пациента (p=0,020). Наши данные хорошо согласуются с результатами других исследователей, изучавших применение комбинированных фаговых препаратов. В частности, исследование З.Ф. Хараевой и соавт. [10] продемонстрировало, что терапия препаратами Пиополифаг и Секстафаг® является эффективным методом санации носоглотки и зева у бактерионосителей S. aureus и пациентов с хроническим тонзиллитом в межрецидивный период. Авторы также отметили значительное снижение обсемененности слизистых, хотя и не всегда достигалась полная эрадикация возбудителя, что сходно с нашими результатами.
Отличный профиль безопасности препарата Пиобактериофаг поливалентный, подтвержденный в нашем исследовании (не зарегистрировано ни одного НЯ или СНЯ), является его критически важным преимуществом. Это особенно актуально для детей с рекуррентными инфекциями, которые зачастую получают множество курсов антибактериальной терапии с риском развития побочных эффектов и формирования антибиотикорезистентности. Фаготерапия, не оказывающая влияния на нормальную микробиоту и лишенная системной токсичности, представляет собой перспективную альтернативу или дополнение к антибиотикам в подобных клинических ситуациях.
Таким образом, проведенное исследование демонстрирует, что включение препарата Секстафаг® в комплексную терапию ОРИ с явлениями тонзиллофарингита у детей с рекуррентными респираторными заболеваниями способствует достоверному улучшению клинической картины и положительной микробиологической динамике. Полученные результаты согласуются с растущим объемом данных об эффективности фаготерапии в лечении инфекционно-воспалительных заболеваний ЛОР-органов [11, 12].
Ограничения исследования: настоящее исследование носило наблюдательный характер и не включало группу контроля. Кроме того, выборка пациентов была относительно немногочисленной, а оценка отдаленных результатов (частоты рецидивов) не входила в задачи данной работы.
Заключение
Включение в комплексную терапию острого тонзиллофарингита Пиобактериофага поливалентного местно в носо- и ротоглотку курсом 10 дней продемонстрировало статистически значимую положительную динамику по ряду ключевых клинических и микробиологических параметров. Отмечены существенное уменьшение выраженности гранулярного фарингита и гипертрофии небных миндалин, а также значимое снижение частоты отека и гиперемии слизистой носовых ходов по данным риноскопии. В течение первых 5 дней у всех пациентов нормализовалась температура тела, к окончанию курса у 98% отсутствовала боль в горле. Кроме того, доля пациентов с выделением хотя бы одного бактериального возбудителя из ротоглотки снизилась с 96 до 67%. Также зафиксировано достоверное уменьшение микробной нагрузки, выразившееся в снижении количества возбудителей, выделяемых от одного пациента.
Терапия препаратом Пиобактериофаг поливалентный охарактеризовалась превосходным профилем безопасности. В ходе исследования не было зарегистрировано ни одного НЯ или СНЯ, связанных с применением препарата.
Таким образом, полученные результаты позволяют рекомендовать Пиобактериофаг поливалентный для местной терапии эпизода ОРИ с явлениями тонзиллофарингита у детей с рекуррентными респираторными инфекциями с целью элиминации бактериального компонента воспаления.
СВЕДЕНИЯ ОБ АВТОРАХ:
Власов Петр Владимирович — аспирант ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0009-0009-3947-4813
Мелехина Елена Валериевна — д.м.н., доцент, ведущий научный сотрудник клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0002-9238-9302
Музыка Анна Драгиевна — к.м.н., старший научный сотрудник клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0002-2269-2533
Контактная информация: Власов Петр Владимирович e-mail: vlsvpetr@gmail.com
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 30.07.2025.
Поступила после рецензирования 22.08.2025.
Принята в печать 16.09.2025.
ABOUT THE AUTHORS:
Petr V. Vlasov — postgraduate student, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0009-0009-3947-4813
Elena V. Melekhina — Dr. Sc. (Med.), Associate Professor, Leading Researcher of the Clinical Department of Infectious Pathology, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human WellBeing; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0002-9238-9302
Anna D. Muzyka — C. Sc. (Med.), Senior Researcher of the Clinical Department of Infectious Pathology, Central Research Institute of Epidemiology of the Russian Federal Service for Supervision of Consumer Rights Protection and Human Well-Being; 3A, Novogireevskaya str., Moscow, 111123, Russian Federation; ORCID iD 0000-0002-2269-2533
Contact information: Petr V. Vlasov, e-mail: vlsvpetr@gmail.com
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 30.07.2025.
Revised 22.08.2025.
Accepted 16.09.2025.
1Государственный доклад «О состоянии санитарно-эпидемиологического благополучия населения Российской Федерации в 2024 году». (Электронный ресурс.) URL: https://www.rospotrebnadzor.ru/documents/details.php?ELEMENT_ID=30171 (дата обращения: 25.07.2025).
2World Health Organization. WHO publishes list of bacteria for which new antibiotics are urgently needed. 2017. (Electronic resource.) URL: https://www.who.int/news/item/27-02-2017-who-publishes-list-of-bacteria-for-which-new-antibiotics-ar… (access date: 25.07.2025).