Введение
Гериатрия как наука, занимающаяся здоровьем и благополучием людей старшего возраста, уделяет все больше внимания стадии «предрасположенности к болезни». Это состояние характеризуется снижением физиологических резервов организма и повышенной вероятностью развития хронических заболеваний, при этом отсутствуют явные клинические проявления. Данный период имеет решающее значение, поскольку своевременные меры могут оказать значительное влияние на процесс старения и предотвратить или отсрочить наступление инвалидности и зависимости [1, 2].
Предболезнь не является четким клиническим диагнозом, а представляет собой континуум состояний между здоровьем и болезнью. Он включает в себя широкий спектр факторов, таких как генетическая предрасположенность, образ жизни, влияние окружающей среды и совокупное воздействие физиологических изменений, связанных со старением. В гериатрической практике выявление предболезни часто основывается на всесторонней оценке функционального статуса, когнитивных функций, психологического состояния и наличия факторов риска, например артериальной гипертензии, дислипидемии и нарушенной толерантности к глюкозе. Важно понимать, что предболезнь — это не просто состояние, предшествующее конкретному заболеванию, а общее снижение сопротивляемости организма к стрессовым факторам, что делает его более уязвимым к различным негативным воздействиям [3, 4].
При рассмотрении предболезни в гериатрическом контексте необходимо учитывать несколько ключевых компонентов:
саркопения и динапения — возрастное уменьшение мышечной массы и силы, приводящее к ограничению подвижности, увеличению риска падений и ухудшению метаболических показателей;
старческая астения — синдром, характеризующийся повышенной уязвимостью к стрессовым факторам, снижением физиологических резервов и увеличением риска неблагоприятных исходов, таких как госпитализация, инвалидность и летальный исход;
когнитивные расстройства: умеренные когнитивные нарушения представляют собой переходную стадию между нормальным старением и деменцией. Они характеризуются субъективными или объективными когнитивными дефицитами, не оказывающими существенного влияния на повседневную жизнь;
сенсорные дефициты: нарушения зрения и слуха, ухудшающие коммуникацию, повышающие риск падений и социальной изоляции;
полиморбидность — наличие нескольких хронических заболеваний, усугубляющих течение друг друга и затрудняющих лечение;
психологические факторы: депрессия, тревога и социальная изоляция, оказывающие негативное влияние на физическое здоровье и функциональный статус [5–8].
Выявление предболезни требует комплексного гериатрического обследования, включающего:
сбор анамнеза (подробный опрос о жалобах, перенесенных заболеваниях, принимаемых лекарствах, образе жизни и социальном окружении);
физикальный осмотр (оценка физического состояния, включая измерение роста, массы тела, артериального давления, частоты сердечных сокращений и дыхания);
оценка функционального статуса (использование стандартизированных шкал и тестов для оценки способности пациента выполнять повседневные действия и инструментальные виды деятельности);
когнитивное тестирование (проведение скрининговых тестов для оценки когнитивных функций, таких как память, внимание и исполнительные функции);
оценка психологического состояния (использование опросников и шкал для выявления симптомов депрессии, тревоги и социальной изоляции);
лабораторные исследования (проведение общего и биохимического анализа крови, клинического анализа мочи, а также определение уровня витамина D и микроэлементов);
инструментальные методы исследования (электрокардиография (ЭКГ), рентгенография грудной клетки, ультразвуковое исследование внутренних органов, денситометрия).
Основная цель вмешательств при предболезни — замедлить прогрессирование возрастных изменений, улучшить функциональный статус, предотвратить развитие хронических заболеваний и улучшить качество жизни. Стратегии профилактики и лечения предболезни должны быть индивидуальными и учитывать особенности каждого пациента [9–12].
Концепция предболезни является перспективным направлением в гериатрии, позволяющим выявлять пожилых людей с высоким риском развития неблагоприятных исходов и разрабатывать индивидуализированные стратегии профилактики и лечения. Однако существует ряд проблем, связанных с внедрением этой концепции в клиническую практику [13–16].
Преодоление этих проблем позволит расширить возможности ранней диагностики и профилактики заболеваний в гериатрии, улучшить качество жизни пожилых людей и увеличить продолжительность активного долголетия [17]. В конечном итоге акцент на предболезни станет важным шагом на пути к более здоровому и благополучному старению населения.
Цель исследования: провести клинико-социальное исследование женщин с предшествующими заболеваниями и состояниями, которые могут быть включены в геронтологические профилактические программы, и выявить возраст начала предболезненных состояний и самих заболеваний, а также изучить соотношение между биологическим и календарным возрастом на момент их проявления.
Материал и методы
В исследовании приняли участие женщины в возрасте от 40 до 70 лет. Были сформированы исследовательские группы, распределенные по возрасту: 40–44 года (n=102), 45–49 лет (n=104), 50–54 года (n=101), 55–59 лет (n=108), 60–64 года (n=105), 65–69 лет (n=103) и 70–75 лет (n=104).
Анализируемые параметры включали: характеристики физического здоровья: антропометрические показатели (рост, масса тела, индекс массы тела, отношение окружности талии к окружности бедер), систолическое и диастолическое артериальное давление (АД), частота сердечных сокращений, общий анализ крови, отношение нейтрофилов к лимфоцитам (NLR) и отношение тромбоцитов к лимфоцитам (PLR); биохимические показатели (гликированный гемоглобин, уровень глюкозы, амилаза, общий белок, мочевина, аспартатаминотрансфераза, аланинаминотрансфераза, кальций, билирубин, тиреотропный гормон, триглицериды, общий холестерин, липопротеины низкой плотности, креатинин, мочевая кислота, цистатин С, высокочувствительный С-реактивный белок (СРБ), омега-3 полиненасыщенные жирные кислоты, лептин, гомоцистеин, N-терминальный фрагмент промозгового натрийуретического пептида (NT-proBNP), витамин D); скорость клубочковой фильтрации; параметры эхокардиографии (конечно-систолический объем, конечно-диастолический объем, фракция выброса, индекс массы миокарда левого желудочка, пик Е, пик А, соотношение Е/А, E/e’); показатели, полученные с использованием программного обеспечения «Кардиовизор» (состояние миокарда, альтернирующий характер зубца T, характеристика ритма); средняя взвешенная вариация ритмограммы (СВВР) при суточном мониторинге ЭКГ; текущая медикаментозная терапия; параметры опорно-двигательной системы: результаты оценки по шкале FRAIL (оценка слабости у пожилых людей), шкале Катца (оценка повседневной активности), динамометрии силы кисти, данные опросника SARC-F (оценка способности человека самостоятельно выполнять основные действия повседневной жизни), показатели биоимпедансометрии (фактический и биологический возраст), параметры сенсорной системы — результаты комплексного офтальмологического обследования, когнитивной системы — результаты теста MMSE (краткий тест для оценки когнитивных функций (память, внимание, ориентация, речь), психологической — данные оценки по шкале Бека и ШАС (тревоги и астенических состояний), нутритивной — результаты краткой оценки пищевого статуса (MNA — краткий опросник для оценки риска недоедания у пожилых людей).
Для измерения АД использовался тонометр Omron M2 (Omron Healthcare, Япония). Прегипертензия, иногда называемая повышенным нормальным АД или пограничной гипертонией, характеризуется показателями систолического АД в диапазоне от 130 до 139 мм рт. ст. и диастолического АД между 85 и 89 мм рт. ст.
Эхокардиографическое обследование выполнялось всем участникам исследования на ультразвуковом аппарате Toshiba Aplio 500 (Canon, Япония).
Предстадия хронической сердечной недостаточности (ХСН) — состояние, при котором отсутствуют симптомы и признаки ХСН в настоящем и прошлом, но есть признаки структурного и/или функционального поражения сердца и/или повышения уровня NT-proBNP.
Для оценки функционального состояния сердечно-сосудистой системы использовалась программа «Кардиовизор» («Салюсмед», Россия), обеспечивающая оперативную оценку активности сердца на базе данных ЭКГ, зарегистрированных с конечностей (стандартные отведения). Данная программа позволяет быстро идентифицировать отклонения, потенциально свидетельствующие о развитии патологий. Полученные в ходе исследования индексы «Миокард» и «Ритм» являются относительными показателями, отражающими общее количество отклонений от нормы и варьирующимися в интервале от 0 до 100%.
Вариабельность сердечного ритма оценивалась при помощи аппарата «Холтер-ДМС» («ДМС Передовые технологии», Россия).
Показатель NLR определялся на основании абсолютных значений числа нейтрофилов (N; ×109/л) и лимфоцитов (L; ×109/л) по формуле: NLR = N / L. Показатель PLR = тромбоциты (Р; ×109/л) / L.
Уровень гликированного гемоглобина определялся методом высокоэффективной жидкостной хроматографии с применением автоматизированной системы ионного обмена, а концентрация СРБ измерялась спектрофотометрическим методом.
Предиабет — это нарушение углеводного обмена, при котором не достигаются критерии сахарного диабета (СД), но превышены нормальные значения глюкозы крови (в интервале 6,0–6,4%).
Для оценки уровня омега-3 ненасыщенных кислот использовался образец цельной венозной крови, полученный утром натощак в специальную пробирку. В течение получаса после взятия кровь центрифугировалась при 2800 об./мин в течение 10 мин при 4 °C. После извлечения плазмы и слоя лейкоцитов эритроциты замораживались и хранились при -80 °C до момента проведения анализа в соответствии с известными протоколами. Измерялось содержание следующих жирных кислот: α-линоленовой, эйкозапентаеновой, докозагексаеновой, линолевой, гамма-линоленовой, дигомо-гамма-линоленовой, арахидоновой, докозатриеновой и докозапентаеновой.
Оценка двигательной функции, в частности наличие синдрома старческой астении, осуществлялась с помощью шкалы FRAIL, включающей пять вопросов, касающихся утомляемости, уровня физической активности, мобильности, наличия сопутствующих заболеваний и потери массы тела. Оценки варьировались от 0 до 5, где 3–5 баллов свидетельствовали о наличии синдрома, а 1–2 балла — о состоянии преастении. Функциональная активность оценивалась с использованием 6-балльной шкалы активности в повседневной жизни по шкале Катца (минимальное значение — 0 баллов, максимальное — 6 баллов).
Для оценки нутритивного статуса применялась полная версия Мини-оценки питания (MNA). Результат MNA ≥23,5 указывал на отсутствие риска недостаточного питания, результат MNA в диапазоне 17–23,5 свидетельствовал о риске развития дефицита питания, а результат MNA <17 баллов указывал на наличие недостаточного питания.
Силу мыщц определяли измерением силы сжатия кисти с помощью аналогового динамометра «МЕГЕОН 04010» («Мегеон», Россия). Оценка объема скелетной мускулатуры осуществлялась методом биоимпедансного анализа на аппарате ACCUNIQ (ACCUNIQ, Южная Корея).
Пресаркопения — это стадия саркопении, при которой уменьшается мышечная масса, а мышечная сила и функция пока остаются неизменными.
Для анализа сенсорных возможностей проводилось комплексное офтальмологическое обследование, включающее детальную оценку состояния сетчатки с использованием цифровой камеры Topcon TRC NW6s (Япония) с разрешением 3872×2892 пикселя, биомикроскопическое исследование с применением щелевой лампы и офтальмоскопию. Дополнительно выполнялась оптическая когерентная томография-ангиография (RTVue XP, Optovue, США).
Оценка психологического статуса проводилась с использованием шкалы Бека (для оценки депрессии, тревоги), а определение возрастной жизнеспособности — шкалы астенических состояний.
Статистическая обработка полученных данных проводилась с применением программного пакета StatTech версии 4.8.0 (ООО «Статтех», Россия). Проверка соответствия распределения количественных параметров нормальному закону проводилась с использованием критерия Колмогорова — Смирнова. Для количественных переменных, имеющих нормальное распределение, приводились средние значения (M) и стандартные отклонения (SD). Для оценки точности средних значений указывались границы 95-процентного доверительного интервала (95% ДИ). В случаях, когда распределение отличалось от нормального, количественные характеристики представлялись в виде медианы (Me) и интерквартильного размаха (Q1–Q3). Категориальные переменные описывались путем указания абсолютных и относительных частот. Для определения 95% ДИ пропорций использовался метод Клоппера — Пирсона.
Результаты и обсуждение
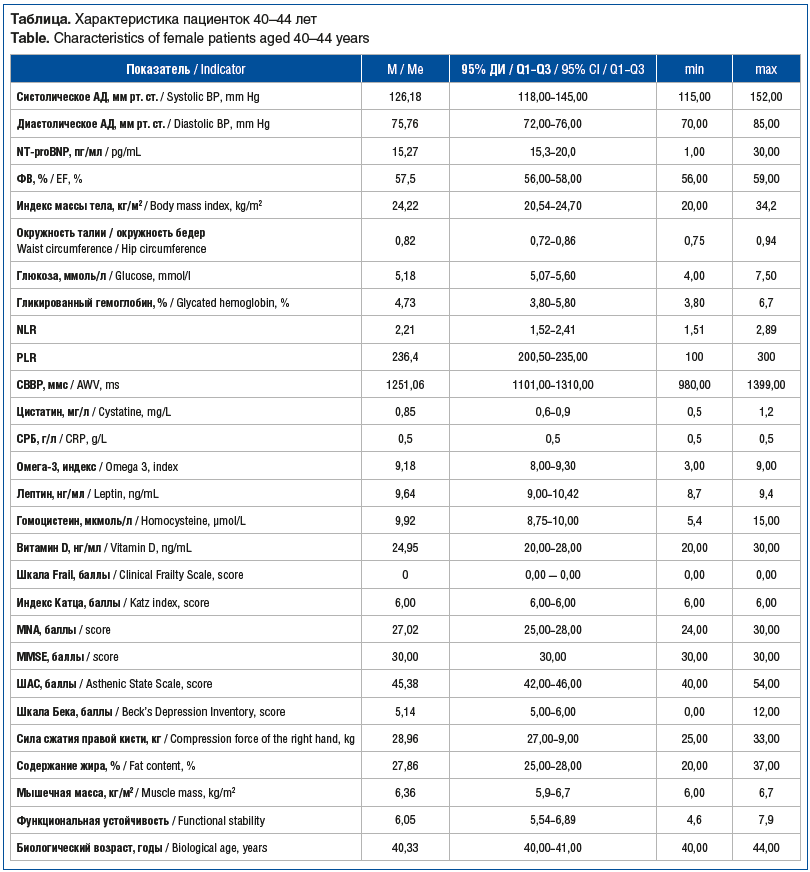
Анализ представленных данных позволяет выделить ряд факторов, потенциально оказывающих влияние на состояние здоровья обследованной группы. Рассмотрим на примере женщин 40 лет (см. таблицу).

Спазм аккомодации имеет тенденцию к уменьшению с годами, вероятно, из-за естественных изменений в аккомодационном аппарате глаза (в 40–44 года — 3%, в 50–54 года — -8%, в 65–69 лет — 0%). Глаукома и катаракта, напротив, обнаруживают выраженную зависимость от возраста, что соответствует общепринятым представлениям об эпидемиологии данных болезней (с 55–59 лет — 5% глаукомы и 6% катаракты, к 70 годам и старше процент возрастает до 36 и 12% соответственно).
Прегипертензия достаточно часто встречается в возрасте 40–44 лет (17–20%), снижаясь с возрастом и практически не выявляясь к 60 годам. Встречаемость артериальной гипертензии (АГ) постепенно растет, составляя в 40–44 лет 6%, в 45–49 лет — 15%, в 50–54 года — 31%, в 70 лет и старше — 64%, т. е. демонстрирует увеличение распространенности с возрастом, что отражает общемировые тенденции роста сердечно-сосудистых заболеваний среди пожилого населения.
ПреХСН выявляется в 45 лет у 3% женщин, увеличивается к 55 годам до 25%, а к 60 годам составляет всего 6%, в то время как клинически выраженная ХСН начинает встречаться с 50 лет в 3% случаев, а в 60 лет уже в 49% случаев.
Избыточная масса тела чаще наблюдается у женщин в 40–44 года — 23%, в 45–49 лет — 18%, снижаясь с возрастом и не встречаясь к 55 годам, а ожирение в 40–44 года выявлено у 8% женщин, а в 65–69 лет — у 62%, т. е. увеличивается в старших возрастных группах.
При рассмотрении показателей предиабета и СД 2 типа (СД2) отмечается их значительный рост с увеличением возраста, что подчеркивает важность своевременной диагностики и профилактики этих заболеваний. Так, предиабет встречается в 40–44 года в 12% случаев, а в 55–59 лет — в 5%, в то время как СД2 растет постепенно и к 55–59 годам встречается у 27% женщин с ожирением, а в 60–64 года — у 59%.
Возрастная забывчивость также становится все более распространенной с возрастом, выявляясь с 55–59 лет в 4%, а к 60–64 годам возникают легкие когнитивные нарушения у 28% женщин. Однако деменция, хотя и встречается, не демонстрирует столь выраженного увеличения, возможно, из-за сложности диагностики на ранних стадиях (в 70 лет — 5%).
Астения (5% в 40–44 года, 66% в 70 лет) и депрессия (9% в 40–44 года, 66% в 70 лет), часто сопровождающие пожилой возраст, также демонстрируют тенденцию к росту с возрастом, что указывает на необходимость комплексного подхода к поддержанию психического здоровья пожилых людей (рис. 1).

В целом представленные данные подчеркивают важность целостного подхода к оценке здоровья людей старшего возраста, учитывающего как физическое, так и психическое благополучие, а также необходимость разработки и внедрения действенных программ профилактики и терапии заболеваний, ассоциированных со старением.
Определение возраста начала болезней на основе представленных данных — сложная задача, требующая учитывать множество факторов. Количественная оценка отклонений от фактического возраста как важный показатель отражает суммарное воздействие различных болезненных состояний на организм. Высокие значения этого показателя в каждой возрастной категории указывают на существенное расхождение между биологическим и паспортным возрастом, обусловленное наличием сопутствующих патологий и предрасполагающих факторов.
Отсутствие глаукомы и катаракты в молодых возрастных группах сменяется увеличением их распространенности с годами, что отражает естественный процесс старения и накопления возрастных изменений в органах зрения.
Прегипертензия и АГ, в свою очередь, демонстрируют постепенное повышение частоты встречаемости с возрастом, подтверждая их тесную взаимосвязь с возрастными изменениями в сердечно-сосудистой системе.
Предстадия ХСН и клиническая ХСН как проявления дисфункции сердца также демонстрируют тенденцию к увеличению с возрастом, что свидетельствует о постепенном снижении функциональных резервов сердечной мышцы.
Избыточная масса тела и ожирение, являющиеся факторами риска развития многих заболеваний, также характеризуются высокой распространенностью в каждой возрастной группе, что подчеркивает важность борьбы с избыточным весом и поддержания здорового образа жизни.
Предсаркопения и саркопения как признаки возрастной потери мышечной массы начинают проявляться в более позднем возрасте, что отражает естественный процесс старения и уменьшения анаболических процессов в организме. Данные состояния выявлены у 28,84 и 25% участников исследования соответственно, что подчеркивает проблему потери мышечной массы и силы в возрасте 70 лет.
Предиабет и СД2, напротив, показывают рост распространенности с возрастом, что подтверждает их тесную связь с возрастными изменениями в метаболизме глюкозы.
Возрастная забывчивость и деменция как признаки когнитивных нарушений также чаще встречаются в старшем возрасте, что отражает естественное старение головного мозга.
Астения и депрессия, в свою очередь, характеризуются высокой распространенностью в каждой возрастной группе, что подчеркивает необходимость комплексной оценки состояния здоровья и учета психоэмоциональных факторов.
У лиц в возрасте 40–44 лет медиана NT-proBNP составляет 15,27 пг/мл (95% ДИ 15,3–20,0), что соответствует нижней границе референтных значений для этой возрастной категории. К 45–49 годам наблюдается более чем двукратное увеличение уровня NT-proBNP, достигающего медианы в 34,60 пг/мл (95% ДИ 15,00–49,25; p<0,05). В 50–54 года концентрация данного пептида продолжает нарастать, достигая медианного значения 46,74 пг/мл (95% ДИ 15,00–69,25; p<0,05). К 55–59 годам отмечается дальнейший рост уровня NT-proBNP, его медиана составляет 59,75 пг/мл, что может отражать прогрессирующие изменения в миокарде. У пациентов 60–64 лет наблюдается существенное повышение концентрации NT-proBNP, медиана достигает 131,67 пг/мл (95% ДИ 130,0–133,0), что может свидетельствовать о развитии ХСН или других кардиоваскулярных заболеваний. В 65–69 лет и 70 лет уровень NT-proBNP продолжает увеличиваться, достигая медианных значений 153,55 пг/мл (95% ДИ 90,0–160,0) и 178,61 пг/мл (95% ДИ 46,50–261,50) соответственно (p<0,05). Представленные результаты акцентируют внимание на важности учета возрастных особенностей при интерпретации результатов анализа NT-proBNP.
В рамках комплексного исследования процессов старения представляется важным анализ отклонений биологического возраста от фактического, или хронологического. Данное отклонение позволяет оценить индивидуальную скорость старения и выявить группы лиц, демонстрирующих ускоренное или замедленное старение. Представленная ниже диаграмма (рис. 2) иллюстрирует распределение лиц разного хронологического возраста в зависимости от степени отклонения их биологического возраста от фактического. Рассматриваются две градации отклонений: умеренное отклонение (1–2 года) и значительное отклонение (3 года и более). Представленные данные демонстрируют интересные закономерности в динамике отклонений биологического возраста. В возрастной группе 40–44 лет наблюдается относительно равномерное распределение между умеренным и значительным отклонениями. Однако уже в группе 45–49 лет картина меняется: количество лиц с умеренным отклонением значительно преобладает над количеством лиц с отклонением в 3 года и более. Это может указывать на то, что в данной возрастной группе большинство индивидуумов демонстрируют относительно «нормальное» старение. Начиная с 50–54 лет наблюдается резкое увеличение количества лиц с отклонением биологического возраста на 3 года и более. Эта тенденция усиливается с возрастом: в группах 60–64, 65–69 и 70 лет и старше практически все обследованные демонстрируют значительное отклонение биологического возраста от фактического. Отсутствие лиц с умеренным отклонением биологического возраста в старших возрастных группах подчеркивает нарастающий характер расхождений между биологическим и хронологическим возрастом.

Заключение
Проведенный клинико-социальный анализ выявляет критические точки перехода от преморбидных состояний к манифестным заболеваниям у женщин в возрасте 40–70 лет. Очевидна необходимость разработки и внедрения персонализированных программ геронтологической профилактики, учитывающих индивидуальные риски и возрастные изменения. Тщательный мониторинг и своевременная коррекция факторов риска, особенно в периоды наиболее выраженных переходов (50–60 лет), могут существенно замедлить прогрессирование заболеваний и улучшить качество жизни.
Динамика отклонения биологического возраста от хронологического представляет собой ценный инструмент для оценки индивидуального темпа старения и прогнозирования рисков развития возраст-ассоциированных заболеваний. Выявленное ускорение старения после 50 лет подчеркивает важность активных профилактических мер в этой возрастной группе. Интеграция оценки биологического возраста в клиническую практику позволит более точно стратифицировать пациентов по степени риска и оптимизировать выбор медицинских вмешательств, приближая нас к эре персонализированной геронтологии.
Сведения об авторе:
Кочеткова Ирина Владимировна — к.м.н., доцент кафедры медицинской профилактики ФГБОУ ВО ВГМУ им. Н.Н. Бурденко Минздрава России; 394036, Россия, г. Воронеж, ул. Студенческая, д. 10; ORCID iD 0000-0002-7546-6679
Контактная информация: Кочеткова Ирина Владимировна, e-mail: iri4217@yandex.ru
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 21.05.2025.
Поступила после рецензирования 13.06.2025.
Принята в печать 08.07.2025.
About the author:
Irina B. Kochetkova — C. Sc. (Med.), Associate Professor of the Department of Otorhinolaryngology, N.N. Burdenko Voronezh State Medical University; 10, Studencheskaya str., Voronezh, 394036, Russian Federation; ORCID iD 0000-0002-7546-6679
Contact information: Irina B. Kochetkova, e-mail: iri4217@yandex.ru
Financial Disclosure: the author has no a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 21.05.2025.
Revised 13.06.2025.
Accepted 08.07.2025.