Введение
Частота встречаемости эктопической беременности увеличилась с 0,5% в конце ХХ в. до 1–2% в наши дни, когда данный показатель составляет 11 случаев на 1 тыс. беременностей, причем около 8% приходится на редкие формы [1]. Редкие нозологические формы эктопической беременности сопровождаются массивным кровотечением и нередко ассоциированы с летальным исходом, будучи одной из причин материнской смертности1. Шеечная беременность (ШБ) — очень редкая форма эктопической беременности, когда имплантация плодного яйца происходит в цервикальном канале. Частота ШБ составляет 0,1–0,4% от всех эктопических беременностей и ее распространенность находится в пределах 1 случая на 9–12 тыс. беременностей [2]. Ранняя диагностика ШБ позволяет применять мини-инвазивные органосохраняющие технологии лечения, предотвращая материнскую заболеваемость и смертность.
Факторами риска эктопической беременности, и в том числе ШБ, служат воспалительные заболевания органов малого таза, внутриматочные вмешательства, применение внутриматочных контрацептивов, лечение бесплодия методами вспомогательных репродуктивных технологий [3]. Эктопическую беременность отличает стертая клиническая картина и трудность своевременной диагностики, в связи с чем нередко происходит внезапное развитие летальных осложнений. Несмотря на то, что ШБ — редкая форма эктопической беременности, по данным российских публикаций, за последние 10 лет авторами проанализировано более 100 исходов лечения ШБ [2]. В зарубежной литературе опубликованы серии клинических случаев. Систематические обзоры либо метаанализы до настоящего времени отсутствуют [4–8]. Выбор объема оперативного лечения определяется клинической ситуацией и репродуктивными планами пациентки. А.В. Козаченко и соавт. [1], проанализировав 49 случаев ШБ, пришли к выводу, что цитостатическая терапия в сочетании с органосохраняющей операцией (эмболизация маточных артерий (ЭМА) и резектоскопическое удаление плодного яйца) — наиболее безопасный метод лечения, позволяющий избежать гистерэктомии и сохранить репродуктивную функцию женщины. При этом данные о реализации фертильности пациентками после органосохраняющего лечения ШБ в мировой литературе представлены в единственной публикации [9].
Представляем собственное клиническое наблюдение пациентки с ШБ. Согласие пациентки на публикацию данных в обезличенном виде получено.
Клиническое наблюдение
Пациентка О., 33 года, в 2016 г. обратилась в ООО КВРТ «ДИП» с целью реализации репродуктивной функции после потери предыдущей беременности. Гинекологический анамнез: менархе в 14 лет, менструации регулярные, по 4–5 дней через 28–30 дней, обычного характера, в 2016 г. по поводу полипа эндометрия выполнена гистерорезектоскопия, без осложнений (гистологически верифицирован фиброзный полип эндометрия). Акушерский анамнез: одна беременность в 2015 г. (замершая, в сроке 5–6 нед. — инструментальное опорожнение полости матки, без осложнений). По данным объективного обследования, индекс массы тела 31,2 кг/м2, варикозное расширение вен обеих голеней. Назначено обследование согласно действующему приказу Минздрава РФ2. Установлен клинический диагноз: эндометриоз матки 1-й степени. Хронический эндометрит. Нарушение жирового обмена 1-й степени. Варикозная болезнь вен нижних конечностей. Грыжа пояснично-крестцового отдела позвоночника.
Проведена прегравидарная подготовка в объеме: коррекция образа жизни и массы тела, дидрогестерон 20 мг/сут внутрь по схеме с 16-го по 25-й день менструального цикла (д.м.ц.), фолиевая кислота 400 мкг/сут внутрь ежедневно в течение 3 мес. [10].
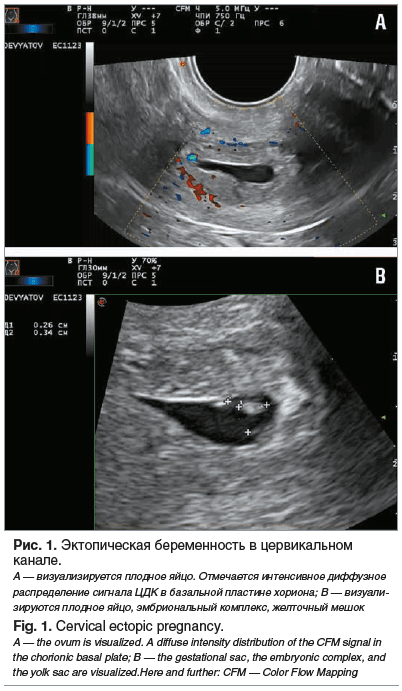
30.11.2016 пациентка обратилась в клинику с жалобами на задержку менструации 7 дней и положительным мочевым тестом на наличие β-субъединицы хорионического гонадотропина (β-ХГЧ), без признаков наружного кровотечения. Было выполнено УЗИ в В-режиме и в режиме цветового допплеровского картирования (ЦДК). По данным трансвагинального УЗИ органов малого таза: эхографические признаки прогрессирующей беременности в цервикальном канале. Размеры эмбриона соответствовали 5 нед. 6 дням гестации; определялось ритмичное сердцебиение 110 уд/мин (рис. 1).

Установлен клинический диагноз: прогрессирующая эктопическая беременность 5–6 нед., цервикальной локализации. Пациентка госпитализирована в ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России, где с 01.12.2016 по 14.12.2016 проведено комплексное высокотехнологичное органосохраняющее лечение в объеме: низкодозная полихимиотерапия (метотрексат внутривенно капельно по схеме, суммарная доза 200 мг, лейковорин внутримышечно по схеме, суммарная доза 24 мг) с последующей селективной ЭМА эмболами из гемостатической губки, резектоскопией, удалением плодного яйца из шейки матки, коагуляцией сосудов плодовместилища, лигированием шеечных ветвей маточных артерий и диагностическим выскабливанием слизистой полости матки. На фоне цитостатической терапии осложнений не было; хирургический этап также выполнен без осложнений. Кровопотеря составила 30 мл. Послеоперационный период (5 койко-дней) протекал без особенностей.
27.05.2017 на 21-й д.м.ц. с помощью УЗИ в В-режиме и режиме ЦДК проведена оценка эндометрия и перфузии матки. По данным УЗИ: рост эндометрия неравномерный, толщина 4–5 мм, распределение сигнала ЦДК в эндометрии отсутствовало (1 балл) (рис. 2) [11].

Установлен клинический диагноз: хронический атрофический эндометрит.
Далее в течение 15 мес. проводилось комплексное лечение, направленное на реабилитацию эндометрия, и прегравидарная подготовка [10]: циклическая гормональная терапия (комбинация эстрадиола 2 мг/сут и дидрогестерона 10 мг/сут внутрь по схеме), лечение для улучшения микроциркуляции включало антиагрегант (ацетилсалициловая кислота 100 мг/сут внутрь с 7-го по 20-й д.м.ц.) и гепариноид (сулодексид 500 ЛЕ/сут внутрь с 7-го по 28-й д.м.ц.); комбинированное физиотерапевтическое лечение, направленное на усиление регенерации и репарации эндометрия (переменное магнитное поле, низкочастотное лазерное излучение внутриматочно № 20).
27.12.2018 пациентка обратилась в клинику с жалобами на задержку менструации 5 дней и положительный мочевой тест на β-ХГЧ. По данным трансвагинального УЗИ диагностирована маточная беременность малого срока, I и II триместры беременности протекали без осложнений. В сроках 16–24 нед. выполняли УЗ-цервикометрию, длина шейки матки составляла более 30 мм. С учетом риска невынашивания превентивно назначен микронизированный прогестерон 200 мг/сут вагинально с ранних сроков и до 34 нед. гестации включительно, согласно действующему приказу Минздрава РФ2. Третий триместр осложнился отеками беременных с 34 нед. гестации с дородовым излитием вод в 35 нед. 31.07.2019 проведено родоразрешение путем операции кесарева сечения в 35 нед. гестации в тазовом предлежании в 36 лет. Кровопотеря составила 600 мл. Извлечена живая недоношенная девочка с массой тела 2600 г, длиной 51 см, с оценкой по шкале Апгар на 1-й минуте 8 баллов, на 5-й минуте 9 баллов. В удовлетворительном состоянии пациентка выписана домой с ребенком на 6-е сутки. По сведениям катамнеза, ребенок развивается в соответствии с возрастом.
Обсуждение
При оценке анамнеза пациенток с ШБ обращает на себя внимание наличие гинекологических заболеваний (эндометрит, миома, эндометриоз), гинекологических операций (гистероскопия, диагностические выскабливания слизистой полости матки, искусственное прерывание беременности на ранних сроках, оперативные вмешательства по поводу доброкачественных образований яичников, миомы матки, эндометриоза и спаечного процесса в малом тазу), отягощенного акушерского анамнеза (замершая беременность, кесарево сечение). Эта информация позволяет предположить ассоциацию вмешательств с травматизацией шейки матки, которая может быть важным фактором риска возникновения ШБ [1]. В нашем клиническом наблюдении у пациентки в анамнезе 2 внутриматочных вмешательства с расширением цервикального канала: 1) гистерорезектоскопия, полипэктомия; 2) инструментальное опорожнение полости матки при замершей беременности в сроке 5–6 нед.
Диагностика и тактика лечения ШБ претерпели колоссальные изменения за последние 20 лет. До 1980 г. диагноз устанавливали с большим опозданием, что вынуждало прибегать к гистерэктомии — единственно возможному варианту лечения для спасения жизни женщины. Развитие химиотерапии позволило уже не прибегать к гистерэктомии, а сохранять фертильность. Хирургические консервативные технологии также развивались. Сегодня они включают ЭМА с последующим бережным кюретажем цервикального канала, интрацервикальную баллонную тампонаду после кюретажа, наложение кругового компрессионного шва на шейку матки и локальную инъекцию простагландинов. Техника может включать также гистероскопическую резекцию, билатеральное лигирование маточных и гипогастральных артерий. ЭМА, лишенная серьезных ограничений хирургического и консервативного лечения, может стать методом выбора. Впервые J. Oliver et al. [12] с успехом применили ЭМА для остановки послеродовых и послеоперационных кровотечений. В 1991 г. J. Ravina [13] первым выполнил ЭМА в качестве планового предоперационного лечения, направленного на уменьшение объема кровопотери в ходе гистерэктомии или миомэктомии. В наши дни данная методика прочно вошла в перечень органосохраняющих вмешательств при миоме матки [14]. Для лечения ШБ с применением ЭМА в качестве основного метода сегодня предложены следующие варианты методик:
-
ЭМА + тампонада шейки матки баллонным катетером Фолея + инъекции метотрексата 1 мг/кг в сутки;
-
ЭМА желатиновой губкой + выскабливание цервикального канала;
-
ЭМА платиновыми спиралями + инъекции метотрексата.
Кроме того, ЭМА может использоваться после неудачных попыток применения метотрексата и лигирования сосудов [3]. Применение ангиохирургической селективной ЭМА у пациенток с признаками врастания хориона в строму шейки матки в сочетании с выраженным кровотоком в этой области обеспечивает минимальную интраоперационную кровопотерю и сохранение детородной функции [1]. Результаты этих исследований указывают на успешность комбинированного лечения ШБ с сохранением репродуктивной функции.
В современной научной литературе крайне мало работ, сообщающих об успешной реализации фертильности после органосохраняющего лечения ШБ. Опубликован лишь один систематический обзор, результаты которого сообщают, что лечение гинекологических заболеваний (миома матки) с помощью ЭМА ассоциировано с более низкой частотой наступления послеоперационной беременности и повышенным риском послеродовых кровотечений [15].
В описанном нами клиническом наблюдении успешно выполнено комплексное высокотехнологичное органосохраняющее лечение: полихимиотерапия с последующей селективной ЭМА эмболами из гемостатической губки, резектоскопией, удалением плодного яйца из шейки матки, коагуляцией сосудов плодовместилища, лигированием шеечных ветвей маточных артерий и диагностическим выскабливанием слизистой полости матки. Наступившая беременность протекала в целом благоприятно и осложнилась лишь в III триместре. В сроке 35 нед. гестации произошло излитие околоплодных вод, родоразрешение проведено путем операции кесарева сечения с учетом тазового предлежания плода при недоношенной беременности. Послеродовый период протекал без осложнений.
По нашему мнению, выбранная тактика при ведении данного клинического наблюдения является безопасным и эффективным методом лечения ШБ, позволила пациентке сохранить и реализовать детородную функцию в отсроченном периоде.
Заключение
Современный взгляд на оказание медицинской помощи пациенткам с ШБ заключается во внедрении в клиническую практику и использовании на всех этапах оптимального алгоритма обследования и лечения с применением высокотехнологичных методик. Результаты комплексного органосохраняющего подхода к лечению пациенток с ШБ демонстрируют высокую эффективность в сочетании с сохранением возможности реализации репродуктивной функции, что подтверждено описанным в данной статье клиническим наблюдением.
1Клинические рекомендации. Внематочная (эктопическая) беременность. 2021. (Электронный ресурс.) URL: https://cr.minzdrav.gov.ru/recomend/642_1 (дата обращения: 01.01.2024).
2Приказ Министерства здравоохранения РФ от 1 ноября 2012 г. № 572н «Об утверждении Порядка оказания медицинской помощи по профилю «акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)». (Электронный ресурс.) URL: https://base.garant.ru/70352632/ (дата обращения: 01.10.2024).
СВЕДЕНИЯ ОБ АВТОРАХ:
Вартанян Эмма Врамовна — д.м.н., доцент, профессор кафедры акушерства и гинекологии ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (Пироговский Университет); 117513, Россия, г. Москва, ул. Островитянова, д. 1, стр. 6; директор ООО КВРТ «ДИП»; 123182, Россия, г. Москва, ул. Щукинская, д. 2; президент саморегулируемого общества Ассоциация клиник ВРТ; ORCID iD 0000-0003-0337-086X
Кирющенков Петр Александрович — д.м.н., руководитель курса клинической гемостазиологии факультета повышения квалификации медицинских работников Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; акушер-гинеколог ООО КВРТ «ДИП»; 123182, Россия, г. Москва, ул. Щукинская, д. 2; ORCID iD 0009-0008-1459-8038
Козаченко Андрей Владимирович — д.м.н., ведущий научный сотрудник ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России; 117997, Россия, г. Москва, ул. Академика Опарина, д. 4; ORCID iD 0000-0001-5343-250X
Девятова Екатерина Александровна — к.м.н., заместитель главного врача, врач ультразвуковой диагностики, акушер-гинеколог ООО КВРТ «ДИП»; 123182, Россия, г. Москва, ул. Щукинская, д. 2; ORCID iD 0000-0003-1533-1593
Цатурова Кристина Ашотовна — к.м.н., ассистент кафедры акушерства и гинекологии ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России (Пироговский Университет); 117513, Россия, г. Москва, ул. Островитянова, д. 1, стр. 6; главный врач, акушер-гинеколог, репродуктолог ООО КВРТ «ДИП»; 123182, Россия, г. Москва, ул. Щукинская, д. 2; ORCID iD 0000-0002-1095-4700
Контактная информация: Девятова Екатерина Александровна, e-mail: devyatova@baby-ivf.ru
Прозрачность финансовой деятельности: авторы не имеют финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 25.01.2024.
Поступила после рецензирования 19.02.2024.
Принята в печать 18.03.2024.
ABOUT THE AUTHORS:
Emma V. Vartanyan — Dr. Sc. (Med.), Associate Professor, Professor of the Department of Obstetrics and Gynecology, Pirogov Russian National Research Medical University; 1, Ostovityanov str., Moscow, 117513, Russian Federation; IVF Clinic «DIP»; 2, Schukinskaya str., Moscow, 123182, Russian Federation; President of the Self-Regulatory Society «Association of ART Clinics»; ORCID iD 0000-0003-0337-086X
Peter A. Kiryushenkov — Dr. Sc. (Med.), Head of the Clinical Hemostasiology Course at the Faculty of Advanced Training of Medical Specialists; RUDN University; 6, Miklukho-Maklaya str., Moscow, 117198, Russian Federation; obstetrician-gynecologist, IVF Clinic «DIP»; 2, Schukinskaya str., Moscow, 123182, Russian Federation; ORCID iD 0009-0008-1459-8038
Andrey V. Kozachenko — Dr. Sc. (Med.), Leading Researcher at the V.I. Kulakov National Medical Research Center of Obstetrics, Gynecology and Perinatology; 4, Academician Oparin str., Moscow, 117997, Russian Federation; ORCID iD 0000-0001-5343-250X
Ekaterina A. Devyatova — C. Sc. (Med.), Deputy Chief Medical Officer, ultrasound physician, obstetrician-gynecologist, IVF Clinic «DIP»; 2, Schukinskaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0003-1533-1593
Kristina A. Tsaturova — C. Sc. (Med.), Assistant Professor at the Department of Obstetrics and Gynecology, Pirogov Russian National Research Medical University; 1, Ostovityanov str., Moscow, 117513, Russian Federation; IVF Clinic «DIP»; 2, Schukinskaya str., Moscow, 123182, Russian Federation; Chief Medical Officer, obstetrician-gynecologist, fertility specialist, IVF Clinic «DIP»; 2, Schukinskaya str., Moscow, 123182, Russian Federation; ORCID iD 0000-0002-1095-4700
Contact information: Ekaterina A. Devyatova, e-mail: devyatova@baby-ivf.ru
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 25.01.2024.
Revised 19.02.2024.
Accepted 18.03.2024.