Введение
Острые респираторные вирусные инфекции (ОРВИ) представляют наиболее частые инфекционные заболевания в детском возрасте, на долю которых приходится 75–90% всех острых инфекционных болезней у детей [1].
По данным проспективного исследования [3], у детей 0–2 лет общая заболеваемость респираторными вирусами составляет 9,4 эпизода на ребенка в год, из которых лишь 37% проявляются клинически: 3,3 случая ОРВИ (95% доверительный интервал 3,01–3,50). Этиологический спектр [2]: риновирусы/энтеровирусы лидируют — 31% детекций, за ними следуют респираторно-синцитиальный вирус (РСВ) (17%), вирус парагриппа (6,5%), аденовирусы (5,4%). Заболеваемость риновирусами достигает 6,42, бокавирусами — 1,19, коронавирусами — 0,87 [3]. Заболеваемость РСВ в популяции составляет 0,46 эпизода на ребенка в год, при этом 73% инфекций проявляются клинически, а госпитализация требуется в 2,4% случаев [4]. Глобальное бремя РСВ у детей до 5 лет оценивается в 33 млн эпизодов и 101 400 смертей ежегодно, причем 97% из них приходятся на развивающиеся страны [5].
Однако наиболее актуальной клинической проблемой в амбулаторной практике врача-педиатра является категория часто болеющих детей (ЧБД). Распространенность ЧБД в популяции достигает 15–30% детского населения в развитых странах и представляет серьезный вызов для первичного звена здравоохранения [6, 7].
Формирование фенотипа ЧБД связано не только с частотой экспозиции к респираторным вирусам (что может быть обусловлено посещением детского сада или социальными факторами), но и, что наиболее существенно, с первичными и вторичными нарушениями иммунной системы, дисбиозом микробиома верхних дыхательных путей (ВДП) и активацией латентных герпесвирусных инфекций (ГВИ) [8].
Цель работы: провести анализ научной литературы по вопросам диагностики и лечения ОРВИ у детей.
Проведен аналитический обзор научной литературы из международных баз данных PubMed, реестров клинических испытаний ClinicalTrials.gov, Cochrane Library, а также русскоязычной базы eLibrary.
Критерии включения: работы, опубликованные в период 2000–2025 гг.; рандомизированные контролируемые исследования, метаанализы, систематические обзоры; клинические наблюдения и когортные исследования с достаточной выборкой (n≥30); обсуждение диагностики, лечения, профилактики ОРВИ или ГВИ у детей; исследования, посвященные микробиому, иммунитету и дисбиозу ВДП.
Результаты
Острые респираторные вирусные инфекции остаются одной из наиболее актуальных проблем педиатрии, особенно у ЧБД с нарушениями микробиома ВДП и активацией латентных ГВИ. ОРВИ являются наиболее распространенным предиктором развития острого воспаления околоносовых пазух и среднего уха, а также способствуют реактивации персистирующих патологических процессов в ВДП и барабанной полости1 [8].
Своевременное и целенаправленное лечение ОРВИ у ЧБД обеспечивает профилактику развития гнойно-воспалительных осложнений ЛОР-органов и тем самым предотвращает частое назначение антибиотиков, сохраняя микробиом. Такая тактика является оправданной с учетом того, что у ЧБД и без того имеются значительные нарушения микробиома как кишечника, так и других локусов, в том числе и ВДП.
Микробиом ВДП у ЧБД
Нормальный микробиом ВДП детей характеризуется доминированием нескольких филумов комменсальных бактерий: Firmicutes (основной филум), Proteobacteria, Actinobacteria, Bacteroidetes и Fusobacteria [9]. В пределах этого профильного распределения преобладающими родами служат Moraxella, Haemophilus, Streptococcus, Flavobacterium, Corynebacterium и Neisseria [10, 11]. Однако у ЧБД развивается характерный дисбиоз, при котором происходит селективное разрастание условно-патогенной флоры, в частности Staphylococcus aureus (выявляется в 41,6% случаев), Streptococcus pneumoniae (30,3%), Haemophilus parainfluenzae, Haemophilus parahaemolyticus, различные виды Gemella, Streptococcus intermedius и Streptococcus agalactiae [10–12].
Более того, было установлено, что респираторные вирусные инфекции непосредственно ассоциированы с формированием дисбиоза назального микробиома путем дополнительного угнетения защитных механизмов местного иммунитета, включая снижение продукции неспецифических факторов местной защиты и муцинов. В независимых исследованиях микробиоты ВДП и кишечника у ЧБД обнаружена корреляция между дисбиозом кишечника (выявлен у 67,6% детей) и изменениями в микробиоте ВДП, а также установлена высокая корреляционная связь между дисбиозом и уровнем секреторного иммуноглобулина A (sIgA) в слюне [10, 11].
Не только наличие дисбиоза кишечника способствует развитию осложнений на фоне ОРВИ у детей. Весомый вклад в нарушение иммунного ответа слизистых ВДП вносит персистирующая ГВИ: вирус Эпштейна — Барр (ВЭБ), цитомегаловирус (ЦМВ), вирус герпеса 6-го типа (ВГЧ-6). Они могут существовать в организме человека в виде моноинфекции или сочетаться друг с другом, что довольно часто встречается в популяции ЧБД [13].
Герпесвирусные инфекции в патогенезе рецидивирующих ОРВИ
В последние годы накопились убедительные данные о критической роли герпесвирусов в формировании рецидивирующих респираторных инфекций у детей. Комплексное микробиологическое и иммунологическое обследование 1120 детей с симптомами ОРВИ выявило активные ГВИ у 26,5% пациентов. Из них наиболее часто обнаруживались ВГЧ-6, ВЭБ и ЦМВ в различных комбинациях. Ключевое патофизиологическое значение герпесвирусов состоит в их способности вызывать иммуносупрессию: после инфицирования они блокируют экспрессию молекул главного комплекса гистосовместимости I класса (major histocompatibility complex, MHC I), что нарушает презентацию антигенов и приводит к снижению активности цитотоксического ответа, блокируют апоптоз инфицированных клеток, продукцию IFN и других цитокинов и активируют регуляторные T-клетки, которые подавляют противовирусный иммунный ответ. Эта вирус-обусловленная иммуносупрессия создает благоприятный фон для присоединения вторичных вирусных и бактериальных инфекций, трансформируя простую острую респираторную инфекцию в сложное полимикробное заболевание [8, 14]. Так, по данным А.С. Левиной и соавт. [15], хроническая ГВИ была диагностирована у 73% из 33 обследованных ЧБД, причем превалировал ВЭБ, а также его сочетание с ЦВМ и ВГЧ-6.
Спектр возбудителей ОРВИ и сезонность
Этиологическая структура ОРВИ варьирует в зависимости от сезона, географического региона и возрастной группы. В настоящее время до трети эпизодов ОРВИ у детей протекают как смешанные вирусные инфекции, когда ребенок последовательно или одновременно заражается несколькими респираторными вирусами, что заметно влияет на клиническое течение заболевания [16, 17].
По данным международного исследования [18], у детей в возрасте 6 мес – 10 лет с гриппоподобным заболеванием частота выявления РСВ составляет 9,7%, а инцидентность РСВ-ассоциированных эпизодов — 7,0 на 100 ребенко-лет. В китайском исследовании (2018–2023) у пациентов всех возрастов с ОРИ наиболее часто обнаруживали вирусы парагриппа (21,3%), гриппа B (17,3%) и гриппа A (9,9%); дети 4–6 лет были наиболее уязвимы [19].
Механизмы врожденного иммунитета и их нарушение при ОРВИ
Естественная защита ВДП от респираторных вирусов обеспечивается многоуровневой системой врожденного иммунитета, включающей:
-
физический барьер: мукоцилиарный клиренс, слизь, содержащую лизоцим, лактоферрин, пероксидазу;
-
врожденные рецепторы: toll-like receptors (TLR), nucleotide-binding oligomerization domain-like receptors (NOD-like), retinoic acid-inducible gene I (RIG-I), которые распознают вирусные паттерны;
-
цитокины врожденного иммунитета: интерфероны (IFN) I типа (IFN-α, IFN-β), интерлейкины (IL) 1β, 6, фактор некроза опухоли α (TNF-α);
-
клеточные компоненты: натуральные киллеры (NK-клетки), дендритные клетки [20, 21].
Интерфероны I типа, индуцируемые при распознавании вирусных РНК, служат ключевыми молекулами врожденного противовирусного ответа. Они активируют передачу сигнала через пути JAK-STAT и MAPK, приводя к экспрессии интерферон-стимулируемых генов, которые кодируют белки, обладающие прямой противовирусной активностью (2′,5′-олигоаденилатсинтетаза, протеинкиназа R и белок MxA) [22, 23].
У ЧБД наблюдаются дефекты в продукции эндогенного IFN, что может быть обусловлено как первичными генетическими дефектами (например, мутации в генах IFNAR, STAT1, TLR3), так и вторичными факторами, такими как микробиом-обусловленное снижение выработки провоспалительных цитокинов комменсальными микроорганизмами [24, 25].
Роль микробиома в формировании локального иммунитета
Комменсальный микробиом ВДП играет фундаментальную роль в обучении и модуляции местного иммунитета [9–11].
Нормальная микробиота:
-
конкурирует с патогенными микроорганизмами за питательные вещества и адгезины (колонизационная резистентность);
-
продуцирует противомикробные метаболиты и бактериоцины;
-
стимулирует выработку слизистыми клетками защитных секреторных компонентов (sIgA, лизоцима, лактоферрина);
-
активирует врожденные лимфоидные клетки (ILC) и регуляторные T-клетки (Tregs), способствуя толерантности и противовоспалительному микроокружению.
Дисбиоз, характеризующийся доминированием условно-патогенных штаммов и снижением видового разнообразия, нарушает эти защитные функции. Установлено, что дисбиоз ВДП и кишечника коррелирует со снижением уровня sIgA в слюне, который служит первой линией защиты мукозальной поверхности. Таким образом, восстановление нормального микробиома является важной составляющей стратегии профилактики рецидивирующих инфекций [26].
Клиническая картина и критерии тяжести
Неосложненная ОРВИ классически проявляется постепенным началом с преобладанием катаральных симптомов (ринорея, назальная обструкция, кашель, боль в горле) в течение 3–7 дней, сопровождаемых субфебрильной или фебрильной лихорадкой (38–39 °C) и общими симптомами интоксикации (утомляемость, отсутствие аппетита, артралгии). У детей первых лет жизни ОРВИ может протекать тяжелее с риском развития обструктивного ларингита, бронхиолита или пневмонии, особенно при наличии преморбидных факторов риска (недоношенность, дисплазия бронхолегочной ткани, врожденные пороки сердца) [2].
В клинических рекомендациях стран СНГ и ЕАЭС по диагностике и лечению ОРВИ у детей [27] выделяют 3 степени тяжести заболевания: легкую: симптомы ограничены ВДП, нет признаков интоксикации, температура ≤38,5 °C; среднетяжелую: катаральные явления + признаки интоксикации (вялость, утомляемость), температура 38,5–39,5 °C; тяжелую: выраженная интоксикация, поражение нижних отделов респираторного тракта, температура >39,5 °C, риск осложнений.
Клиническая диагностика и дифференцирование от бактериальных инфекций
Диагностика неосложненной ОРВИ основана на клинических признаках, анамнезе и эпидемиологическом контексте и не требует лабораторного подтверждения в большинстве амбулаторных случаев [28].
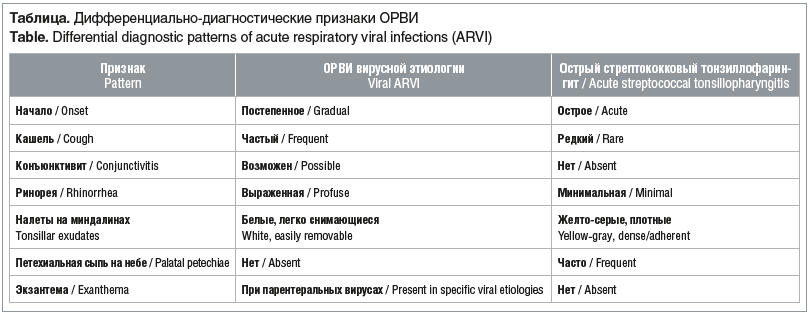
Ключевые клинические особенности, отличающие вирусную инфекцию от первичной бактериальной (стрептококковой) инфекции, представлены в таблице.

Лабораторное подтверждение (ПЦР, экспресс-тесты) показано в следующих случаях [29]:
-
пациенты в критическом состоянии (для исключения осложнений);
-
подозрение на грипп (особенно для назначения ингибиторов нейраминидазы);
-
скрининг в стационаре и домах престарелых;
-
исследовательские цели и эпидемиологический надзор.
Алгоритм ведения ребенка с ОРВИ можно представить следующим образом.
1. Первичный осмотр (амбулаторный прием / осмотр на дому)
→ перейти к оценке тяжести состояния.
2. Оценка тяжести и решение о госпитализации
a. Спросить и осмотреть на предмет «опасных признаков»:
ребенок не может пить / сосать грудь;
выраженная сонливость, отсутствие контакта;
выраженное затрудненное дыхание, признаки дыхательной недостаточности.
b. Если есть ≥1 опасный признак: → РЕКОМЕНДОВАТЬ ГОСПИТАЛИЗАЦИЮ (вызов СМП / направление в стационар).
c. Если опасных признаков нет: → продолжить амбулаторное ведение и перейти к клинической диагностике ОРВИ.
3. Клиническая диагностика ОРВИ
Оценить типичность картины ОРВИ:
-
постепенное начало болезни;
-
преобладают катаральные симптомы: ринорея, кашель, боль в горле;
-
повышение температуры тела;
-
нет выраженной общей интоксикации, ребенок сохраняет активность.
Если критерии выполняются: → установить диагноз: ОРИ (предположительно вирусная этиология).
Параллельно: исключить признаки локальных осложнений (отит, синусит, пневмония и др.) по действующим клиническим рекомендациям.
4. Исключение бактериального фарингита (стрептококковой инфекции)
Оценить наличие признаков, типичных для бактериального фарингита:
-
острое (часто внезапное) начало, высокая температура;
-
интенсивная боль в горле, затруднение глотания;
-
налеты на миндалинах, увеличенные и болезненные шейные лимфоузлы;
-
отсутствие кашля, ринореи, конъюнктивита.
Если клиника соответствует бактериальному поражению: → предположить стрептококковый фарингит,
→ рекомендовать экспресс‑тест на стрептококк (стрептотест) и/или назначение системного антибиотика в соответствии с клиническими рекомендациями.
Если картина не типична для бактериального фарингита:→ продолжаем терапию, как при неосложненной вирусной ОРВИ.
5. Оценка статуса «часто болеющего ребенка»
Уточнить частоту эпизодов ОРВИ за последний год с учетом возраста:
-
до 1 года: ≥4 эпизодов ОРВИ в год;
-
1–3 года: ≥6 эпизодов ОРВИ в год;
-
4–5 лет: ≥5 эпизодов ОРВИ в год;
-
старше 5 лет: ≥4 эпизодов ОРВИ в год.
a. Если частота выше возрастных пороговых значений:
-
присваиваем статус «часто болеющий ребенок»;
-
планируем углубленное обследование (иммунный статус, ЛОР‑патология, очаги хронической инфекции и др.);
-
включаем ребенка в группу риска и обсуждаем вопросы длительной системной иммуномодулирующей терапии (с опорой на клинические рекомендации и доказательную базу).
b. Если критерии ЧБД не выполняются:
-
ведем ребенка как стандартный случай неосложненной ОРВИ;
-
проводим симптоматическую и локальную противовоспалительную терапию по действующим клиническим рекомендациям.
Для присвоения статуса «часто болеющий ребенок» и определения объема иммунологического обследования используются следующие критерии [30–32]:
Клинические критерии:
-
возраст до 5 лет: более 4–6 ОРИ;
-
возраст 5–14 лет: более 4 эпизодов в год;
-
возраст старше 14 лет: более 2 эпизодов в год.
Показания для скрининга иммунодефицитов: наличие отягощенного семейного анамнеза по иммунологическим заболеваниям; рецидивирующие инфекции, требующие госпитализации; наличие оппортунистических инфекций; персистирующие и прогрессирующие инфекции; необычная восприимчивость к микроорганизмам.
Базовые лабораторные исследования: клинический анализ крови с дифференцированным подсчетом лейкоцитов; уровень иммуноглобулинов A, G, M; общий белок и белковые фракции; при необходимости: исследование функции фагоцитов, Т-лимфоцитов, комплемента [15, 29].
Общие принципы лечения ОРВИ у детей
Общие принципы лечения ОРВИ у детей носят симптоматический характер, лечение обычно проводится амбулаторно, госпитализация может быть показана только в случае тяжелого течения ОРВИ или при наличии значимой сопутствующей патологии1.
Прежде всего необходимы постельный режим, обильное питье, увлажнение воздуха в помещениях, а также исключение приема антибактериальных препаратов и мощных иммуномодуляторов без показаний. В случае повышения температуры тела выше 38,5 °С (или выше 38 °С при наличии сопутствующей патологии) важно применять жаропонижающие и противовоспалительные препараты. В клинических рекомендациях по лечению ОРВИ у детей предлагается парацетамол в дозе 10–15 мг на 1 кг на прием не чаще 4–5 р/сут, а также ибупрофен в случае недостаточной эффективности парацетамола или при выраженном болевом синдроме в дозе от 5 до 10 мг на 1 кг не чаще 3–4 р/сут, прием парацетамола и ибупрофена вместе не рекомендуется без строгих показаний1.
Системная противовирусная терапия
В случае подтвержденного диагноза гриппа можно использовать этиотропные препараты, которые назначают в первые 48 ч от начала симптомов, в случае тяжелого течения заболевания возможно назначение до 72 ч от его начала.
Другие ОРВИ не имеют этиотропного лечения, возможен выбор противовирусных средств по решению врача с учетом возраста и сопутствующей патологии [33].
Одним из таких препаратов является инозин пранобекс, проявляющий противовирусную и иммуностимулирующую активность [34].
Механизмы действия инозина пранобекса. Прямая противовирусная активность. Инозин пранобекс подавляет репликацию различных РНК- и ДНК-содержащих вирусов путем ингибирования синтеза вирусной РНК и протеинов [35, 36].
Иммуностимуляция. Инозин пранобекс усиливает функцию T-лимфоцитов и натуральных киллеров, увеличивая продукцию IFN и IL [37, 38]. В экспериментальных моделях показано, что препарат повышает активность цитотоксических T-лимфоцитов и NK-клеток, опосредующих элиминацию вирус-инфицированных клеток.
Усиление врожденного иммунитета. Инозин пранобекс стимулирует выработку IFN-α и -β как макрофагами, так и эпителиальными клетками и фибробластами. Механизм включает активацию TLR на иммунных клетках.
Модуляция адаптивного иммунитета. Исследования показали, что инозин пранобекс усиливает дифференцировку Th1-ответа, способствуя выработке IFN-γ и IL-2 [37].
Клинические исследования эффективности. Эффективность инозина пранобекса в лечении ОРВИ подтверждена многочисленными рандомизированными плацебо-контролируемыми исследованиями на большом количестве наблюдений.
Рандомизированное контролируемое исследование (РКИ) на когорте из 163 детей (2025 г.) [34]. Исследование, проведенное в условиях амбулаторного ведения, включило 163 ребенка в возрасте 3–17 лет с диагнозом ОРВИ. Пациенты были разделены на группы в зависимости от вида противовирусного препарата, который они получали. Первичные исходы включали продолжительность основных клинических симптомов (гипертермия, ринит, боль в горле) и общую длительность острого периода заболевания. Основные результаты исследования: у детей, получавших инозин пранобекс, нормализация температуры тела наступала к 3–5-м суткам (в среднем на 2–3 сут раньше, чем в группе пациентов, получавших другие противовирусные препараты; p<0,05); кашель у детей, принимавших инозин пранобекс, регистрировали в 4,0–4,5 раза реже по сравнению с пациентами, получавшими другие противовирусные препараты; продолжительность ринита сокращалась на 2–3 сут; боль в горле купировалась на 1–2 сут раньше.
Масштабная фармакоэпидемиологическая программа «ОРИентир» (дети и подростки 3–18 лет, n=11 334) [35]. Результаты показали высокую эффективность инозина пранобекса в лечении ОРВИ различной этиологии: существенное сокращение общей продолжительности заболевания на 2–3 дня; снижение в 4 раза частоты осложнений ОРВИ (пневмонии, отиты, синуситы) по сравнению с целым рядом других противовирусных препаратов и симптоматической терапией; частота осложнений в группе инозина пранобекса составила 11,8% против 71,2% в группе без противовирусной терапии; потребность в антибиотикотерапии была значительно ниже при использовании инозина пранобекса.
В ходе программы «АлгОРИтм» (январь — апрель 2024 г.) 379 врачей из 115 городов и 38 регионов РФ оценили тактику ведения 4319 детей 3–7 лет с ОРВИ. Противовирусные препараты получали лишь 20,8% пациентов. В группе, получавшей Гроприносин®, регресс симптомов наступал на 2 дня раньше, а пик проявлений фиксировали уже на 3-й день болезни, тогда как при симптоматической терапии он смещался на 5-й день, а общая длительность заболевания нередко достигала 10 дней. У детей 4–5 лет, не получавших противовирусных средств, клинические симптомы наблюдались в 7 раз чаще (р<0,05). Кроме того, в группе Гроприносина частота назначения антибиотиков оказалась минимальной (11,8%), что в 6 раз ниже, чем в группе без противовирусной терапии (71,2%). Таким образом, раннее применение противовирусных средств, в частности инозина пранобекса (Гроприносин®), способствует более быстрому купированию симптомов респираторной инфекции, снижает вероятность возникновения бактериальных осложнений и, соответственно, минимизирует необходимость в антибактериальной терапии, что в итоге позволяет сдерживать рост антибиотикорезистентности и избегать избыточной лекарственной нагрузки в педиатрической практике [39].
Назначение при ГВИ. Особое значение инозина пранобекса для ЧБД состоит в его эффективности против ГВИ. Высокая распространенность активности герпесвирусов у детей с симптомами ОРВИ (26,5%) и их иммуносупрессивное действие обусловливают необходимость применения препаратов широкого спектра противовирусного действия [18]. Исследование эффективности инозина пранобекса у детей с подтвержденной ГВИ показало элиминацию маркеров активной ГВИ в течение 2–3 нед. лечения, предотвращение реактивации герпесвирусов и развития осложнений, а также нормализацию показателей клеточного иммунитета после завершения курса терапии [35, 40].
Безопасность и переносимость. Обычно дети хорошо переносят лечение инозином пранобексом, однако возможны побочные реакции, например, диспепсические явления (тошнота, рвота, боль в эпигастрии), аллергические реакции (сыпь, зуд), нечасто — полиурия [39, 40]. Противопоказаниями служат гиперчувствительность к препарату, подагра, мочекаменная болезнь, хроническая почечная недостаточность, аритмии, детский возраст до 3 лет. Важно учитывать, что иммунодепрессанты (цитостатики, высокие дозы кортикостероидов) ослабляют иммуностимулирующий эффект инозина пранобекса.
При определении показаний к системной противовирусной терапии инозином пранобексом следует учитывать, что он снижает риск развития осложнений у ЧБД и детей с отягощенным отоларингологическим анамнезом (рецидивирующие синуситы и отиты), а также у детей с сопутствующей коморбидной патологией, с наличием ВЭБ, ЦМВ, ВГЧ-6 в анамнезе, рецидивирующего лабиального герпеса, выраженным увеличением шейных лимфатических узлов и наличием петехиальной сыпи непосредственно после начала ОРВИ [38].
Также возможно назначение инозина пранобекса при среднетяжелом течении ОРВИ с выраженной интоксикацией, повышением температуры до 38,5 °С; при прогнозе длительного течения заболевания, когда отсутствует тенденция к улучшению состояния на 3–4-й день ОРВИ; наличии в анамнезе недавно перенесенной тяжелой респираторной вирусной инфекции и недостаточности предыдущей противовирусной терапии [41].
Таким образом, на основании проанализированных многочисленных публикаций можно утверждать, что инозин пранобекс может использоваться в качестве противовирусного иммуномодулирующего средства в группе ЧБД при ОРВИ и высоком риске развития осложнений на фоне респираторных вирусных инфекций.
Не нужно забывать и о симптоматической терапии при ОРВИ. При наличии выделений из носа и заложенности носа необходимо промывание физиологическим или изотоническим морским растворами, а у детей младшей группы следует проводить отсасывание секрета из полости носа специальными устройствами. При выраженной назальной обструкции возможно применение короткого курса деконгестантов с учетом возраста ребенка, но не дольше 3–5 дней. При наличии продуктивного кашля и затекания отделяемого по задней стенке глотки возможно применение муколитиков и мукорегуляторов. Боль в горле купируется назначением лекарственных форм, содержащих нестероидные противовоспалительные препараты (НПВП), топические анальгетики и противомикробные средства1.
Локальная противовоспалительная и микробная терапия
Локальная противовоспалительная и антимикробная терапия при ОРВИ направлена на уменьшение боли в горле, отека и воспаления слизистой ротоглотки, а также на частичное снижение микробной нагрузки, не заменяя при этом системное лечение и общие меры. В педиатрической практике для орошения слизистой глотки применяются спреи и растворы, содержащие средства с противовоспалительным и анальгезирующим эффектом, такие, например, как бензидамин, который обладает локальным обезболивающим, противовоспалительным и подтвержденным антимикробным действием в отношении ряда клинически значимых патогенов, что позволяет уменьшить выраженность боли и дискомфорта при глотании. Препараты этой группы используют в виде дозированных спреев или полосканий с последующим воздержанием от еды и питья на 15–30 мин, при строгом учете возрастных ограничений и соблюдении техники применения, особенно у детей младшего возраста, чтобы обеспечить адекватный контакт раствора со слизистой и снизить риск нежелательных реакций.
При выборе локального препарата учитывают доказательную базу, профиль безопасности и возраст ребенка, избегая многокомпонентных средств с недоказанной эффективностью и агрессивным воздействием на слизистую, а также не назначая местные антибиотики без четких показаний, чтобы не способствовать нарушению местного микробиоценоза ротоглотки1 [42].
Фармакология и механизм действия бензидамина. Бензидамин гидрохлорид является индазольным производным, обладающим комбинированным противовоспалительным, местноанестезирующим и антимикробным действием [41, 42]. В отличие от НПВП бензидамин оказывает свои эффекты исключительно локально и не подавляет синтез простагландинов, необходимых для защиты слизистой желудочно-кишечного тракта.
Механизмы действия бензидамина. Противовоспалительный эффект. Бензидамин действует локально через модуляцию макрофагов и фибробластов в очаге воспаления, предотвращает высвобождение провоспалительных цитокинов (особенно TNF-α и IL-1β), что приводит к снижению активности циклооксигеназы 2. Более поздние исследования показали, что бензидамин также может ингибировать миграцию моноцитов и блокировать путь p38 MAPK, ключевой регулятор биосинтеза провоспалительных цитокинов. Наряду с уменьшением количества воспалительных цитокинов бензидамин также оказывает влияние на воспалительный процесс посредством различных механизмов: снижение проницаемости сосудов, вызванное высвобождением гистамина, ацетилхолина, серотонина и адреналина; ингибирование агрегации тромбоцитов и образования тромбов; ингибирование дегрануляции полиморфно-ядерных лейкоцитов человека; ингибирование миграции моноцитов человека [43].
Местноанестезирующее действие. Бензидамин обладает структурной схожестью с местными анестетиками (прокаин, новокаин) и блокирует трансмембранный ток натрия в нервных волокнах, снижая возбудимость ноцицепторов. Местная анестезирующая активность была продемонстрирована в клинических исследованиях [44, 45].
Анальгезирующий эффект. Снижение концентрации биогенных аминов с альгогенными свойствами (гистамина, брадикинина, серотонина, норадреналина) в результате ингибирования синтеза простагландинов и блокады взаимодействия брадикинина с тканевыми рецепторами способствует повышению порога болевой чувствительности в очаге воспаления. Восстановление микроциркуляции и улучшение оксигенации тканей дополнительно способствуют уменьшению боли [46, 47].
Антимикробное действие. Бензидамин оказывает антибактериальный эффект против широкого спектра микроорганизмов (в том числе Streptococcus pyogenes, S. aureus, S. pneumoniae, H. influenzae) путем быстрого проникновения через клеточные мембраны микроорганизмов с последующим повреждением их внутриклеточных структур и нарушением метаболических процессов [42, 48].
Противогрибковое действие. Препарат активен против штаммов Candida albicans и non-albicans, вызывая структурные модификации клеточной стенки грибов и их метаболических цепей, препятствуя репродукции [42].
Эффективность бензидамина подтверждается многочисленными исследованиями. Так, в рандомизированном двойном слепом плацебо-контролируемом исследовании терапии острого тонзиллофарингита у 147 пациентов отмечено значительное снижение интенсивности клинических признаков в группе активного лечения с применением бензидамина по сравнению с группой контроля (p<0,05). На 7-й день лечения разницы в качестве жизни между группами не было выявлено, препараты хорошо переносились; серьезных побочных эффектов не отмечено. Авторы заключили, что спрей с хлоргексидином и бензидамином, добавленный к стандартной антибиотикотерапии, значительно снижает интенсивность клинических симптомов при стрептококковом фарингите [43].
Также проведен ряд исследований, подтвердивших местное анальгезирующее и противовоспалительное действие и безопасность бензидамина при боли в горле различного генеза [44–49].
Технология доставки и формы препарата. Бензидамин в виде препарата Оралсепт® представлен в нескольких лекарственных формах, различающихся по скорости наступления эффекта и продолжительности действия.
Технологические преимущества спрея Оралсепт®:
- прямая доставка активного вещества на воспаленную ткань;
- минимизация проглатывания лекарства (в отличие от полосканий и таблеток);
- точная дозировка (одна доза = одно распыление = 0,255 мг);
- быстрое облегчение симптомов.
В качестве иллюстрации важности и эффективности комплексного подхода к лечению неосложненной ОРВИ у ЧБД приводим клиническое наблюдение.
Клиническое наблюдение
Пациент М., мальчик, 5 лет 2 мес. Масса тела 19 кг, посещает детский сад, первый год посещения.
Из анамнеза: беременность и роды у матери протекали без осложнений, ребенок родился доношенным, с массой тела 3400 г, развивался нормально, прививки выполнены в соответствии с национальным календарем, аллергические реакции ранее не отмечались, отоларингологических вмешательств не проводилось.
В семейном анамнезе: мать здорова, работает в образовательном учреждении и имеет профессиональный контакт с детьми, отец также здоров, случаев первичных иммунодефицитов среди близких родственников не выявлено.
Текущее заболевание началось 3 дня назад, при этом первым днем болезни считается период двухдневной давности; первоначально появились прозрачная ринорея и чихание, затем в течение первых двух суток постепенно нарастала заложенность носа, возникла умеренная боль в горле и кашель, петехиальная сыпь на верхних конечностях и груди, а на 3-й день температура повысилась до 38,7 °C, усилились общее недомогание и утомляемость, кашель. Родители подчеркивают, что это уже третий эпизод выраженной ОРВИ за последние 4 мес. (предыдущие эпизоды были 2 и 4 мес. назад), а суммарно за последние 12 мес. у ребенка отмечено 5 эпизодов острых респираторных заболеваний, что превышает возрастной порог и соответствует статусу часто болеющего ребенка в возрасте до 5 лет.
Ребенок во время осмотра активен, но выглядит утомленным, охотно вступает в контакт, ест хуже обычного, хотя пьет охотно, сон нарушен из-за кашля и назальной обструкции; температура тела составляет 38,5 °C, частота дыхания 28 в 1 мин при возрастной норме 20–25, частота сердечных сокращений 110 в 1 мин при норме 95–105, артериальное давление 100/65 мм рт. ст., насыщение кислородом 98% на комнатном воздухе.
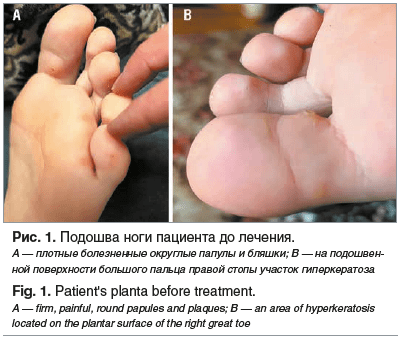
При объективном осмотре кожа и слизистые бледные, без сыпи, нормальной влажности; в полости носа отмечается прозрачное отделяемое, слизистая гиперемирована и отечна; миндалины увеличены до второй степени без налетов, задняя стенка глотки гиперемирована и отечна, глотание сопровождается болью (см. рисунок, А). Шейные лимфатические узлы увеличены до 1 см, безболезненные, подвижные, не спаянные с окружающими тканями; форма грудной клетки нормальная, дыхание везикулярное, хрипов нет, кашель сухой; сердечные тоны звучные, границы сердца в пределах нормы, шумы не выслушиваются; живот мягкий, безболезненный, печень не увеличена, селезенка не пальпируется, менингеальные симптомы отсутствуют.
На основании анамнеза и клинических данных выставлен диагноз: острая респираторная вирусная инфекция неуточненной этиологии, среднетяжелое течение, без признаков осложнений. С учетом амбулаторного ведения и отсутствия признаков бактериальной суперинфекции дополнительные лабораторно-инструментальные исследования на данном этапе не проводились, однако при осложненном или затяжном течении либо при отсутствии улучшения к 5–7-му дню заболевания запланировано проведение ПЦР-диагностики респираторных вирусов и, при наличии показаний, бактериологического исследования мокроты.
Дополнительно уточнено, что за последний год у ребенка было 5 эпизодов острых респираторных заболеваний, он регулярно контактирует с большим детским коллективом в детском саду, при этом организованных мероприятий по закаливанию и систематических занятий физической культурой не проводилось, что рассматривается как дополнительный фактор риска формирования статуса ЧБД.
Назначенное лечение:
системная противовирусная терапия препаратом инозина пранобекса (Гроприносин®): сироп 50 мг/мл (с мерным шприцем для облегчения дозирования); доза: 50 мг/кг (1 мл на 1 кг массы тела в сутки) = 19 мл сиропа (950 мг) в сутки для ребенка массой тела 19 кг; схема: разделить на 3 приема по 6 мл 3 р/сут после еды; продолжительность: 7 дней (3–9-й день болезни);
локальная противовоспалительная и антимикробная терапия препаратом бензидамина (спрей Оралсепт®) по 4 дозы (распыления) на одно применение; кратность: 4 р/день (после завтрака, обеда, полдника, ужина); продолжительность: 5–7 дней. Техника: распыление на воспаленную область (миндалины, глотку), воздержание от еды/питья 15–30 мин.
Также назначены симптоматическая терапия (жаропонижающие препараты, элиминационная терапия полости носа), обильное теплое питье, щадящая диета с легкоусвояемой пищей, запрет на посещение детского дошкольного учреждения в течение как минимум 5–7 дней и до полного выздоровления.
На фоне проводимой терапии на 2-й день от начала лечения отмечено повышение активности ребенка, температура снизилась до субфебрильной, петехиальная сыпь исчезла, купировались болезненные ощущения в горле и уменьшились воспалительные явления. На 5-й день от начала лечения отмечали нормализацию температуры тела, значительное уменьшение кашля и боли в горле, уменьшение выраженности симптомов интоксикации и улучшение носового дыхания. При осмотре ротоглотки отмечена положительная динамика: уменьшение гиперемии и отечности слизистой зева (см. рисунок, В).

Полученные результаты лечения показывают положительное потенцирующее влияние совместного применения системной противовирусной и топической противовоспалительной терапии на улучшение состояния ребенка и ускорение выздоровления.
Обсуждение
Острые респираторные вирусные инфекции у ЧБД формируются на фоне сочетанного нарушения микробиома ВДП, персистенции герпесвирусов и дефектов врожденного иммунитета, что повышает риск развития рецидивов и осложнений со стороны ЛОР‑органов. В этой ситуации целесообразно сочетать системную противовирусную и иммуномодулирующую терапию (инозин пранобекс) с топическим контролем воспаления и боли в горле (бензидамина гидрохлорид), обеспечивая многоуровневое воздействие на патологический процесс.
Инозин пранобекс действует системно, подавляя репликацию широкого спектра вирусов (включая герпесвирусы) и усиливая функцию T‑лимфоцитов и NK‑клеток, что способствует более быстрому купированию интоксикации и снижению частоты осложнений ОРВИ. Бензидамина гидрохлорид, применяемый местно в виде спрея или таблеток, оказывает выраженный противовоспалительный, анальгезирующий и антимикробный эффект на уровне слизистой ротоглотки, уменьшая отек, боль и бактериальную нагрузку, без значимого системного воздействия.
Клинические исследования показывают, что назначение бензидамина в составе комплексной терапии ОРВИ у детей сокращает общую продолжительность заболевания примерно на 1–1,5 сут и ускоряет регресс боли в горле и катарального синдрома, при этом препарат хорошо переносится и не требует коррекции дозы системных НПВП. Совместное применение инозина пранобекса и бензидамина гидрохлорида логично сочетает системное противовирусное и иммуномодулирующее действие с локальным противовоспалительным и обезболивающим эффектом, что особенно важно у ЧБД с выраженной болью в горле, отеком миндалин и риском возникновения бактериальных осложнений.
С точки зрения безопасности, прямых клинически значимых фармакокинетических взаимодействий между инозином пранобексом и бензидамина гидрохлоридом не описано; инозин пранобекс в основном взаимодействует с иммунодепрессантами и некоторыми антиретровирусными препаратами, а бензидамин действует преимущественно местно, не подавляя системный синтез простагландинов. Поэтому при соблюдении возрастных дозировок и схем применения (инозин пранобекс — системно, бензидамин — топически) их сочетание может рассматриваться как патогенетически обоснованная и безопасная комбинация в комплексном лечении ОРВИ у детей, в том числе у часто болеющих.
Заключение
Совместное применение инозина пранобекса и бензидамина гидрохлорида позволяет сочетать системное противовирусное и иммуномодулирующее действие с выраженным местным противовоспалительным и обезболивающим эффектом, что особенно актуально у детей с выраженной интоксикацией, болью в горле и высоким риском развития ЛОР‑осложнений. Отсутствие описанных клинически значимых взаимодействий между препаратами, хорошо изученный профиль безопасности делают такую комбинацию патогенетически обоснованной и приемлемой в педиатрической практике.
1Клинические рекомендации Мин здрава России. Острая респираторная вирусная инфекция (ОРВИ). 2022-2023-2024. (Электронный ресурс.) https://recipture.ru/recommend/LOR/ORVI1d.pdf? (дата обращения: 03.02.2026).
Сведения об авторах:
Кириченко Ирина Михайловна — д.м.н., профессор кафедры оториноларингологии Медицинского института Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; главный оториноларинголог ООО «Он Клиник Арбат»; 121069, Россия, Москва, ул. Большая Молчановка, д. 32, стр. 1; ORCID iD 0000-0001-6966-8656
Попадюк Валентин Иванович — д.м.н., профессор, декан факультета ФНМО и заведующий кафедрой оториноларингологии Медицинского института Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; ORCID iD 0000-0003-3309-4683.
Чернолев Анна Ильинична — к.м.н., доцент кафедры оториноларингологии Медицинского института Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; ORCID iD 0000-0003-3082-3182
Мамадкулов Муслихиддин Мирзоевич — аспирант кафедры оториноларингологии Медицинского института Российского университета дружбы народов; 117198, Россия, г. Москва, ул. Миклухо-Маклая, д. 6; ORCID iD 0009-0000-7132-6815
Каннер Екатерина Валерьевна — д.м.н., старший научный сотрудник клинического отдела инфекционной патологии ФБУН ЦНИИ Эпидемиологии Роспотребнадзора; 111123, Россия, г. Москва, ул. Новогиреевская, д. 3А; ORCID iD 0000-0003-3204-1846
Фарбер Ирина Михайловна — к.м.н., ассистент кафедры детских болезней клинического института детского здоровья им. Н.Ф. Филатова ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет); 119991, Россия, г. Москва, ул. Трубецкая, д. 8, стр. 2; ORCID iD 0000-0001-6919-6732
Контактная информация: Кириченко Ирина Михайловна, e-mail: loririna@yandex.ru
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 14.12.2025.
Поступила после рецензирования 13.01.2026.
Принята в печать 30.01.2026.