Введение
Вирусные бородавки с различной локализацией, причиной которых могут являться многочисленные штаммы вирусов папилломы человека (ВПЧ), являются достаточно распространенной патологией кожи и слизистых оболочек как у детей, так и у взрослых [1, 2]. Инфицирование может происходить контактно-бытовым путем при наличии микротравм и воспалительных процессов кожных покровов, а также это зависит от общего и локального иммунного статуса человека, когда отсутствует местный иммунный ответ на ВПЧ-инфекцию, опосредованный Т-клетками. При начале процесса репликации ВПЧ в эпителии нарушается дифференцировка клеток, что приводит к морфологическим изменениям в тканях и формированию гиперкератоза. Исключительно на ладонях и подошвах локализуются глубокие ладонно-подошвенные бородавки, вызываемые ВПЧ 1-го, реже 3, 27, 29 и 57-го типов. Клинически они представлены плотными болезненными округлыми бляшками, покрытыми сухим ороговевшим слоем эпидермиса, при удалении которого можно увидеть мелкие черные точки, и зачастую имеют глубокий так называемый корень [3, 4]. Данные кожные проявления являются доброкачественными и в некоторых случаях могут редуцироваться самостоятельно, но у большинства пациентов может ухудшаться качество жизни в связи с болезненностью при травмировании, отмечается частое рецидивирование после удаления бородавок. В литературе указывается на связь низкого содержания витамина D и ферритина в сыворотке крови с нарушением иммунной защиты против ВПЧ, провоцирующих появление бородавок с подошвенной локализацией [5–7].
В клинических рекомендациях описаны различные методы местной деструкции элементов, такие как хирургический, радиоволновой, лазерный, жидким азотом, прижиганием лекарственными препаратами. Однако в настоящее время в комплексное лечение могут включаться как иммунотропные препараты, так и различные системные неспецифические противовирусные препараты, поскольку в патогенезе возникновения подошвенных бородавок, вызванных ВПЧ-инфекцией, определенную роль играет нарушение механизмов клеточного иммунитета [8–11].
Терапия подошвенных бородавок бывает затруднительна в связи с использованием химических методов лечения с низкой проникающей способностью кислот, а также высокой травматизацией у детей при радикальном удалении разросшихся элементов. При несоблюдении антисептических условий в период заживления раневая поверхность может инфицироваться, что приведет к воспалительным реакциям, увеличению сроков заживления и рубцеванию тканей. В литературе описаны исследования эффективности крио-терапии подошвенных бородавок, при этом отмечена высокая травматичность метода и показано превосходство противовирусных препаратов и химиотерапии [12, 13].
Препаратом выбора для комплексной терапии подошвенных бородавок стал комбинированный лекарственный препарат, содержащий три известные фармакологические субстанции: α-глутамил-триптофан натрия, бендазол и аскорбиновую кислоту, — с доказанным протективным и лечебным действием, противовирусным эффектом относительно многих вирусов за счет интерфероногенных свойств, уменьшением процессов активации интрацеллюлярного воспаления (инфламмасом) и снижением пироптотической гибели клеток [14]. Увеличение общей резистентности организма за счет активации клеточного иммунитета и других факторов неспецифической защиты неоднократно было доказано в экспериментальных и клинических исследованиях [15, 16].
Также известно, что местное применение α-глутамил-триптофана натрия оказывает регулирующее влияние на реакции локального клеточного и гуморального иммунитета, стимулирует регенерацию кожи за счет улучшения процессов клеточного метаболизма путем воздействия на глутаматные метаботропные рецепторы и широко используется для ускорения заживления повреждений кожных покровов различной природы у пациентов разного возраста [17, 18].
Авторами была предложена схема комбинированного применения пероральной (капсулы) и местной (крем) формы препаратов, содержащих α-глутамил-триптофан натрия, основанная на показаниях к применению препарата с МНН действующего вещества α-глутамил-триптофан в лекарственной форме раствор для внутримышечного введения[1], применяемого у взрослых и детей в возрасте от 6 мес. для комплексной терапии острых и хронических вирусных и бактериальных заболеваний, сопровождающихся снижением иммунитета. Проведенные ранее исследования, в ходе которых определяли содержание в сыворотке крови мышей лизоцима, миелопероксидазы и неспецифической эстеразы в динамике по дням после приема препарата, продемонстрировали снижение данных показателей до фонового уровня к 10–14-му дню наблюдения. В клинических испытаниях зарегистрировали снижение до фоновых значений к 10–14 дню уровня интерферонов и фагоцитарной активности нейтрофилов у здоровых добровольцев, а также у пациентов с иммунодефицитными состояниями, что позволило предложить схему назначения препарата для поддержания у пациента защитных сил организма на достаточном уровне [16, 18, 19].
Таким образом, актуальной является разработка новых схем лечения ювенильных бородавок для улучшения терапевтического эффекта деструктивных методов лечения с целью предотвращения рецидивов возникновения бородавок у детей. Представляем собственное клиническое наблюдение пациента со множественными подошвенными бородавками.
Пациент и его законный представитель добровольно подписали информированное согласие на получение соответствующего лечения и публикацию персональной медицинской информации в обезличенной форме в научно-медицинской литературе.
Клиническое наблюдение
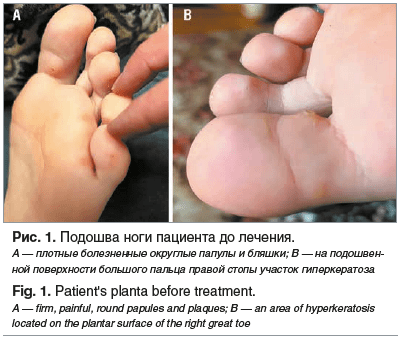
Под нашим наблюдением в течение 4 мес. (с ноября 2023 г. по март 2024 г.) находился мальчик в возрасте 13 лет с установленным диагнозом «множественные подошвенные бородавки», код B07 по МКБ-10. Семейный анамнез без особенностей. Появление первых элементов отмечалось более 6 мес. назад в январе-феврале 2023 г. В течение 2 мес. (сентябрь, октябрь 2023 г.) пациент проходил лечение у дерматолога по поводу данного заболевания. Пациент получал инозин пранобекс 500 мг после еды 3 р/день 14 дней и применял гель на основе гидроксида натрия для деструкции бородавок 1 раз в 4 дня в течение 1 мес. При этом было рекомендовано не мочить бородавки в течение первых 7 дней, что значительно ухудшало качество жизни пациента. Несмотря на применяемое лечение, элементы разрастались и появлялись новые плотные болезненные округлые папулы и бляшки (рис. 1А). На подошвенной поверхности большого пальца правой стопы сохранялся округлый возвышающийся участок гиперкератоза 1,2×0,8 см (рис. 1В). Пациент отмечал болезненность при ходьбе и медленное заживление бородавок в течение 2 мес. с формированием косметических дефектов. В связи с отсутствием значимого лечебного эффекта врачом-дерматологом была рекомендована плановая крио- или лазеродеструкция очагов. Так как бородавки располагались на подошвенной поверхности, родители мальчика опасались более сильной травматизации кожи стоп и самостоятельно обратились к врачу аллергологу-иммунологу в СПб ГБУЗ «Городская поликлиника № 106» для коррекции иммунной терапии.

Результаты физикального, лабораторного и инструментального исследования
При осмотре в области подошв на обеих ногах, преимущественно на правой, визуализировались множественные (до 9 элементов) папулы разного размера от 0,2 до 0,9 см, цвета кожи, с веррукозными разрастаниями на поверхности и очагами микротромботизации, с наслоением гиперкератотических масс по периферии. Непораженные кожные покровы нормальной окраски и влажности.
На рис. 1 видно, что подошвенными бородавками значительно поражены глубокие слои эпидермиса, которые после деструкции химическим или лазерным методом могут образовывать глубокие раневые поверхности. При подошвенной локализации повреждений заживление идет медленнее, чаще возможно травмирование, что вызывало у пациента болезненность при ходьбе и значительно ухудшало качество жизни.
До назначения иммуномодулирующей терапии проведена оценка статуса витамина D с помощью определения общего 25(ОН)D в сыворотке крови по международным стандартам (DEQAS, NIST). У пациента при отсутствии субъективных симптомов инфекционно-воспалительного процесса выявлен сниженный уровень 25(OH)D (32 нг/мл при норме выше 40 нг/мл), ферритин ближе к нижней границе нормы — 28 мкг/л при норме от 7 до 140 мкг/л, что свидетельствует о дефиците витамина D и скрытом дефиците железа. Показатели клинического анализа крови без клинически значимых отклонений от возрастной нормы, хотя относительное и абсолютное число нейтрофилов было на нижней границе нормы.
Дифференциальный диагноз проводился с мозолями, кератодермией, псориазом ладоней и подошв. Тщательно собранный анамнез и характерный признак — мелкие черно-коричневые точки в центре наростов позволили поставить диагноз «подошвенные бородавки».
Лечение
Решением врачебной комиссии СПб ГБУЗ «Городская поликлиника № 106» было одобрено применение комбинированной терапии препаратами с α-глутамил-триптофаном без применения деструктивных методов, поскольку используемые препараты обладают высоким уровнем безопасности, не имеют эффекта превышения возрастных дозировок, не увеличивают риск ухудшения заболевания при применении «вне инструкции» и могут быть назначены по описанной ниже схеме. После подписания пациентом и его законным представителем информированного согласия на предложенный курс лечения пациенту назначили внутрь препарат α-глутамил-триптофан + аскорбиновая кислота + бендазол (регистрационный номер ЛП-№ (002868)-(РГ-RU) от 25.07.2023) для детей старше 6 лет для профилактики и лечения вирусных инфекций по 1 капсуле, содержащей α-глутамил-триптофан натрия 0,5 мг, аскорбиновую кислоту 50 мг, бендазола гидрохлорид 20 мг 3 р/день в течение 4 дней, затем перерыв 10 дней и еще один курс 4 дня. С первого дня лечения рекомендовалось наносить α-глутамил-триптофан 0,05% крем с действующим веществом α-глутамил-триптофан натрия 0,05 г 2–3 р/день на пораженные участки кожи (суточная доза — 2 г крема). Дополнительно пациент получал витамин D3 в суточной дозе 2000 МЕ 1 р/день утром во время еды в течение 2 мес. по назначению врача-дерматолога. От ферротерапии было решено воздержаться во избежание полипрагмазии в данном случае.
Исход и результаты последующего наблюдения
Уже через 2 нед. пациент отмечал значительное улучшение, учитывая поражение более глубоких слоев эпидермиса после деструкции основных элементов бородавок, проведенной ранее гелем на основе гидроксида натрия. Появления новых элементов в течение 3 мес. не наблюдалось. Через 2 нед. от начала лечения в сыворотке крови уровень 25(OH)D и ферритина повысился до нормальных значений (49 нг/мл и 56 мкг/л соответственно), что свидетельствовало о восстановлении механизмов иммунитета, в которых участвует железо и витамин D. В клиническом анализе крови отмечено незначимое увеличение в пределах возрастной нормы относительного и абсолютного числа нейтрофилов по сравнению с первым исследованием.
На рисунке 2А показано, что через 2 нед. комбинированной терапии препаратами с α-глутамил-триптофаном натрия наблюдался заключительный этап интенсивного заживления на месте бородавок с отшелушиванием глубоких слоев эпидермиса.
Через 2 мес. наблюдения на ступне отмечали абсолютно гладкую кожу без рубцов и других косметических дефектов (рис. 2В). Рецидивирования бородавок не отмечалось в течение всего периода наблюдения. Пациент и его родители были довольны результатом лечения.

Обсуждение
В иммунотерапии вирусных бородавок допускаются различные препараты с иммуномодулирующим действием. В связи с тем, что причиной появления подошвенных бородавок являются ВПЧ, с которыми не справляется иммунная система, авторами были выбраны препараты с α-глутамил-триптофаном натрия, которые применяются в педиатрической практике для лечения и профилактики острых и хронических вирусных и бактериальных заболеваний, сопровождающихся снижением иммунитета, в том числе при поражении кожи и подкожной клетчатки.
Исследования механизма действия этого дипептида на иммунную систему человека показали его способность повышать функциональную активность нейтрофилов за счет активации системы ICAM-1, а также снижать уровень провоспалительного цитокина IL-1, способствуя репарации поврежденных тканей [16, 18].
Назначение витамина D в лечебной дозе позволило купировать его недостаточность в организме и устранить вероятный предрасполагающий фактор снижения неспецифической резистентности и репаративных процессов в организме. Предложенная схема двух курсов иммуномодулирующего препарата, а также местная обработка подошвенных бородавок кремом, влияющим на регенерацию тканей, оказала положительное влияние на механизмы естественного иммунитета, что значительно ускорило процесс заживления после деструкции основных элементов. Также было отмечено исчезновение неповрежденных бородавок и отсутствие раннего рецидивирования в течение 3 мес. наблюдения. Лечение не травматично, хорошо переносится, отмечено полное восстановление кожи на ступнях без формирования рубцов, что значительно улучшило качество жизни пациента.
Заключение
Комбинированное пероральное применение иммуномодулирующего препарата с ежедневной обработкой кремом пораженных участков кожи может быть более эффективным, чем изолированное применение препаратов. Положительный клинический эффект на фоне предложенной схемы комбинированного применения (местного и перорального) двух лекарственных форм α-глутамил-триптофана натрия может быть обусловлен как противовоспалительным, так и противовирусным действием, которое, возможно, предотвращает распространение ВПЧ — фактора рецидивирования процессов образования бородавок. Также вероятно, что эффект был достигнут не только за счет применения α-глутамил-триптофана натрия, но и благодаря назначению витамина D в лечебной дозе, что позволило купировать его недостаточность в организме. Однако необходимо дальнейшее изучение предложенной схемы применения препаратов с α-глутамил-триптофаном для рационального обоснования методов иммунокоррекции и совершенствования тактики лечения вирусных бородавок у детей.
Сведения об авторах:
Головачева Екатерина Георгиевна — д.м.н., ведущий научный сотрудник отдела респираторных вирусных инфекций у детей ФГБУ «НИИ гриппа им. А.А. Смородинцева» Минздрава России; 197376, Россия, г. Санкт-Петербург, ул. Профессора Попова, д. 15/17; врач аллерголог-иммунолог СПб ГБУЗ «Городская поликлиника № 106»; 198328, Россия, г. Санкт-Петербург, ул. Рихарда Зорге, д. 1; ORCID iD 0000-0002-1934-7288
Афанасьева Ольга Ивановна — д.м.н., заведующая отделом респираторных вирусных инфекций у детей ФГБУ «НИИ гриппа им. А.А. Смородинцева» Минздрава
России; 197376, Россия, г. Санкт-Петербург, ул. Профессора Попова, д. 15/17; ORCID iD 0000-0002-1229-171X
Гончарова Елена Сергеевна — к.м.н., старший научный сотрудник отдела респираторных вирусных инфекций у детей ФГБУ «НИИ гриппа им. А.А. Смородинцева» Минздрава России; 197376, Россия, г. Санкт-Петербург, ул. Профессора Попова, д. 15/17; врач-педиатр СПб ГБУЗ «Городская поликлиника № 106»; 198328, Россия, г. Санкт-Петербург, ул. Рихарда Зорге, д. 1; ORCID iD 0000-0002-1615-9919
Быковская Анна Геннадьевна — заведующая СПб ГБУЗ «Городская поликлиника № 106»; 198328, Россия, г. Санкт-Петербург, ул. Рихарда Зорге, д. 1; ORCID iD 0000-0003-0482-953X
Апрятина Вера Анатольевна — к.м.н., старший научный сотрудник лаборатории нейробиологии и молекулярной фармакологии Института трансляционной биомедицины СПбГУ; Россия, 199034, г. Санкт-Петербург, Университетская наб., д. 7–9, пом. 1050; ORCID iD 0000-0002-9819-6835
Источник финансирования: работа выполнена при поддержке СПбГУ, шифр проекта № 117033714.
Контактная информация: Головачева Екатерина Георгиевна, e-mail: okdixi@mail.ru
Конфликт интересов: отсутствует.
Статья поступила 29.11.2024.
Поступила после рецензирования 24.12.2024.
Принята в печать 16.01.2025.
About the authors:
Ekaterina G. Golovacheva — Dr. Sc. (Med.), Leading Researcher of the Department of Respiratory Viral Infections in Pediatric Patients, Smorodintsev Research Institute of Influenza; 15/17, Professor Popov str., St. Petersburg, 197376, Russian Federation; allergologist-immunologist, St. Petersburg Outpatient Clinic No. 106; 13, Richard Sorge str., St. Petersburg, 198328, Russian Federation; ORCID iD 0000-0002-1934-7288
Olga I. Afanasyeva — Dr. Sc. (Med.), Head of the Department of Respiratory Viral Infections in Pediatric Patients, Smorodintsev Research Institute of Influenza; 15/17, Professor Popov str., St. Petersburg, 197376, Russian Federation; ORCID iD 0000-0002-1229-171X
Elena S. Goncharova — C. Sc. (Med.), Senior Researcher at the Department of Respiratory Viral Infections in Pediatric Patients, Smorodintsev Research Institute of Influenza; 15/17, Professor Popov str., St. Petersburg, 197376, Russian Federation; pediatrician, St. Petersburg Outpatient Clinic № 106; 13, Richard Sorge str., St. Petersburg, 198328, Russian Federation; ORCID iD 0000-0002-1615-9919
Anna G. Bykovskaya — Head of the St. Petersburg Outpatient Clinic № 106; 13, Richard Sorge str., St. Petersburg, 198328, Russian Federation; ORCID iD 0000-0003-0482-953X
Vera A. Apryatina — C. Sc. (Med.), Senior Researcher of Neurobiology and Molecular Pharmacology Laboratory, Institute of Translational Biomedicine, St. Petersburg State University; 7/9, Universitetskaya emb., St. Petersburg, 199034, St. Petersburg, Russian Federation; ORCID iD 0000-0002-9819-6835
Contact information: Ekaterina G. Golovacheva, e-mail: okdixi@mail.ru
Financial Disclosure: the work was supported by St. Petersburg State University, project code No. 117033714.
There is no conflict of interest.
Received 29.11.2024.
Revised 24.12.2024.
Accepted 16.01.2025.
[1] Реестр ОХЛП и ЛВ ЕАЭС. (Электронный ресурс.) URL: https://lk.regmed.ru/Register/EAEU_SmPC (дата обращения: 31.01.2025).