Введение
Хроническая ишемия головного мозга (ХИГМ) — форма сосудистой церебральной патологии, вызванная постепенно нарастающей диффузной недостаточностью кровоснабжения мозговой ткани, что ведет к неуклонному ухудшению функционирования головного мозга и проявляется комплексом неврологических и нейропсихологических расстройств. Основным субстратом хронически протекающей сосудистой патологии головного мозга является церебральная болезнь мелких сосудов, проявляющаяся характерными клиническими и нейровизуализационными изменениями [1, 2]. По данным отечественной литературы, уже с ранних стадий развития ХИГМ пациенты часто предъявляют жалобы на головную боль (ГБ), которая многими врачами и исследователями рассматривается как одно из возможных ее проявлений, в связи с чем пациенты получают традиционную терапию вазоактивными и ноо-тропными средствами, зачастую без эффекта, что приводит к значительному ухудшению качества жизни пациента и дальнейшего прогноза [3]. Почти каждый третий пациент, наблюдавшийся в поликлинике с диагнозом ХИГМ, предъявлял жалобы на ГБ, расстройства эмоционального спектра и нарушения сна [4]. При обследовании пациентов с хронической ежедневной ГБ у 52,2% были выявлены психические расстройства невротического уровня [5]. Выявление взаимосвязи ГБ с эмоциональными и диссомническими нарушениями у пациентов с ХИГМ представляется актуальным, так как предполагает выяснение возможных механизмов формирования цефалгии и применение патогенетически оправданных методов терапии.
Цель исследования: анализ эмоциональных и диссомнических нарушений у пациентов с ХИГМ, страдающих ГБ.
Материал и методы
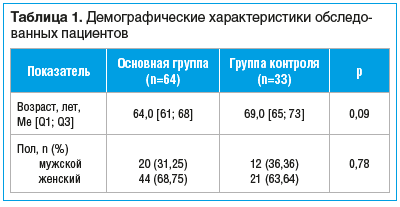
Исследование проведено методом поперечных срезов (cross-sectional). Было включено 97 пациентов (65 женщин и 32 мужчины) в возрасте 50–85 лет (средний возраст 66 лет) с установленным диагнозом ХИГМ. Все пациенты были разделены на 2 группы: в основную группу вошли 64 пациента, страдающих ГБ. Группу контроля составили 33 пациента, не предъявляющих жалобы на ГБ. Пациенты обеих групп были идентичны по полу и возрасту (табл. 1).

С целью оценки изменений вещества головного мозга проводили магнитно-резонансную томографию (МРТ) на томографах с величиной магнитной индукции не менее 1,5 Тл. Диагностику ХИГМ осуществляли по критериям, установленным Wardlaw и исследовательской группой STRIVE (the STandards for ReportIng Vascular changes on nEuroimaging) [15]. Всем пациентам проводили клиническое неврологическое обследование, анализ жалоб и анамнеза заболевания. Диагноз ГБ устанавливали на основании критериев Международной классификации ГБ 3-го пересмотра (МКГБ-3)[1]. Наличие и тяжесть эмоциональных нарушений определяли с помощью госпитальной шкалы тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS) [6], где результат 0–7 баллов расценивался как отсутствие достоверно выраженных симптомов тревоги/депрессии, 8–10 баллов — субклинически выраженная тревога/депрессия, ≥11 баллов — клинически выраженная тревога/депрессия. Для выявления диссомнических нарушений использовали анкету балльной оценки субъективных характеристик сна Я.И. Левина [7], в которой максимальная суммарная оценка составляет 30 баллов, результат менее 19 баллов свидетельствует о наличии нарушений сна.
Статистический анализ выполнен с помощью языка Python 3.12.4, пакетов pandas, scipy, numpy, statsmodels. Проверка на нормальность распределения проводилась с помощью теста Шапиро — Уилка, нормально распределенные данные представлены в формате mean±sd, данные, не удовлетворяющие условиям нормального распределения, — в формате Me [Q1; Q3]. Сравнение двух групп по количественным признакам проводилось с помощью t-критерия Стьюдента для нормально распределенных данных, во всех остальных случаях — с помощью критерия Манна — Уитни. Для качественных признаков сравнение двух групп осуществлялось с помощью критерия χ2 Пирсона (при значениях в таблице сопряженности менее 5 — точного критерия Фишера). Расчет отношения шансов проводился с помощью модели логистической регрессии, в которую в качестве ковариат были включены пол и возраст пациента. Отбор значимых результатов проводился после применения поправки Бенджамини — Хохберга, значение уровня значимости α перед поправкой — 0,05.
Результаты исследования
Из 97 включенных в исследование пациентов с ХИГМ жалобы на ГБ предъявляли 64 (65,98%) человека. Клинический анализ группы пациентов, предъявлявших жалобы на ГБ, выявил, что большинство (39 (60,9%)) пациентов имели длительный анамнез рецидивирующих цефалгий, но при этом до включения в исследование правильно установлен фенотип ГБ был только у 15% пациентов. Во всех остальных случаях наличие ГБ объяснялось недостаточностью мозгового кровообращения. Из 64 пациентов основной группы 51 (79,7%) человек отметил одновременное появление или усиление ГБ по мере возникновения головокружения, неустойчивости, нарушения концентрации внимания и памяти. Первичные формы ГБ диагностированы у 48 (75%) человек, вторичные — у 16 (25%).
Анализ цефалгического синдрома у пациентов основной группы в соответствии с критериями диагноза ГБ по МКГБ-31 позволил установить, что в большинстве случаев отмечалась ГБ напряжения, у четверти пациентов — мигрень. Среди вторичных форм ГБ чаще диагностировалась цервикогенная ГБ. Было установлено, что у 8 пациентов первичные формы ГБ трансформировались в лекарственно-индуцированную ГБ, вызванную избыточным приемом анальгетических препаратов (см. рисунок).

При анализе данных получены результаты, свидетельствующие о том, что у пациентов, страдающих ГБ, чаще, чем у пациентов группы контроля, встречаются расстройства эмоционального спектра (табл. 2).

При анализе степени выраженности тревоги в основной группе пациентов средний суммарный балл по шкале HADS составил 11 [8, 14], в группе контроля — 8 [6, 12], полученные различия показателей оказались статистически незначимыми (p=0,197). При анализе депрессии у пациентов основной группы депрессивное расстройство диагностировано более чем в 50% случаев, а у пациентов группы контроля — в трети (см. табл. 2).
При анализе выраженности депрессии по шкале HADS достоверных различий между группами также не выявлено: средний балл — 10 [8, 13] в основной группе и 6 [4, 8] в группе контроля (p=0,647).
При анализе диссомнии были выявлены статистически значимые различия: в основной группе сон был нарушен у 75% пациентов, в группе контроля — более чем у 50% (см. табл. 2).
Обсуждение
Среди пациентов, страдающих ХИГМ, жалоба на ГБ — одна из ведущих. У пациентов с хроническими нарушениями мозгового кровообращения трактовка формы цефалгического синдрома крайне сложна, поскольку в настоящее время МКГБ-3 не предполагает ее выделение в самостоятельную форму. Кроме того, частота первичных ГБ, в том числе у лиц среднего и старшего возраста, значительно превосходит распространенность вторичных цефалгий, в том числе при цереброваскулярных заболеваниях. При этом использование общепринятых терапевтических стратегий при ХИГМ часто сопровождается клиническим эффектом в отношении цефалгического синдрома, что, однако, не является поводом для исключения первичного характера ГБ, которая может нуждаться в самостоятельном лечении [8]. Результаты проведенного нами исследования демонстрируют недостаточный уровень диагностики фенотипа ГБ и игнорирование у пациентов с ХИГМ коморбидных расстройств, прежде всего тревожно-депрессивных и диссомнических, что в свою очередь приводит к использованию неоптимальных терапевтических стратегий.
Расстройства тревожно-депрессивного спектра и нарушения сна являются одними из самых частых форм коморбидных заболеваний при первичных ГБ. Так, метаанализ [9] 139 исследований с включением 4,19 млн случаев первичной ГБ выявил сопутствующую депрессию в 23%, тревогу в 25%, а нарушения сна в 48% случаев. Исследования доказали ассоциацию нарушений сна с болью, депрессией и тревогой, а также причинно-следственную связь между хронической болью и дефицитом сна [10]. У пациентов с мигренью нарушения сна не только часто отмечаются как триггеры приступов (49,8% случаев) [11], но и являются фактором хронификации заболевания. По результатам исследования [12], посвященного анализу связи мигрени и нарушений сна, у 60,5% из 1750 пациентов, страдающих мигренью, были выявлены различные варианты нарушений сна: короткая продолжительность сна, трудности засыпания, дневная сонливость, низкое качество сна, применение снотворных.
Нарушения циркадного ритма являются важной составляющей в портрете пациента не только с хронической болью, но и с тревожно-депрессивными расстройствами. При наличии ГБ значительно чаще отмечаются аномальное поведение пациентов во сне, проблемы инициирования и поддержания сна, дневная сонливость и плохая гигиена сна. Данные полисомнографии подтверждают сокращение продолжительности сна у пациентов с мигренью и ГБ напряжения. В дополнение было выявлено нарушение фаз медленного и быстрого сна при мигрени, изменение β-ритма по данным электроэнцефалографии в ночное время перед приступом мигрени, сопровождающееся снижением кортикальной активности [13].
В другом исследовании [14] был проведен анализ полисомнографических данных пациентов с ГБ и без ГБ, который показал, что нарушение дыхания во сне чаще (56,6%) встречалось при мигрени по сравнению с пациентами без ГБ. Было отмечено, что механизмы, лежащие в основе нарушений сна, расстройств эмоционального спектра, а также ГБ, являются результатом общих социально-демографических характеристик, поведенческих паттернов, вегетативной дисрегуляции. Также отмечено, что анатомические субстраты для сна и ГБ в головном мозге перекрываются, как и физиологические пути, включающие дофамин, орексин и мелатонин [15].
Эмоционально-аффективные нарушения негативно влияют на течение цефалгий, ухудшая терапевтические возможности, прогноз, качество жизни и активность пациентов, особенно пожилого возраста [16]. Тревога и депрессия являются независимыми факторами риска хронификации мигрени, ГБ напряжения и некоторых других форм цефалгий, предопределяя во многих случаях резистентность к традиционной терапии [17]. Их верификация и адекватное лечение могут существенно уменьшить бремя заболевания [18].
При нарастании частоты эпизодов цефалгий продолжающаяся тригеминальная ноцицепция, вызванная нейрогенным воспалением, связанным с CGRP, является условием прогрессирования мигрени. Продолжительная стимуляция волокон C во время повторных приступов и последующая активация волокон Aδ и сателлитных ганглиозных клеток приводит к нейрогенному нейровоспалению в тригеминоваскулярной системе, изменениям в нескольких сетях мозга, связанных как с болевыми, так и с неболевыми проявлениями [19].
В условиях хронической ишемии мозга несоответствие между энергообеспечением и потребностями мозга в энергии может служить условием для формирования или усугубления существующей ГБ. Так, на моделях мигрени изучение церебральных метаболических механизмов демонстрирует фундаментальную роль в этих процессах дисфункции митохондрий с формированием дисбаланса между повышенным мозговым метаболизмом и снижением доступности свободной клеточной энергии, что рассматривается в качестве биохимического субстрата для приступа ГБ [20]. Провоцирование ГБ такими факторами, как голодание и физические упражнения, нарушение чувствительности к инсулину и более высокий уровень инсулина в плазме натощак в межприступные периоды с пониженным его высвобождением во время приступов, также указывает на роль метаболических процессов. В межприступные периоды у страдающих мигренью выявляется гипометаболизм глюкозы в нескольких регионах, участвующих в обработке центральной боли, что коррелирует с продолжительностью заболевания и частотой ГБ [21]. Эти закономерности позволяют интерпретировать не только высокую частоту цефалгий при ХИГМ, но также и вклад различных коморбидных расстройств в формирование и поддержание болевых проявлений у данной категории пациентов.
Заключение
Таким образом, в клинической практике цефалгии при ХИГМ встречаются часто, во многих случаях остаются не диагностированными как самостоятельная нозология, а жалобы пациентов на ГБ рассматриваются в рамках ХИГМ. Наиболее частыми коморбидными расстройствами являются расстройства эмоционального спектра и нарушения сна.
Подход к терапии пациентов с ХИГМ и ГБ должен быть индивидуальным, основываться на учете всех жалоб, возможной трансформации цефалгического синдрома с возрастом, приобретении ГБ атипичных черт, выявлении сопутствующих расстройств, в том числе эмоциональных и диссомнических, которые являются одними из наиболее частых и значимых факторов, способствующих хронизации цефалгий, утяжелению приступов и ухудшению дальнейшего прогноза у пациентов старшей возрастной группы, которые страдают цереброваскулярными заболеваниями.
1The International Classification of Headache Disorders, 3rd edition (ICHD-3). Cephalalgia. 2018;38(1):1–211.